信迪利单抗联合同步放化疗用于晚期宫颈癌患者的效果论文
2024-01-01 09:31:37 来源: 作者:liyuan
摘要:目的:观察信迪利单抗联合同步放化疗用于晚期宫颈癌患者的效果。方法:选取2021—2022年该院收治的64例晚期宫颈癌患者进行前瞻性研究,按照随机数字表法将其分为对照组和观察组各32例。对照组予以同步放化疗,观察组在对照组基础上联合信迪利单抗治疗。比较两组临床疗效,治疗前后血清学指标[鳞状上皮细胞癌抗原(SCC)、血小板与淋巴细胞比值(PLR)、淋巴细胞与单核细胞比值(LMR)]水平、卡氏(KPS)评分,以及不良反应发生率。结果:观察组疾病控制率(DCR)为84.38%(27/32),高于对照组的59.38
【摘要】目的:观察信迪利单抗联合同步放化疗用于晚期宫颈癌患者的效果。方法:选取2021—2022年该院收治的64例晚期宫颈癌患者进行前瞻性研究,按照随机数字表法将其分为对照组和观察组各32例。对照组予以同步放化疗,观察组在对照组基础上联合信迪利单抗治疗。比较两组临床疗效,治疗前后血清学指标[鳞状上皮细胞癌抗原(SCC)、血小板与淋巴细胞比值(PLR)、淋巴细胞与单核细胞比值(LMR)]水平、卡氏(KPS)评分,以及不良反应发生率。结果:观察组疾病控制率(DCR)为84.38%(27/32),高于对照组的59.38%(19/32),差异有统计学意义(r<0.05);治疗后,观察组PLR、SCC水平均低于对照组,LMR水平高于对照组,差异有统计学意义(r<0.05);治疗后,观察组KPS评分高于对照组,差异有统计学意义(r<0.05);两组皮疹、肝肾功能异常、胃肠道反应、放射性膀胱炎、骨髓抑制等不良反应发生率比较,差异均无统计学意义(r>0.05)。结论:信迪利单抗联合同步放化疗用于晚期宫颈癌患者可提高DCR和KPS评分,改善血清学指标水平,效果优于单纯同步放化疗。
【关键词】晚期;宫颈癌;同步放化疗;信迪利单抗;疾病控制率;卡氏评分;不良反应
Effects of Sintilimab combined with concurrent chemoradiotherapy in treatment of patients with advanced cervical cancer【Abstract】Objective:To observe effects of Sintilimab combined with concurrent chemoradiotherapy in treatment of patients with advanced cervical cancer.Methods:A prospective study was conducted on 64 patients with advanced cervical cancer admitted to this hospital from 2021 to 2022.They were divided into control group and observation group according to the random number table method,32 cases in each group.The control group was treated with concurrent chemoradiotherapy,while the observation group was treated with Sintilimab on the basis of that of the control group.The clinical efficacy,the serological indexes[squamous cell carcinoma antigen(SCC),platelet-to-lymphocyte ratio(PLR),lymphocyte-to-monocyte ratio(LMR)]levels,the KPS score and incidence of adverse reactions were compared between the two groups before and after the treatment.Results:The disease control rate(DCR)of the observation group was 84.38%(27/32),which was higher than 59.38%(19/32)of the control group,and the difference was statistically significant(r<0.05).After the treatment,the levels of PLR and SCC in the observation group were lower than those in the control group,the level of LMR was higher than that in the control group,and the differences were statistically significant(r<0.05).After the treatment,the KPS score of the observation group was higher than that of the control group,and the difference was statistically significant(r<0.05).However,there was no significant difference in the incidence of adverse reactions such as rash,abnormal liver and kidney function,gastrointestinal reaction,radioactive cystitis and bone marrow suppression between the two groups(r>0.05).Conclusions:Sintilimab combined with concurrent chemoradiotherapy in the treatment of the patients with advanced cervical cancer can improve the DCR and KPS scores and improve the levels of serological indexes.Moreover,it is superior to single concurrent chemoradiotherapy.
【Keywords】Advanced;Cervical cancer;Concurrent chemoradiotherapy;Sintilimab;Disease control rate;Karnofsky score;Adverse reaction
宫颈癌是临床妇科常见的恶性肿瘤,其发病率和病死率均较高[1]。早期宫颈癌患者优先采用手术治疗,对于晚期或出现远处转移的患者,临床常采取保守治疗[2-3]。同步放化疗是常用的保守治疗手段,可抑制癌细胞生长,控制病情进展,但患者仍存在一定的复发风险[4]。信迪利单抗属于免疫治疗药物,可与程序性死亡配体-1(PD-L1)受体结合,阻断其介导的免疫抑制反应,增高抗肿瘤效果[5]。本文观察信迪利单抗联合同步放化疗用于晚期宫颈癌患者的效果。

1资料与方法
1.1一般资料选取2021—2022年本院收治的64例晚期宫颈癌患者进行前瞻性研究。纳入标准:符合《宫颈癌诊疗规范(2018年版)》中晚期宫颈癌诊断标准[6];经组织病理学检查确诊;卡氏(KPS)评分>60分,可耐受放化疗;意识清楚,可配合研究;PD-L1表达阳性。排除标准:合并其他恶性肿瘤;预计生存期<3个月;合并严重肝、肾功能衰竭;发生远处转移。患者均知情本研究内容并签署知情同意书,本研究经本院医学伦理委员会批准。按照随机数字表法将其分为观察组和对照组各32例。观察组年龄37~74岁,平均(55.91±7.28)岁;体质量40~77 kg,平均(59.22±6.74)kg;病理类型:腺癌20例,鳞状细胞癌12例;临床分期:Ⅲ期19例,Ⅳ期13例。对照组年龄37~76岁,平均(56.19±7.37)岁;体质量40~78 kg,平均(59.56±6.91)kg;病理类型:腺癌21例,鳞状细胞癌11例;临床分期:Ⅲ期20例,Ⅳ期12例。两组一般资料比较,差异无统计学意义(P>0.05),有可比性。
1.2方法对照组予以同步放化疗。(1)放疗:采用6MV医用直线加速器,常规设野,全盆腔外照射1.8 Gy/次,5次/周,肿瘤组织吸收量45.0~50.4 Gy(25~28次);后改为盆腔四野外照射,肿瘤组织吸收量50.4~54.0 Gy(28~30次)。(2)化疗:第1天,予以紫杉醇注射液(扬子江药业集团有限公司,国药准字H20053001,5 mL∶30 mg)135 mg/m2,静脉滴注;第1~3天,予以顺铂注射液(江苏豪森药业集团有限公司,国药准字H20040813,6 mL∶30 mg)60 mg/m2,静脉滴注,21 d为1个周期。
观察组在对照组基础上联合信迪利单抗注射液[信达生物制药(苏州)有限公司,国药准字S20180016,100 mg)]治疗。化疗第1天使用,200 mg/次,静脉滴注,21 d为1个周期。
两组均连续治疗2个周期。
1.3观察指标(1)比较两组临床疗效。疗效标准参照《实体瘤治疗疗效评价标准-RECIST》[7],完全缓解(CR):病灶彻底消失,且维持≥4周;部分缓解(PR):病灶缩小≥50%,且维持≥4周;疾病稳定(SD):病灶缩小<50%或增大<25%;疾病进展(PD):病灶增大≥25%,或出现新发病灶。疾病控制率(DCR)=(CR+PR+SD)例数/总例数×100%。(2)比较两组治疗前后血清学指标水平。采集患者空腹静脉血3 mL,以3000 r/min,离心半径15 cm,离心10 min,留取血清,采用微粒子酶免疫分析法检测鳞状上皮细胞癌抗原(SCC)水平,采用血细胞分析仪检测血小板与淋巴细胞比值(PLR)、淋巴细胞与单核细胞比值(LMR)。(3)比较两组治疗前后KPS评分。KPS总分100分,评分越高表明健康状况越好。(4)比较两组不良反应发生率。
1.4统计学方法采用SPSS 22.0统计学软件处理数据,计量资料以(x(—)±s)表示,采用t检验,计数资料以率(%)表示,采用χ2检验,以P<0.05为差异有统计学意义。
2结果
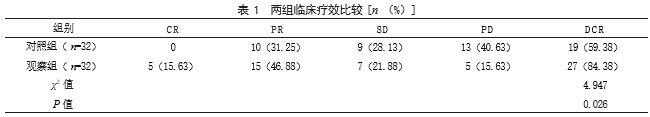
2.1两组临床疗效比较观察组DCR为84.38%(27/32),高于对照组的59.38%(19/32),差异有统计学意义(P<0.05)。见表1。
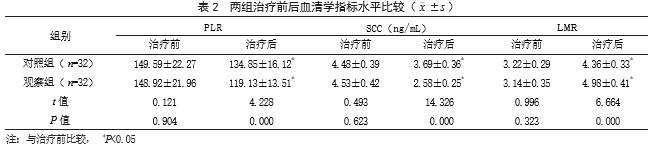
2.2两组治疗前后血清学指标水平比较治疗前,两组PLR、SCC、LMR水平比较,差异均无统计学意义(P>0.05);治疗后,两组PLR、SCC水平均低于治疗前,且观察组低于对照组,两组LMR水平均高于治疗前,且观察组高于对照组,差异有统计学意义(P<0.05)。见表2。
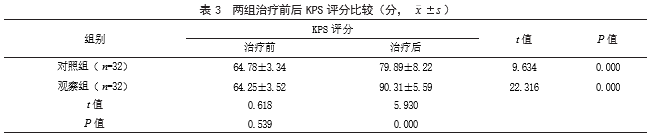
2.3两组治疗前后KPS评分比较治疗前,两组KPS评分比较,差异无统计学意义(P>0.05);治疗后,两组KPS评分均高于治疗前,且观察组高于对照组,差异有统计学意义(P<0.05)。见表3。
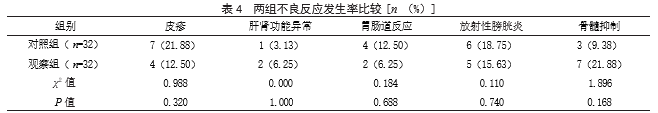
2.4两组不良反应发生率比较两组皮疹、肝肾功能异常、胃肠道反应、放射性膀胱炎、骨髓抑制等不良反应发生率比较,差异均无统计学意义(P>0.05)。见表4。
3讨论
宫颈癌的发病机制较为复杂,常由高危型人乳头瘤病毒感染引起,患者早期无明显体征,随病情进展可出现盆腔疼痛、阴道流血等症状,该病进展速度快,大部分患者确诊时已处于晚期,错失手术时机[8]。目前,同步放化疗已成为晚期宫颈癌患者的标准治疗手段,但效果具有个体差异性,因此寻找更加高效的治疗方案是临床研究的重难点[9]。
程序性死亡受体-1(PD-1)是免疫细胞表面受体,肿瘤细胞表面主要表达PD-L1,二者结合可使肿瘤细胞逃避免疫系统的攻击,导致肿瘤快速增殖、转移[10]。抗PD-L1治疗是一种新型肿瘤免疫疗法,在多种实体瘤的治疗中效果显著。
PLR高表达提示肿瘤新生血管增多。SCC水平升高可促进癌细胞浸润和转移。LMR水平越低提示肿瘤负荷越大,免疫抑制越严重[11]。本研究结果显示,观察组DCR和LMR水平均高于对照组,PLR、SCC水平均低于对照组。提示信迪利单抗联合同步放化疗用于晚期宫颈癌患者可提高治疗效果,改善血清学指标水平。分析原因为信迪利单抗属于PD-L1抑制剂,可阻断PD-1与PD-L1的结合,恢复免疫系统功能,增强对肿瘤细胞的杀灭能力,发挥较好的抗肿瘤作用,进而调节PLR、SCC、LMR水平[12]。
本研究结果还显示,观察组治疗后KPS评分高于对照组。分析原因为信迪利单抗可调节机体免疫功能,解除免疫抑制效应,增强对肿瘤细胞的杀伤能力,进而抑制病情进展,改善患者健康状况[13]。本研究结果同时显示,两组皮疹、肝肾功能异常、胃肠道反应、放射性膀胱炎、骨髓抑制等不良反应发生率比较,差异均无统计学意义。提示联合信迪利单抗用药未增加安全风险。
综上所述,信迪利单抗联合同步放化疗用于晚期宫颈癌患者可提高DCR和KPS评分,改善血清学指标水平,效果优于单纯同步放化疗。
参考文献
[1]Corbeau A,KuipersSC,de Boer SM,et al.Correlations between bone marrow radiation dose and hematologic toxicity in locally advanced cervical cancer patients receiving chemoradiation with cisplatin:asystematic review[J].RadiotherOncol,2021(164):128-137.
[2]肖鑫,盛晓安,施险峰,等.热疗联合同步放化疗对中晚期宫颈癌的临床疗效及血清热休克蛋白90α表达的影响[J].中华全科医学,2022,20(7):1109-1112.
[3]Benson R,Pathy S,Kumar L,et al.Locally advanced cervical cancer-neoadjuvant chemotherapy followed by concurrent chemoradiation and targeted therapy as maintenance:a phase II study[J].J Cancer Res Ther,2019,15(6):1359-1364.
[4]刘昵,刘新福,陈忠东.同步热放化疗治疗中晚期宫颈癌的效果及对细胞增殖凋亡相关蛋白表达的影响[J].实用癌症杂志,2020,35(3):363-365.
[5]冯成军,张日光,韦蒙专.信迪利单抗联合同步放化疗对晚期宫颈癌患者肿瘤标志物及程序性死亡受体-1/程序性死亡配体1的影响[J].中华实用诊断与治疗杂志,2022,36(7):740-743.
[6]中华人民共和国国家卫生健康委员会.宫颈癌诊疗规范(2018年版)[J].肿瘤综合治疗电子杂志,2020,6(3):33-43.
[7]杨学宁,吴一龙.实体瘤治疗疗效评价标准-RECIST[J].循证医学,2004,4(2):85-90.
[8]张贤雨,马欢,席强,等.局部晚期宫颈癌患者同步放化疗后应用TP方案巩固化疗效果及血清miR-155、miR-24水平变化[J].山东医药,2020,60(29):43-45.
[9]朱园园,张兰胜,张璐,等.同步放化疗联合热疗与同步放化疗治疗局部晚期宫颈癌的有效性和安全性比较[J].现代肿瘤医学,2020,28(21):3771-3775.
[10]邵莎莎,曹丽艳,王光霞,等.抗PD-1/PD-L1免疫疗法联合同步放化疗治疗局部晚期宫颈癌的临床效果[J].中国医师杂志,2022,24(6):916-921.
[11]Xu Q,Wang J,Sun Y,et al.Efficacy and safety of sintilimab plus anlotinib for PD-L1-Positive recurrent or metastatic cervical cancer:a multicenter,single-arm,prospective phase II trial[J].J Clin Oncol,2022,40(16):1795-1805.
[12]何宁宁,汪善兵,任粤,等.程序性死亡蛋白-1/程序性死亡蛋白配体-1抑制剂治疗宫颈癌的进展[J].四川医学,2021,42(7):741-745.
[13]郝晓慧,张志林,卢秀荣,等.信迪利单抗静注联合全身化疗治疗复发转移宫颈癌的临床疗效观察[J].山东医药,2022,62(5):78-81.










