卵巢癌新辅助化疗联合肿瘤细胞减灭术后患者复发的影响因素论文
2026-05-07 11:03:18 来源: 作者:xuling
摘要:临床分期为Ⅲ~Ⅳ期、BRCA-1阳性、无术中淋巴结清扫、残留病灶直径>1 cm、术前HE4>400 pmol/L、术后2个月CA125>35 U/L均为卵巢癌新辅助化疗联合肿瘤细胞减灭术后患者复发的危险因素。
【摘要】目的:分析卵巢癌新辅助化疗联合肿瘤细胞减灭术后患者复发的影响因素。方法:选取2023—2024年该院收治的116例卵巢癌患者进行横断面研究,收集患者一般资料,术后随访1年,根据术后是否复发将其分为复发组与未复发组,采用Logistic回归分析卵巢癌新辅助化疗联合肿瘤细胞减灭术后患者复发的影响因素。结果:116例卵巢癌新辅助化疗联合肿瘤细胞减灭术后患者复发67例,占57.76%;两组年龄、居住地、肿瘤分化程度、组织分型、淋巴结转移占比比较,差异均无统计学意义(P>0.05);复发组临床分期为Ⅲ~Ⅳ期、乳腺癌易感基因-1(BRCA-1)阳性、无术中淋巴结清扫、残留病灶直径>1 cm、术前人附睾蛋白4(HE4)>400 pmol/L、术后2个月糖类抗原125(CA125)>35 U/L占比均高于未复发组,差异有统计学意义(P<0.05);Logistic回归分析结果显示,临床分期为Ⅲ~Ⅳ期、BRCA-1阳性、无术中淋巴结清扫、残留病灶直径>1 cm、术前HE4>400 pmol/L、术后2个月CA125>35 U/L均为卵巢癌新辅助化疗联合肿瘤细胞减灭术后患者复发的危险因素(OR>1,P<0.05)。结论:临床分期为Ⅲ~Ⅳ期、BRCA-1阳性、无术中淋巴结清扫、残留病灶直径>1 cm、术前HE4>400 pmol/L、术后2个月CA125>35 U/L均为卵巢癌新辅助化疗联合肿瘤细胞减灭术后患者复发的危险因素。
【关键词】卵巢癌;化疗;肿瘤细胞减灭术;复发;影响因素
卵巢癌发病率在女性生殖系统恶性肿瘤中位居前列,严重威胁患者生命健康[1]。尽管以新辅助化疗联合肿瘤细胞减灭术的综合治疗方案已在临床广泛应用,显著延长了患者生存期,但部分术后患者1年内即出现复发,为临床诊疗带来巨大压力[2-3]。本文分析卵巢癌新辅助化疗联合肿瘤细胞减灭术后患者复发的影响因素。
1资料与方法
1.1一般资料选取2023—2024年本院收治的116例卵巢癌患者进行横断面研究。纳入标准:符合卵巢癌诊断标准[4];经病理检查确诊;进行新辅助化疗联合肿瘤细胞减灭术治疗;意识清楚,具备基本沟通能力。排除标准:合并严重心、肺、肝、肾功能不全;合并凝血功能障碍;合并其他原发性恶性肿瘤或既往5年内有恶性肿瘤病史。
1.2方法
1.2.1一般资料收集通过电子病历系统收集患者一般资料,包括年龄(>50岁、≤50岁)、居住地(城市、农村)、肿瘤分化程度(低分化、中高分化)、临床分期(Ⅱ期、Ⅲ~Ⅳ期)、组织分型(浆液性、黏液性、其他)、乳腺癌易感基因-1(BRCA-1)(阳性、阴性)、淋巴结转移(有、无)、术中淋巴结清扫(有、无)、残留病灶直径(>1 cm、≤1 cm)。
术前,采集患者清晨空腹肘静脉血2 mL,以3000 r/min,离心半径10cm,离心10 min,留取血清,采用酶联免疫吸附法检测人附睾蛋白4(HE4)水平;术后2个月,采集患者空腹静脉血2 mL,常规离心后取血清,采用酶联免疫吸附法检测糖类抗原125(CA125)水平。
1.2.2卵巢癌复发判定术后随访1年,进行腹部增强CT检查,若发现原手术区域、盆腔、腹腔或远处部位出现新发占位性病灶,则视为卵巢癌复发。
1.3观察指标(1)统计卵巢癌新辅助化疗联合肿瘤细胞减灭术后患者复发情况,根据是否复发将其分为复发组与未复发组。(2)卵巢癌新辅助化疗联合肿瘤细胞减灭术后患者复发的单因素分析。(3)卵巢癌新辅助化疗联合肿瘤细胞减灭术后患者复发的Logistic回归分析。
1.4统计学方法采用SPSS 24.0统计学软件处理数据,计数资料以率(%)表示,采用χ2检验,影响因素分析采用Logistic回归分析,以P<0.05为差异有统计学意义。
2结果
2.1卵巢癌新辅助化疗联合肿瘤细胞减灭术后患者复发情况116例卵巢癌新辅助化疗联合肿瘤细胞减灭术后患者复发67例,占57.76%;未复发49例。
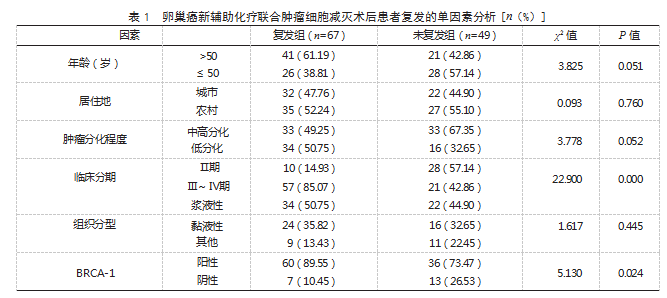
2.2卵巢癌新辅助化疗联合肿瘤细胞减灭术后患者复发的单因素分析两组年龄、居住地、肿瘤分化程度、组织分型、淋巴结转移占比比较,差异均无统计学意义(P>0.05);复发组临床分期为Ⅲ~Ⅳ期、BRCA-1阳性、无术中淋巴结清扫、残留病灶直径>1 cm、术前HE4>400 pmol/L、术后2个月CA125>35 U/L占比均高于未复发组,差异有统计学意义(P<0.05)。见表1。
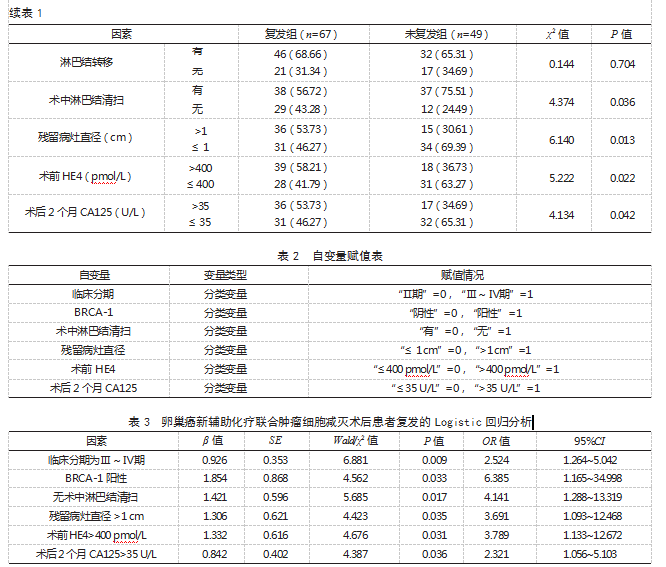
2.3卵巢癌新辅助化疗联合肿瘤细胞减灭术后患者复发的Logistic回归分析将卵巢癌新辅助化疗联合肿瘤细胞减灭术后患者复发情况作为因变量(复发=1,未复发=0),将表1中P<0.05的因素作为自变量,赋值见表2。Logistic回归分析结果显示,临床分期为Ⅲ~Ⅳ期、BRCA-1阳性、无术中淋巴结清扫、残留病灶直径>1 cm、术前HE4>400 pmol/L、术后2个月CA125>35 U/L均为卵巢癌新辅助化疗联合肿瘤细胞减灭术后患者复发的危险因素(OR>1,P<0.05)。见表3。
3讨论
卵巢癌早期症状隐匿,确诊时多进展至中晚期,预后较差,规范化治疗是提高患者生存率的关键[5-6]。新辅助化疗联合肿瘤细胞减灭术可清除原发灶及转移灶,抑制肿瘤细胞扩散[7]。本研究结果显示,116例卵巢癌新辅助化疗联合肿瘤细胞减灭术后患者复发67例,占57.76%。提示卵巢癌新辅助化疗联合肿瘤细胞减灭术后患者复发风险较高。
本研究Logistic回归分析结果显示,临床分期为Ⅲ~Ⅳ期、BRCA-1阳性、无术中淋巴结清扫、残留病灶直径>1 cm、术前HE4>400 pmol/L、术后2个月CA125>35 U/L均为卵巢癌新辅助化疗联合肿瘤细胞减灭术后患者复发的危险因素。分析原因:(1)临床分期为Ⅲ~Ⅳ期。临床分期为Ⅲ~Ⅳ期患者疾病进展已达中晚期,此阶段肿瘤多突破卵巢局限,侵犯盆腔、腹腔脏器甚至出现远处转移,手术难以彻底清除所有病灶,残留肿瘤细胞易复发,同时晚期患者肿瘤细胞增殖活性更强,对化疗的耐药性更高[8-9];此外晚期患者免疫功能普遍受损,无法有效监视和清除肿瘤细胞,进一步增加术后复发风险。对此,应建立个性化随访体系,术后前3个月每月复查肿瘤标志物及盆腔超声,强化患者遵医意识,并做好症状管理。(2)BRCA-1阳性。BRCA-1是DNA损伤修复的关键基因,阳性状态下其功能缺陷可导致肿瘤细胞DNA双链断裂修复能力降低,修复机制异常可加速肿瘤细胞基因突变累积,快速产生化疗耐药性,使微小残留病灶难以被持续清除,因此术后复发风险较高[10]。对此,应建立基因靶向随访机制,除常规监测外,增加BRCA-1基因甲基化状态复查,每2个月进行1次循环肿瘤DNA检测,实现复发早预警。(3)无术中淋巴结清扫。卵巢癌具有早期沿淋巴途径转移的特性,残留淋巴结病灶可持续释放肿瘤相关因子,削弱机体抗肿瘤免疫应答,降低化疗对微小病灶的清除效率,加速肿瘤细胞耐药性产生[11-12];未清扫的淋巴结可破坏局部免疫微环境,导致免疫细胞无法有效识别和杀灭肿瘤细胞,最终导致复发。对此,应聚焦残留病灶监测与免疫增强,指导患者每日进行30 min舒缓运动,搭配富含膳食纤维的饮食,调节免疫细胞活性。(4)残留病灶直径>1 cm。较大残留病灶内所含的肿瘤细胞数量远超微小病灶,化疗仅能杀灭部分肿瘤细胞,剩余肿瘤细胞易进入休眠状态规避治疗,待药物作用减弱后可重新激活增殖[13]。同时较大残留病灶在化疗压力下更易产生耐药基因突变,导致后续治疗效果下降,增加术后复发风险[14]。对此,应建立双维度监测体系,术后复查腹部增强CT,精准追踪病灶大小变化,同步增加血清乳酸脱氢酶检测,提前预警病灶活性。(5)术前HE4>400 pmol/L。HE4作为卵巢癌特异性肿瘤标志物,其水平与肿瘤细胞增殖活性、分化程度直接相关。术前HE4>400 pmol/L提示肿瘤可能已突破局部局限,存在微小转移灶或隐匿性浸润,手术难以完全清除[15]。同时HE4水平升高常伴随肿瘤细胞耐药相关基因表达增强,增加术后复发风险。对此,应建立HE4靶向随访体系,若指标持续异常升高,应及时联合盆腔增强磁共振成像检查进行排查。(6)术后2个月CA125>35 U/L。卵巢癌患者术后规范化疗后,CA125可在1~2个月内降至正常范围,若此时仍高于35 U/L,提示肿瘤细胞未被完全清除,仍在持续增殖[16]。同时,持续升高的CA125还反映出机体抗肿瘤免疫应答不足的现状,因此术后复发风险较高。对此,建议同步结合阴道超声检查评估盆腔情况,提升复发预警的准确性。
综上所述,临床分期为Ⅲ~Ⅳ期、BRCA-1阳性、无术中淋巴结清扫、残留病灶直径>1 cm、术前HE4>400 pmol/L、术后2个月CA125>35 U/L均为卵巢癌新辅助化疗联合肿瘤细胞减灭术后患者复发的危险因素。
参考文献
[1]ZHANG R,SIU M K Y,NGAN H Y S,et al.Molecular Biomarkers for the Early Detection of Ovarian Cancer[J].Int J Mol Sci,2022,23(19):12041.
[2]ARONSON S L,LOPEZ-YURDA M,KOOLE S N,et al.Cytoreductive surgery with or without hyperthermic intraperitoneal chemotherapy in patients with advanced ovarian cancer(OVHIPEC-1):final survival analysis of a randomised,controlled,phase 3 trial[J].Lancet Oncol,2023,24(10):1109-1118.
[3]FILIS P,MAURI D,MARKOZANNES G,et al.Hyperthermic intraperitoneal chemotherapy(HIPEC)for the management of primary advanced and recurrent ovarian cancer:a systematic review and meta-analysis of randomized trials[J].ESMO Open,2022,7(5):100586.
[4]中国抗癌协会妇科肿瘤专业委员会.卵巢恶性肿瘤诊断与治疗指南(第四版)[J].中国实用妇科与产科杂志,2018,34(7):739-749.
[5]鲍群丽,万淑琼,黄耿,等.miR-1277-5p通过调控PHF8对卵巢癌SKOV-3细胞增殖和凋亡的影响[J].国际医药卫生导报,2021,27(20):3153-3157.
[6]MAHONEY D E,PIERCE J D.Ovarian Cancer Symptom Clusters:Use of the NIH Symptom Science Model for Precision in Symptom Recognition and Management[J].Clin J Oncol Nurs,2022,26(5):533-542.
[7]朱连成,林蓓.新辅助化疗对卵巢癌肿瘤细胞减灭术手术结局的影响[J].中国实用妇科与产科杂志,2023,39(7):706-711.
[8]朱艳红,蔡玉洁,葛银.上皮性卵巢癌术后复发的相关影响因素分析[J].实用癌症杂志,2022,37(1):117-119.
[9]彭光彩,周锦红,曾淑梅,等.二次肿瘤细胞减灭术联合化疗治疗复发性卵巢癌的预后与影响因素分析[J].中华内分泌外科杂志,2021,15(3):243-247.
[10]陈燕荣,武明娟,刘冰,等.卵巢癌患者肿瘤细胞减灭术后复发的影响因素[J].实用临床医药杂志,2022,26(15):103-108.
[11]金雯,李宇,王雯智,等.上皮性卵巢癌患者肿瘤细胞减灭术后复发的列线图预测模型构建[J].临床肿瘤学杂志,2024,29(10):988-992.
[12]贾颖娜,郑翠,何慧,等.卵巢癌组织中线粒体融合蛋白2对初次肿瘤细胞减灭术后复发的预测价值[J].标记免疫分析与临床,2024,31(10):1907-1912.
[13]梅金枝.早期上皮性卵巢癌患者腹腔镜术后复发的危险因素及风险预测模型构建[J].河南医学研究,2025,34(12):2183-2186.
[14]郝鑫,马丽丽,高松硕.血清HE4、TM4SF1、HSP90α预测卵巢癌患者术后复发价值[J].中国计划生育学杂志,2024,32(9):2165-2169.
[15]左尔比亚·买买提,古再力努尔·艾白,阿斯木古丽·克力木.动态监测HE4、Smad4、HGF预测卵巢癌外科术后早期复发的价值[J].分子诊断与治疗杂志,2021,13(8):1345-1348.
[16]牟姗,范凌晔,刘洁曦,等.血清人附睾蛋白和癌抗原125联合预测上皮性卵巢癌术后复发的价值分析[J].川北医学院学报,2023,38(10):1362-1366.










