新生儿肺炎的危险因素研究论文
2026-04-18 15:55:24 来源: 作者:xuling
摘要:羊水污染和出生1 min Apgar评分≤7分是新生儿肺炎发生的独立危险因素,预防性应用抗菌药物可降低其发生风险。
[摘要]目的探讨新生儿肺炎的主要危险因素,并构建风险评估模型,旨在为临床早期识别、干预及预防策略的制定提供循证依据。方法回顾性收集2022年5月—2025年5月太仓市第一人民医院收治的197例新生儿的临床资料,按是否伴有新生儿肺炎将研究对象分为两组:未发生新生儿肺炎的152例为未发生组,发生新生儿肺炎的45例为发生组。收集一般人口学资料、围产期相关资料。通过单因素、多因素二元Logistic回归分析发生新生儿肺炎的独立危险因素。结果两组胎膜早破、羊水污染、预防性应用抗菌药物、出生1 min Ap⁃gar评分相比,差异均有统计学意义(P均<0.05)。多因素二元Logistic回归结果显示,羊水污染和出生1 min Apgar评分≤7分是新生儿肺炎的独立危险因素,差异均有统计学意义(OR=5.045,9.967;P均<0.05),预防性应用抗菌药物为新生儿肺炎的独立保护因素,差异有统计学意义(OR=0.440,P<0.05)。结论羊水污染和出生1 min Apgar评分≤7分是新生儿肺炎发生的独立危险因素,预防性应用抗菌药物可降低其发生风险。
[关键词]新生儿;肺炎;危险因素;Logistic回归分析
新生儿肺炎是新生儿期最常见且严重的感染性疾病之一,发病率居高不下[1]。由于新生儿免疫系统发育尚不完善,呼吸道防御功能不足,一旦受到病原体侵袭,极易引发急性炎症反应,导致呼吸窘迫甚至多器官功能损伤[2]。尽管现代新生儿重症监护水平显著提升,抗菌药物及呼吸支持治疗不断进步,但新生儿肺炎仍是导致新生儿住院和死亡的重要原因,还可能造成长期的呼吸系统和神经系统后遗症[3]。临床上,新生儿肺炎的病因复杂,既涵盖产前母体感染、宫内窘迫、羊水污染等围产期因素,又包括出生后的环境暴露和护理因素[4]。早期识别高危新生儿并进行针对性干预,是降低疾病发生率、改善预后的关键。然而,目前针对新生儿肺炎危险因素的研究缺乏系统性分析和基于多因素的预测模型,临床在风险评估与防控策略制定方面仍存在不足。因此,本研究旨在通过多因素Logistic回归方法分析影响新生儿肺炎的独立影响因素,为临床提供更科学的早期预防与干预依据。
1资料与方法
1.1一般资料
回顾性收集2022年5月—2025年5月太仓市第一人民医院收治的197例新生儿的临床资料,按是否伴有新生儿肺炎将研究对象分为两组:未发生新生儿肺炎的152例为未发生组,发生新生儿肺炎的45例为发生组。本研究已通过太仓市第一人民医院医学伦理委员会的批准(TCS202501)。
1.2纳入与排除标准
纳入标准:发生组为经临床、实验室检查及胸部X线检查确诊的新生儿肺炎;均为出生后28d以内;入院时具有完整的病历资料和围产期信息;母亲孕期和分娩资料可完整追溯;均为单胎出生;入院时,监护人签署知情同意书并知情同意本研究。
排除标准:合并严重先天畸形或遗传代谢性疾病(如先天性心脏病、染色体异常等)新生儿;出生后即确诊为其他严重呼吸系统疾病(如先天性肺发育不良、肺囊性疾病)新生儿;合并免疫缺陷或严重血液系统疾病新生儿;入院前已接受系统性抗生素治疗超过48 h者;临床资料不完整新生儿。
1.3资料收集方法
收集两组一般人口学资料及围产期相关资料,包括性别、胎龄、出生体质量、早产、胎膜早破、羊水污染、母体生殖道感染、预防性应用抗菌药物、静脉营养支持、住院时间、剖宫产分娩、妊娠期糖尿病、胆汁淤积及新生儿出生1 min Apgar评分。其中,母体生殖道感染及羊水污染参照《妇产科学》(第9版)[5]相关诊断标准,母体生殖道感染以病原菌培养阳性为判定依据;羊水污染根据羊水颜色及性状分为3度:Ⅰ度为微黄色或淡绿色,Ⅱ度为黄绿色或深绿色,Ⅲ度为棕黄色、稠厚呈糊状并可见颗粒物。胎膜早破参照《ACOG实践指南第188号:胎膜早破》[6]相关诊断标准进行判定。出生1 min Apgar评分[7]于出生后1 min进行评估,依据心率、呼吸、肌张力、反射反应及皮肤颜色五个项目进行评分,每项按0分、1分、2分分级,总分0~10分。
1.4观察指标
单因素分析:比较两组性别、胎龄、出生体质量、早产、胎膜早破、羊水污染、母体生殖道感染、预防性应用抗菌药物、静脉营养支持、住院时间、剖宫产分娩、妊娠期糖尿病、胆汁淤积及新生儿出生1 min Apgar评分。
多因素分析:采用多因素二元Logistic回归方法分析新生儿发生肺炎的独立影响因素。
1.5统计方法
采用SPSS 23.0统计学软件处理数据,胎龄、出生体质量等为计量资料,经Shapiro-Wilk检验符合正态分布,以(x-±s)表示,组间比较行两独立样本t检验。性别、早产等为计数资料,以例数(n)和率(%)表示,组间比较行χ2检验。采用多因素二元Logistic回归模型分析新生儿发生肺炎的独立影响因素。P<0.05为差异有统计学意义。
2结果
2.1新生儿发生肺炎的单因素分析
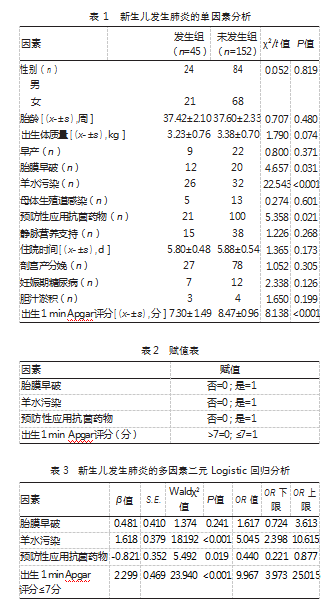
两组新生儿胎膜早破、羊水污染、预防性应用抗菌药物、出生1 min Apgar评分相比,差异均有统计学意义(P均<0.05);两组新生儿性别、胎龄、出生体质量、早产、母体生殖道感染、静脉营养支持、住院时间、剖宫产分娩、妊娠期糖尿病、胆汁淤积相比,差异均无统计学意义(P均>0.05)。见表1。
2.2新生儿发生肺炎的多因素二元Logistic回归分析
以新生儿是否发生肺炎为因变量(发生=1;未发生=0),将表1单因素分析结果作为自变量,对上述因素进行赋值,见表2。多因素二元Logistic回归分析结果显示,羊水污染、出生1 min Apgar评分≤7分是新生儿肺炎的独立危险因素;预防性应用抗菌药物为保护因素,差异均有统计学意义(P均<0.05)。见表3。
3讨论
新生儿肺炎是新生儿期的常见疾病,也是导致新生儿死亡的重要原因。尽管近年来围产期保健水平持续提升,但其发病风险在部分高危人群中仍较为突出。因此,早期识别相关危险因素并构建预测模型,对开展针对性防控具有重要意义[8-9]。本研究通过多因素分析发现,羊水污染和出生1 minApgar评分≤7分是新生儿肺炎的独立危险因素,而预防性应用抗菌药物则为保护因素。
本研究结果显示,新生儿肺炎发生组的胎膜早破、羊水污染比例高于未发生组,预防性应用抗菌药物的比例则显著低于未发生组,同时发生组出生1 min Apgar评分低于未发生组(P均<0.05)。进一步的多因素二元Logistic回归分析表明,羊水污染是新生儿肺炎的独立危险因素(OR=5.045),这与钱睿源等[8]基于全国多中心数据的研究结果一致,该研究指出羊水粪染可使新生儿肺炎风险增加2.3倍。此外,ÖKTEM A等[10]通过肺超声研究证实,羊水污染的新生儿中肺部炎症征象检出率显著升高,进一步支持了本研究结论。羊水污染与新生儿肺炎的关联机制可能涉及2个方面:①污染的羊水中可能存在病原微生物,胎儿吸入后可直接引发肺部感染;②羊水污染,尤其是胎粪污染,可诱发化学性炎症及气道阻塞,为细菌繁殖创造条件,从而增加肺炎发生风险[10-11]。出生1 minApgar评分≤7分通常提示新生儿存在围产期窒息、应激或生理功能抑制状态[12]。本研究发现,出生1 min Apgar评分≤7分也是新生儿肺炎的独立危险因素(OR=9.967),这与沈文文等[9]的研究结果相互印证,后者发现Apgar评分≤7分者的血清25-OH-D水平显著降低,且免疫球蛋白G、补体第三成分水平下降,提示免疫抑制状态可能是感染易感性增加的机制之一。本研究还显示,预防性应用抗菌药物对新生儿肺炎具有一定保护作用(OR=0.440),这与邓春香等[13]的研究结果一致,该研究发现羊水Ⅲ度污染的新生儿预防性使用抗生素可使肺炎发生率从28.6%降至12.3%。因此,临床上对存在羊水污染等高危因素的新生儿,早期、合理的抗菌药物干预可能抑制细菌增殖,阻断感染进程。不过,需严格掌握用药指征,避免无序使用导致耐药性或微生态紊乱[14]。
综上所述,产科与新生儿科协作中需重点关注以下环节:①加强产时监护,积极处理羊水污染及胎儿窘迫问题,降低新生儿吸入风险;②对出生1 min Apgar评分≤7分的新生儿,出生后尽早开展呼吸支持与感染评估;③针对有明确高危因素的患儿,可在权衡利弊后考虑预防性抗菌治疗。本研究存在一定局限性,包括单中心回顾性设计、样本量有限。未来应开展多中心、前瞻性研究,整合产前、产时多项指标,构建更精准的风险预测模型,并对其临床适用性进行验证与优化,从而推动新生儿肺炎的早期分层干预及医疗资源的合理配置。
[参考文献]
[1]孙鹏超,郑凌云.新生儿肺炎的抗生素临床应用进展[J].继续医学教育,2021,35(9):160-162.
[2]ANDRÉS SP,MONTERO GJ,VÁZQUEZ NL,et al.Neo⁃natal lung ultrasound:Early diagnosis of necrotizing pneumonia[J].An Pediatr(Engl Ed),2024,100(2):155-157.
[3]秦华均,王启义,李长金.持续呼吸道正压通气联合纳洛酮治疗新生儿肺炎的临床疗效分析[J].实用临床医药杂志,2017,21(11):220-221,226.
[4]刘弦,杭杲,胡金绘,等.1 135例新生儿呼吸困难的病因、特点和危险因素分析[J].中国医药导报,2019,16(36):100-103.
[5]谢幸,孔北华,段涛,等.妇产科学[M].9版.北京:人民卫生出版社,2018,47-52.
[6]Prelabor rupture of membranes:ACOG practice bulletin,number 217[J].Obstet Gynecol,2020,135(3):e80-e97.
[7]American academy of pediatrics committee on fetus and newborn,American college of obstetricians and gynecolo⁃gists committee on obstetric practice.The Apgar score[J].Pediatrics,2015,136(4):819-822.
[8]钱睿源,吴薇,芦亚娟,等.新生儿肺炎的危险因素及预测模型构建[J].中华医院感染学杂志,2025,35(11):1670-1673.
[9]沈文文,姚小龙,王茜,等.新生儿肺炎血清25-羟维生素D水平检测及对其预后的预测价值[J].中国实验诊断学,2024,28(8):909-914.
[10]ÖKTEM A,ZENCIROĞLU A,ÜNERÇ,et al.Effi⁃ciency of lung ultrasonography in the diagnosis and follow-up of viral pneumonia in newborn[J].Am J Peri⁃natol,2023,40(4):432-437.
[11]ALANEZI G,ALMULHEM A,ALDRIWESH M,et al.A triple antimicrobial regimen for multidrug-resistant Klebsiella pneumonia in a neonatal intensive care unit outbreak:A case series[J].J Infect Public Health,2022,15(1):138-141.
[12]RAZAZ N.From soranus score to apgar score[J].Acta Paediatr,2021,110(3):746-747.
[13]邓春香.应用抗生素对重度羊水污染新生儿肺炎发生率的影响[J].临床合理用药,2023,16(5):140-142.
[14]孟瑶,丁翊君,王晓玲,等.抗菌药物管理项目对减少新生儿肺炎抗菌药物使用的质量改进研究[J].中国循证儿科杂志,2023,18(4):272-575.










