齐墩果酸通过诱导铁死亡对卵巢癌细胞恶性生物学行为的影响论文
2026-04-18 11:40:32 来源: 作者:xuling
摘要:OA可通过诱导卵巢癌A2780、HO-8910细胞细胞铁死亡从而抑制其恶性生物学行为,其机制与下调NRF2、HO-1、GPX4、SLC7A11蛋白表达水平有关。
[摘要]目的探讨齐墩果酸(oleanolic acid,OA)通过诱导铁死亡对卵巢癌A2780、HO-8910细胞恶性生物学行为的影响及其机制。方法选取2025年7—10月牡丹江医科大学体外培养的卵巢癌A2780、HO-8910细胞,分别分为5组,对照组(常规培养)、OA低浓度组(30μmol/L)、OA中浓度组(60μmol/L)、OA高浓度组(120μmol/L)和OA+铁抑素-1(ferrostatin-1,Fer-1)组(OA 120μmol/L+Fer-1 30 nmol/L)。分别以细胞计数试剂盒-8、划痕实验、Transwell实验检测细胞增殖、迁移和细胞侵袭能力,比色法检测亚铁离子(Fe2+)、丙二醛(malo-ndialdehyde,MDA)和谷胱甘肽(glutathione,GSH)水平,Western blot实验检测核因子E2相关因子2(nuclear factor erythroid 2-related factor 2,NRF2)、血红素加氧酶1(heme oxygenase-1,HO-1)和谷胱甘肽过氧化物酶4(glutathione peroxidase 4,GPX4)蛋白和溶质载体家族7成员11(solute carrier family 7 member 11,SLC7A11)蛋白表达水平。结果对照组、OA低浓度组、OA中浓度组、OA高浓度组和OA+Fer-1组卵巢癌A2780细胞增殖活力分别为(100.00±0.00)%、(83.52±2.62)%、(66.39±2.98)%、(47.10±2.18)%、(54.83±2.21)%;HO-8910细胞增殖活力分别为(100.00±0.00)%、(88.31±4.49)%、(72.67±2.57)%、(44.02±1.66)%、(62.60±3.10)%。与对照组比较,OA低浓度组、OA中浓度组和OA高浓度组卵巢癌A2780、HO-8910细胞细胞增殖能力降低;与OA高浓度组比较,OA+Fer-1组卵巢癌A2780、HO-8910细胞增殖活力升高,差异均有统计学意义(F=273.225,182.968;P均<0.05)。与对照组比较,OA低浓度组、OA中浓度组和OA高浓度组卵巢癌A2780、HO-8910细胞迁移能力、侵袭能力、GSH、NRF2、HO-1、GPX4、SLC7A11蛋白表达水平下调,Fe2+、MDA水平上调;与OA高浓度组比较,OA+Fer-1组卵巢癌A2780、HO-8910细胞迁移能力、侵袭能力、GSH、NRF2、HO-1、GPX4、SLC7A11蛋白表达水平上调,Fe2+水平、MDA水平下调,差异均有统计学意义(P均<0.05)。结论OA可通过诱导卵巢癌A2780、HO-8910细胞细胞铁死亡从而抑制其恶性生物学行为,其机制与下调NRF2、HO-1、GPX4、SLC7A11蛋白表达水平有关。
[关键词]齐墩果酸;卵巢癌;核因子E2相关因子2;血红素加氧酶1;铁死亡
卵巢癌发病隐匿,现有临床治疗方法虽有一定进展,但整体治疗效果仍存在明显局限,亟需探索创新性治疗策略以有效抑制肿瘤细胞恶性生物学行为,该方向已成为现代医学研究的重要前沿[1-2]。目前,针对肿瘤的靶向治疗和新型药物的研究正在成为研究热点。卵巢癌的临床治疗急需可以用于靶向治疗的新靶点和新型药物。值得关注的是,我国传统中草药在卵巢癌治疗领域的应用正日益受到学术界关注,该方向已成为具有鲜明中国特色的创新点[3]。齐墩果酸(oleanolic acid,OA)是从龙胆科獐牙菜属植物青叶胆的全草或木犀科女贞属植物的果实中分离获得的五环三萜类天然产物,该化合物以游离态或糖苷结合形式广泛分布于多种植物中[4]。现代药理学研究证实,OA具有显著的保肝、免疫调节及降血脂等生物活性,而近年来其潜在的抗肿瘤效应正日益受到学术界关注[5]。铁死亡是一种新型程序性细胞死亡方式,与自噬、凋亡及焦亡等传统细胞死亡机制存在显著差异,其特征为细胞内脂质过氧化物和活性氧(reactive oxygen spe-cies,ROS)簇的异常积累。最新研究显示,铁死亡途径可有效抑制肝癌、胰腺癌、结直肠癌等肿瘤进展,诱导肿瘤细胞铁死亡已成为癌症治疗领域的新的方向[6-8]。在铁死亡调控机制研究中,核因子E2相关因子2(nuclear factor erythroid 2-related factor 2,NRF2)作为抗氧化防御系统的核心调控元件,在铁离子代谢、脂质稳态维持及谷胱甘肽(glutathione,GSH)生物合成等过程中发挥枢纽作用。本研究以卵巢癌A2780、HO-8910为模型,探讨OA通过诱导铁死亡对卵巢癌细胞恶性生物学行为的影响及其作用机制,为开发卵巢癌新型治疗策略提供理论依据。
1对象与方法
1.1细胞系
人卵巢癌A2780细胞株,购自武汉普诺赛生命科技有限公司;人卵巢癌HO-8910细胞株,购自中科院上海细胞库。
1.2主要仪器与试剂
OA(纯度>98%,货号:Q-003)购自成都瑞芬思德丹生物科技有限公司;NRF2、铁抑素-1(ferro-statin-1,Fer-1)、血红素加氧酶1(heme oxygenase-1,HO-1)、谷胱甘肽过氧化物酶4(glutathione Peroxi-dase 4,GPX4)蛋白、溶质载体家族7成员11(solute carrier family 7 member 11,SLC7A11)抗体、细胞计数试剂盒-8(cell counting kit-8,CCK-8)试剂盒、GSH试剂盒、丙二醛(malondialdehyde,MDA)试剂盒Transwell小室和细胞铁含量检测试剂盒均购自上海碧云天生物技术有限公司(货号分别为:AF7623、Y240805、AG2181、AF7020、AF7992、C0038、S0052、S0131S、FTW031-48Ins、S1066S)。DYCZ-40S电泳仪、WD-2102B酶标仪,WD-9413BX型凝胶成像分析系统购自北京六一仪器厂。
1.3检测方法
1.3.1细胞培养卵巢癌A2780、HO-8910细胞(传代2~3次)于含10%胎牛血清的DMEM培养基中培养(37℃、5%CO2),每3天换液1次。
1.3.2实验分组及处理将卵巢癌A2780、HO-8910细胞分别分为5组,空白对照组(常规培养)、OA低浓度组(30μmol/L)、OA中浓度组(60μmol/L)、OA高浓度组(120μmol/L)和OA+Fer-1组(OA 120μmol/L+Fer-1 30 nmol/L)。
1.3.3 CCK-8实验将卵巢癌细胞以1×104个/mL密度接种于96孔板,每组3个复孔,48 h后每孔加入10μl CCK-8溶液孵育1 h(37℃、5%CO2),用酶标仪在450 nm波长处检测OD值。细胞活力=(OD实验组-OD空白组)/(OD对照组-OD空白组)×100%。OD空白组:培养基、CCK-8试剂(不含卵巢癌细胞);OD对照组:卵巢癌细胞(未经处理);OD实验组:卵巢癌细胞(接受特定处理)。
1.3.4划痕实验将卵巢癌细胞以2×104个/孔密度接种于6孔板,每组3个复孔,移液器枪头匀速划出划痕后用PBS冲洗漂浮细胞,于0、24 h倒置光学显微镜在光学显微镜下(每孔选取6个视野)拍照后计算宽度平均值。迁移率=(0 h划痕宽度-24 h划痕宽度)/0 h划痕宽度×100%。
1.3.5细胞侵袭实验200μl细胞悬液接种于Tran-swell小室上室(基底胶稀释1∶4,每孔20μl,37℃孵育3 h凝固),每组3个复孔,下室加入600μl完全
培养液,培养24 h后固定、染色,随机选取5个视野计数穿膜细胞数。
1.3.6亚铁离子(Fe2+)、丙二醛(malondialdehyde,MDA)和谷胱甘肽(glutathione,GSH)水平检测收集卵巢癌细胞,离心(1 000 r/min、离心半径10 cm、10 min)后弃上清液,将细胞沉淀加入等渗磷酸缓冲液后,再次离心收集沉淀细胞;再次加入磷酸盐缓冲液后手动破碎细胞制成细胞匀浆后,根据试剂盒说明书进行操作,采用比色法检测亚铁离子、MDA和GSH水平。
1.3.7 Western blot实验细胞裂解液提取总蛋白,BCA法测定浓度后分离蛋白、转膜、封闭(5%脱脂牛奶,2 h)、加入一抗(NRF2、HO-1、GPX4、SLC7A11)4℃孵育过夜。将膜与二抗(山羊抗鼠IgG,1∶4 000)室温孵育2 h,以GAPDH为内参,Im-age J软件量化蛋白灰度值。
1.4统计方法
采用SPSS 25.0统计学软件进行分析,符合正态分布的计量资料以(±s)表示,多组间比较用单因素方差分析。P<0.05为差异有统计学意义。
2结果
2.1不同浓度OA对卵巢癌A2780、HO-8910细胞增殖活性的影响
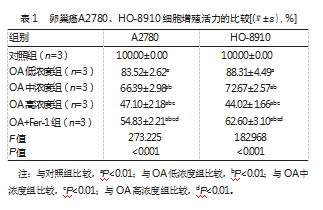
CCK-8实验数据显示,与对照组比较,OA低浓度组、OA中浓度组和OA高浓度组卵巢癌A2780、HO-8910细胞细胞增殖能力降低;与OA高浓度组比较,OA+Fer-1组卵巢癌A2780、HO-8910细胞增殖活力升高,差异均有统计学意义(P均<0.05)。见表1。
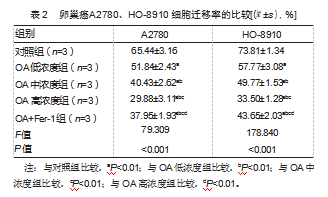
2.2不同浓度OA对卵巢癌A2780、HO-8910细胞迁移能力的影响
划痕实验数据显示,与对照组比较,OA低浓度组、OA中浓度组和OA高浓度组卵巢癌A2780、HO-8910细胞迁移率降低;与OA高浓度组比较,OA+Fer-1组卵巢癌A2780、HO-8910细胞迁移率升高,差异均有统计学意义(P均<0.05)。见表2。
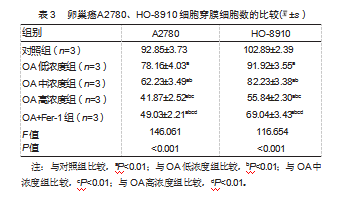
2.3不同浓度OA对卵巢癌A2780、HO-8910细胞侵袭能力的影响
Transwell实验数据显示,与对照组比较,OA低浓度组、OA中浓度组和OA高浓度组卵巢癌A2780、HO-8910细胞穿膜细胞数降低;与OA高浓度组比较,OA+Fer-1组卵巢癌A2780、HO-8910细胞穿膜细胞数升高,差异均有统计学意义(P均<0.05)。见表3。
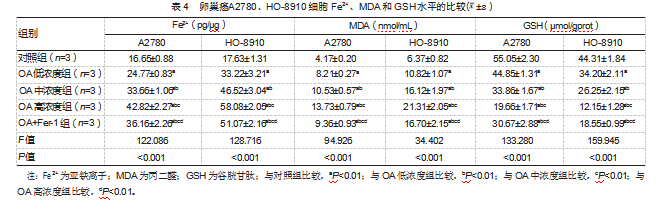
2.4不同浓度OA对卵巢癌A2780、HO-8910细胞Fe2+、MDA和GSH水平的影响
与对照组比较,OA低浓度组、OA中浓度组和OA高浓度组卵巢癌A2780、HO-8910细胞的Fe2+、MDA水平增高,GSH水平降低;与OA高浓度组比较,OA+Fer-1组卵巢癌A2780、HO-8910细胞的Fe2+、MDA水平降低,GSH水平增高,差异均有统计学意义(P均<0.05)。见表4。
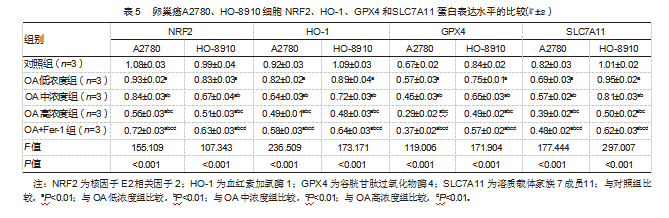
2.5不同浓度OA对卵巢癌A2780、HO-8910细胞NRF2、HO-1、GPX4和SLC7A11蛋白表达水平的影响
Western blot实验数据显示,与对照组比较,OA低浓度组、OA中浓度组和OA高浓度组卵巢癌A2780、HO-8910细胞NRF2、HO-1、GPX4、SLC7A11蛋白表达水平下调;与OA高浓度组比较,OA+Fer-1组卵巢癌A2780、HO-8910细胞NRF2、HO-1、GPX4、SLC7A11蛋白表达水平上调,差异均有统计学意义(P均<0.05)。见表5。
3讨论
目前全球范围内卵巢癌现有治疗方法疗效不佳,开发新型药物和新的治疗靶点治疗卵巢癌任务非常紧迫,因此,筛选有效的临床治疗药物并探索其作用机制具有重要的研究价值。中药单体在抗肿瘤领域有显著优势[9-15]。OA具有广泛的药理活性及抗肿瘤作用[4-5]。本研究结果显示:卵巢癌A2780、HO-8910细胞经低、中、高浓度OA处理后,细胞增殖、迁移和侵袭能力明显降低;OA+Fer-1组增殖活力升高(P均<0.05),这表明OA对卵巢癌A2780、HO-8910细胞的恶性生物学行为具有抑制作用。
铁死亡是新型细胞程序性死亡方式,其主要机制与细胞内铁累积密切相关,主要通过细胞内亚Fe2+、ROS堆积,GSH代谢障碍,线粒体结构改变,细胞膜脂质过氧化,诱导细胞死亡[16-17]。作为体内重要的抗氧化物,GSH的功能主要是通过将过氧化氢还原为H2O对抗ROS堆积造成的细胞膜损伤,抑制脂质过氧化并修复生物膜,其是对抗细胞铁死亡的关键酶。MDA作为脂质过氧化的终末产物,其水平可反映铁死亡进展程度。本研究结果显示:卵巢癌A2780、HO-8910细胞OA低浓度组、OA中浓度组和OA高浓度组Fe2+、MDA水平增高,GSH水平降低;OA+Fer-1组Fe2+、MDA水平降低,GSH水平增高(P均<0.05),这表明OA导致卵巢癌A2780、HO-8910细胞内Fe2+堆积和细胞膜脂质过氧化损伤,提示细胞可能发生铁死亡。
HO-1可促进吸收游离Fe2+蛋白的转录、修饰与翻译。NRF2作为核心转录因子,可激活内源性抗氧化反应元件。NRF2在维持代谢平衡、氧化还原稳态及蛋白质稳态中起关键作用,其是铁死亡的主要抑制因子。当ROS积累时,NRF2表达上调,进而促进抗氧化酶和解毒酶的表达,抑制铁死亡发生。中药单体、NRF2与铁死亡之间的相互作用在不同种类细胞间存在明显差异。在受到化学、炎症等损伤的细胞中,中药单体可以提高NRF2表达,抑制铁死亡,起到保护细胞的作用,例如:OA可通过激活NRF2-抗铁死亡轴减轻重症急性胰腺炎大鼠肝损伤[18]。然而,在肿瘤细胞中,中药单体可以降低NRF2表达,促进铁死亡,降低肿瘤细胞的细胞增殖,例如:木犀草素可以通过降低NRF2、HO-1蛋白表达诱导人耐多柔比星慢性髓系白血病K562/ADR铁死亡从而抑制其增殖[19]。此外,GPX4作为NRF2下游蛋白,是氧化应激和细胞死亡信号的关键传感器,近年研究显示其参与触发铁死亡程序。SLC7A11是铁死亡上游调节因子,与GPX4共同组成抗氧化防御系统,SLC7A11下调可以导致细胞内GSH合成水平降低,上调可以导致MDA水平升高和抑制GPX4活性,使ROS和脂质过氧化物在细胞内堆积,诱导细胞发生铁死亡[20-24]。本研究结果显示:经低、中、高浓度OA处理后,卵巢癌A2780、HO-8910细胞细胞的NRF2、HO-1、GPX4、SLC7A11蛋白水平下调,这表明通过调节NRF2/HO-1/GPX4/SLC7A11信号通路诱导卵巢癌A2780、HO-8910细胞铁死亡。
综上所述,OA通过诱导卵巢癌A2780、HO-8910细胞铁死亡从而抑制其恶性生物学行为,其机制与下调NRF2、HO-1、GPX4、SLC7A11蛋白表达水平有关。本实验提示OA治疗卵巢癌可能发挥较好作用,未来可能将其应用于卵巢癌的临床治疗。
[参考文献]
[1]徐慧,申芳,李佳,等.卵巢癌中铁死亡调节机制及其相关研究进展[J].现代肿瘤医学,2025,33(10):1785-1792.
[2]沙晓雨,左卫微,甘静,等.卵巢癌的高危因素和治疗研究进展[J].肿瘤防治研究,2025,52(7):637-644.
[3]高越,石百超,余健楠,等.中药多糖抗妇科恶性肿瘤作用的研究进展[J].国际妇产科学杂志,2025,52(6):685-689,707.
[4]万晓莉.齐墩果酸药理作用的研究进展[J].黔南民族医专学报,2023,36(1):73-75.
[5]袁彬,韦燕飞,周凤玲,等.齐墩果酸抗肿瘤作用及机制研究进展[J].中国医药导报,2023,20(33):60-62,66.
[6]李留峥,徐雷升,罗康虹,等.SLC7A11基因通过调控铁死亡通路对肝细胞癌进展的影响[J].昆明医科大学学报,2025,46(10):32-43.
[7]陈鑫球,张正则,刘抒伟,等.健脾化瘀方协同吉西他滨通过Nrf2/SLC7A11/GPX4轴诱导胰腺癌细胞铁死亡并抑制其生长[J].中国病理生理杂志,2025,41(6):1077-1087.
[8]梁家,刘俊杰,庞天舒,等.毛蕊异黄酮调控GSK-3β/Nrf2/GPX4铁死亡通路逆转结直肠癌5-FU耐药的研究[J].胃肠病学和肝病学杂志,2025,34(12):1792-1796.
[9]万珊珊,孙晓冬,闫磊.甘草查尔酮A对人脑胶质瘤U251细胞增殖和凋亡的影响[J].中国当代医药,2022,29(3):4-7.
[10]包翔,朱倩影,汤汇涓,等.灵芝酸D通过调控p53/Bax通路对人结直肠肿瘤细胞的作用机制研究[J].中国临床药理学杂志,2022,38(12):1339-1343.
[11]何能婷,秦燕萍,李昊,等.裂果薯皂苷Ⅰ通过干预谷氨酰胺代谢影响人肝癌BEL-7404细胞增殖的研究[J].中国临床药理学杂志,2023,39(9):1232-1236.
[12]李红,万珊珊,刘志新,等.甘草查尔酮A通过PI3K/Akt信号通路对胶质瘤U87细胞增殖、迁移、侵袭和氧化损伤的影响[J].中国临床药理学杂志,2024,40(5):678-682.
[13]林珊,屈思萌,张荣,等.藏红花素诱导视网膜母细胞瘤自噬性死亡并抑制细胞侵袭和PI3K/AKT的活化[J].解剖学杂志,2022,45(6):542-546,567.
[14]张正平,李坤正,吴彬杰,等.败酱草水提物通过调控circ_0000936/miR-665抑制胶质瘤细胞增殖、迁移及侵袭[J].现代肿瘤医学,2024,32(6):1017-1024.
[15]刘彬,曾宪晶,袁金华,等.高三尖杉酯碱对肺癌A549侧群细胞增殖及凋亡的影响[J].中国老年学杂志,2023,43(23):5796-5800.
[16]穆清爽,李沛珊,李艳霞,等.维生素D通过Nrf2/HO-1抑制铁死亡缓解6-羟基多巴胺所致PC12细胞损伤的作用机制研究[J].新疆医科大学学报,2023,46(12):1580-1588.
[17]杨洋,杨梦婷,许潇,等.醋酸棉酚通过诱导铁死亡抑制脑胶质瘤细胞生长[J].江苏大学学报(医学版),2022,32(3):246-250.
[18]李建,常东鸽,霍刘斌,等.齐墩果酸通过Nrf2抑制铁死亡并减轻重症急性胰腺炎大鼠肝损伤[J].中国病理生理杂志,2022,38(8):1470-1477.
[19]周欣宇,王翠翠,张婷,等.木犀草素通过Nrf2/HO-1通路诱导耐多柔比星K562/ADR细胞发生铁死亡[J].肿瘤,2023,43(12):947-959.
[20]施磊,姜晨晨,陆嘉珺,等.藁本内酯通过抑制铁死亡减轻PC12细胞OGD/R损伤的分子机制研究[J].中国中药杂志,2023,48(11):3046-3054.
[21]孔春艳,李纪华,王艳丽.虾青素对脂多糖诱导的肾小管上皮细胞铁死亡的影响[J].中国临床药理学杂志,2023,39(21):3092-3096.
[22]范昕怡,魏小棋,柴王静,等.基于NRF2/HO-1/GPX4通路探讨鸡鸣散抑制铁死亡治疗心肌梗死的效应机制[J].中国中药杂志,2025,50(11):3108-3116.
[23]谌程程,何平,黄宇婧,等.鸦胆子苦醇调节Nrf2/SLC7A11/GPX4信号通路对皮肤鳞癌细胞铁死亡的影响[J].重庆医科大学学报,2023,48(4):369-374.
[24]王智槟,邹晓玲,邹译娴,等.基于Nrf2/HO-1/GPX4信号轴探讨参芪地黄汤抑制高糖诱导人肾小管上皮细胞铁死亡的作用机制[J].中国中药杂志,2023,48(19):5337-5344.










