调强放疗联合 XELOX 方案治疗局部晚期直肠癌的临床效果论文
2026-04-15 17:16:00 来源: 作者:xuling
摘要:局部晚期RC患者采用IMRT联合XELOX方案治疗,可提高临床疗效,改善肿瘤标志物及免疫功能,且不会增加不良反应。
[摘要]目的探讨局部晚期直肠癌(rectal cancer,RC)患者采用调强放疗(intensity modulated radiation therapy,IMRT)联合XELOX方案治疗的临床效果。方法随机选取2024年1月—2025年5月甘肃中医药大学第三附属医院收治的90例局部晚期RC患者为研究对象,以治疗方法的不同分成研究组(n=45)和对照组(n=45),对照组给予XELOX方案治疗,研究组给予IMRT联合XELOX方案治疗。比较两组临床疗效、肿瘤标志物、免疫功能、不良反应。结果研究组客观缓解率为64.44%(29/45)、疾病控制率为86.67%(39/45),较对照组的42.22%(19/45)、68.89%(31/45)更高,差异均有统计学意义(χ2=4.464,4.114;P均<0.05)。治疗后,研究组癌胚抗原、糖类抗原19-9低于对照组,差异均有统计学意义(P均<0.05)。治疗后,两组细胞毒性T淋巴细胞(CD8+T Lymphocytes,CD8+)较治疗前升高,T淋巴细胞(CD3+T Lymphocytes,CD3+)、辅助/诱导T淋巴细胞(CD4+T Lymphocytes,CD4+)及CD4+/CD8+均降低;且研究组CD8+较对照组更低,CD3+、CD4+、CD4+/CD8+较对照组更高,差异均有统计学意义(P均<0.05)。两组不良反应发生率比较,差异无统计学意义(P>0.05)。结论局部晚期RC患者采用IMRT联合XELOX方案治疗,可提高临床疗效,改善肿瘤标志物及免疫功能,且不会增加不良反应。
[关键词]调强放疗;XELOX方案;局部晚期直肠癌;临床效果
在消化系统恶性肿瘤疾病中,直肠癌(rectal cancer,RC)是较为常见的一种,局部晚期RC是指肿瘤已侵犯至肠壁外组织或器官,此时患者会出现排便习惯异常,例如排便次数增加、便秘、腹泻等,部分患者还会伴有腹痛、血便等问题,严重者还会出现肠梗阻,甚至发生远处转移,危及患者生命[1-2]。因此治疗核心在于精准控制局部肿瘤进展与减少远处转移风险,同时兼顾患者免疫功能保护及治疗安全性。XELOX方案是治疗肠癌的常用化疗方案,由卡培他滨和奥沙利铂组成,可有效抑制肿瘤细胞增长,控制疾病发展[3]。但长期使用肿瘤容易出现耐药性,效果局限。调强放疗(intensity modulated radiation therapy,IMRT)是一种先进的放疗技术,通过调整射线强度,使高剂量区与肿瘤靶区高度吻合,在提高肿瘤局部照射剂量的同时,减少周围正常组织的受照剂量,从而提高治疗效果,进一步控制肿瘤进展[4]。本研究旨在探究调强放疗联合XELOX方案治疗局部晚期RC患者的临床效果,现报道如下。
1资料与方法
1.1一般资料
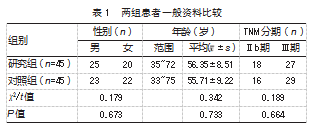
随机选取2024年1月—2025年5月甘肃中医药大学第三附属医院收治的90例局部晚期RC患者为研究对象,以治疗方法的不同分成研究组(n=45)与对照组(n=45)。两组基线资料比较,差异均无统计学意义(P均>0.05),均衡可比。见表1。患者或家属均知情同意本研究,本研究经甘肃中医药大学第三附属医院医学伦理委员会批准(2023-12012)。
1.2纳入与排除标准
纳入标准:①符合RC诊断标准[5],经病理组织学检查确诊;②预计生存期>6个月;③无放化疗禁忌;④近6个月内均未接受免疫抑制剂等治疗。
排除标准:①合并远处转移者;②合并其他恶性肿瘤(肺癌、胃癌等)者;③有严重脏器功能不全者;④对本研究使用药物(奥沙利铂、卡倍他滨等)过敏者。
1.3治疗方法
对照组给予XELOX方案化疗,每周期第1天给予注射用奥沙利铂(国药准字H20133094;规格:50 mg),静脉滴注,130 mg/(m2·次);每周期第1~14天口服卡培他滨片(国药准字H20243386;规格:0.5 g),1 000 mg/(m2·次),2次/d。一个治疗周期为21 d,治疗4个周期。
研究组给予IMRT联合XELOX方案(同对照组)治疗,具体操作:①定位与靶区勾画:指导患者取仰卧位,对患者实施CT扫描,扫描范围从膈顶至坐骨结节下缘,层厚5 mm。将CT图像传输至治疗计划系统,由两名资深放疗科医师共同确定靶区位置并勾画。确定临床靶区,对其实施上下界扩展(2~3 cm)、左右及前后界扩展(1~2 cm),计划靶区为临床靶区外扩0.5~1.0 cm,以补偿呼吸运动及摆位误差。②治疗计划制定:在IMRT技术的支持下实施治疗,选用6MVX射线,设置照射野(5~7个),使95%的计划靶区接受处方剂量,处方剂量计划靶区1.8 Gy/次,共照射28次,总剂量50.4 Gy,照射5次/周,共治疗6周。
1.4观察指标
①临床疗效[6]:完全缓解:肿瘤病灶减少>90%或消失,无新病灶出现(1个月内);部分缓解:病灶减少50%~90%,无新病灶出现(1个月内);疾病稳定:病灶减少<50%或增加<25%;疾病进展:病灶增加≥25%或出现新病灶。客观缓解率=(完全缓解+部分缓解)例数/总例数×100%;疾病控制率=(完全缓解+部分缓解+疾病稳定)例数/总例数×100%。②肿瘤标志物:治疗前后抽取肘静脉血,剂量为3 mL,空腹采集,离心(转速3 000 r/min、半径10 cm)10 min后分离血清,检测癌胚抗原、糖类抗原19-9水平(酶联免疫发光法)。③免疫功能:治疗前后采集患者空腹静脉血(3 mL),设置转速为3 000 r/min,半径为15 cm,离心处理10 min,取血清,使用流式细胞仪(粤械注准20202221588,型号:EasyCell 103A0)对T淋巴细胞(CD3+T Lymphocytes,CD3+)、辅助/诱导T淋巴细胞(CD4+T Lymphocytes,CD4+)、细胞毒性T淋巴细胞(CD8+T Lymphocytes,CD8+)进行测定,并计算CD4+/CD8+。④不良反应:统计患者治疗期间胃肠道反应、骨髓抑制、周围神经病变、肝肾功能损害发生情况。不良反应总发生率=(胃肠道反应例数+周围神经病变例数+骨髓抑制例数+肝肾功能损害例数)/总例数×100%。
1.5统计方法
采用SPSS 26.0统计学软件处理数据,经S-W检验符合正态分布的计量资料(肿瘤标志物、免疫功能)以(x-±s)表示,组间比较行两独立样本t检验,组内比较行配对t检验;计数资料(临床疗效、不良反应)以例数(n)和率(%)表示,组间比较行χ2检验,等级资料行秩和检验。P<0.05为差异有统计学意义。
2结果
2.1两组患者临床疗效比较
研究组客观缓解率、疾病控制率较对照组更高,差异均有统计学意义(P均<0.05)。见表2。
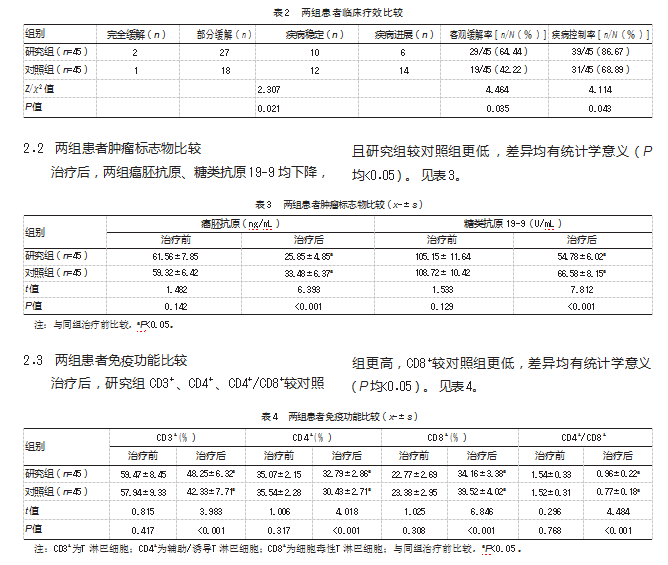
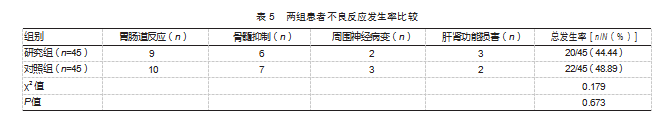
2.4两组患者不良反应总发生率比较
两组胃肠道反应、骨髓抑制等不良反应总发生率比较,差异无统计学意义(P>0.05)。见表5。
3讨论
RC发病率和死亡率均居恶性肿瘤前列,局部晚期RC虽无远处转移,但肿瘤浸润深度较深,单纯手术治疗效果不佳,术后复发率较高,5年生存率较低,因此需要采用综合治疗方案以改善预后[7]。
XELOX方案是RC化疗的经典方案,通过奥沙利铂抑制肿瘤细胞DNA合成,卡培他滨在肿瘤组织内转化为5-氟尿嘧啶发挥细胞毒性作用,虽能在一定程度控制肿瘤进展,但化疗药物缺乏对肿瘤组织的穿透性,难以将局部浸润的癌细胞彻底清除,单纯化疗的疗效往往有限[8]。IMRT技术能够借助精准的剂量分布优势,在对肿瘤组织进行高剂量照射的同时,可最大限度使周围正常肠道及其他健康器官的受照剂量减少,以达到“靶向放疗”的效果[9]。
龚伟等[10]研究指出,对中晚期结RC患者实施调强放疗辅助XELOX方案治疗,可有效降低肿瘤标志物水平,提高疾病缓解率。本研究中,研究组客观缓解率、疾病控制率比对照组更高(P均<0.05)。分析其原因,联合治疗可直接杀伤局部肿瘤细胞,使肿瘤体积缩小,促进肿瘤微环境改善,增强化疗药物敏感性,还可将潜在微转移病灶清除,降低局部复发风险,提高疗效[11]。肿瘤标志物水平的变化是评估治疗效果的重要客观指标,其中癌胚抗原、糖类抗原19-9均与肿瘤负荷、浸润转移程度密切相关,在RC患者中呈异常升高状态[12]。本研究结果中,研究组癌胚抗原、糖类抗原19-9水平更低(P均<0.05)。考虑其原因,联合治疗可有效地杀伤肿瘤细胞,减少肿瘤细胞的增殖与代谢,减少肿瘤标志物的释放的同时,缩小局部肿瘤体积,进一步减少肿瘤标志物的合成来源,从而降低肿瘤标志物水平。
免疫功能紊乱是恶性肿瘤患者的重要病理特征,而放化疗对免疫系统的损伤会进一步削弱机体抗肿瘤能力,形成恶性循环[13]。CD3+反映机体总T细胞免疫功能状态,CD4+具有调节免疫反应、辅助体液免疫的作用,CD8+可直接杀伤病毒感染或肿瘤细胞,CD4+/CD8+是评估免疫平衡的关键指标,其水平降低则提示机体存在免疫抑制问题[14-15]。本研究中,治疗后,研究组CD3+、CD4+、CD4+/CD8+更高,CD8+更低(P均<0.05)。分析其原因,IMRT技术照射时照射野覆盖正常组织,对周围正常免疫器官的影响较小,可减轻对免疫细胞造成的损伤,且联合治疗可有效控制肿瘤细胞释放的免疫抑制因子,降低肿瘤对免疫系统的抑制作用,改善免疫功能。此外,关于不良反应发生率,两组比较差异无统计学意义(P>0.05)。分析其原因,IMRT具有优化剂量分布的特点,正常肠道黏膜及膀胱壁等组织的受照剂量较低,可有效降低放射性损伤,且联合治疗中的化疗药物剂量未增加,可有效避免化疗不良反应的叠加,因此不会增加不良反应的发生。两组均存在胃肠道反应、骨髓抑制、周围神经病变、肝肾功能损害等不良反应,针对胃肠道反应,及时给予对症处理,遵医嘱给予止吐止泻药物,并及时补液避免脱水,同时给予适当的饮食指导;针对骨髓抑制者,对血小板计数及中性粒细胞绝对值进行重点监测,并遵医嘱进行分级针对性处理;针对周围神经病变者,用药期间避免冷刺激,注意保暖并避免接触冷水,输液时使用恒温器加温,同时遵医嘱给予神经营养药物;针对肝肾功能损害者,治疗前评估患者肝肾功能,避免使用肝毒性、肾毒性药物,必要时调整治疗方案。
本研究为单中心研究,样本量仅为90例,未观察生存期等远期指标,可能影响结果的普适性,之后将开展多中心、大样本研究,将随访时间延长,纳入生存期等指标,旨在为RC患者的治疗提供更可靠数据支持。
综上所述,IMRT联合XELOX方案应用于局部晚期RC患者治疗中,有效提高患者疗效,可促进肿瘤标志物改善,提升免疫功能,安全性较高。
[参考文献]
[1]陈丽霞,罗云婷,徐晶晶,等.参芪补肺汤联合穴位按摩对气虚证结直肠癌术后化疗老年患者的临床疗效[J].中成药,2024,46(1):334-337.
[2]陈昌江,杨春康,简锦亮,等.短程放疗联合化疗的全程新辅助治疗在中低位直肠癌治疗中的应用[J].中华医学杂志,2023,103(4):271-277.
[3]刘信,高广泽,崔红霞.卡培他滨单药及联合奥沙利铂方案治疗伴有癌结节的Ⅲ期结直肠癌术后患者的疗效比较[J].中国医科大学学报,2025,54(4):375-378.
[4]沈锦霞,杜德希,何慧娟,等.直肠癌新辅助同步加量调强放疗对侧方淋巴结转移的影响[J].中华放射医学与防护杂志,2023,43(11):866-872.
[5]中华人民共和国国家卫生健康委员会.中国结直肠癌诊疗规范(2023版)[J].协和医学杂志,2023,14(4):706-733.
[6]SEYMOUR L,BOGAERTS J,PERRONE A,et al.iRECIST:Guidelines for response criteria for use in tri-als testing immunotherapeutics[J].Lancet Oncol,2017,18(3):143-152.
[7]纪云松,王磊,李学敏,等.直肠癌盆腔复发患者二程放疗的长期疗效分析[J].中华放射肿瘤学杂志,2025,34(7):671-676.
[8]何亚琳,程志强.调脾安肠方联合XELOX方案治疗结直肠癌术后患者的临床研究[J].中华中医药杂志,2023,38(1):437-441.
[9]杨俊昌,姚成云,孙晓奕,等.直肠癌术后调强放疗降低S2/S3以上计划靶区剂量的临床效果[J].中国肿瘤外科杂志,2023,15(5):469-475.
[10]龚伟,潘腾升,陈显诚.调强放疗辅助XELOX方案对中晚期结直肠癌患者疾病缓解率及血清肿瘤标志物水平的影响[J].中国医药指南,2025,23(21):90-92.
[11]郭琴琴,张静,燕丽香.阿帕替尼联合卡培他滨+奥沙利铂方案对中晚期结直肠癌患者近期疗效及血管生成指标的影响[J].药物评价研究,2024,47(4):809-816.
[12]马淑霞,田莉霞,张姝燕.FOBT及CEA、CA19-9在结直肠癌早期筛查中的意义[J].中国肛肠病杂志,2025,45(4):1-4.
[13]陈天一,李超凡,包灵波,等.APE1通过免疫抑制性肿瘤微环境介导结肠炎相关结直肠癌的发生发展[J].陆军军医大学学报,2024,46(16):1825-1837.
[14]陈颖秀,卢仁泉,郭林,等.直肠癌患者外周血淋巴细胞亚群与新辅助治疗效果的关系[J].中华检验医学杂志,2024,47(12):1419-1425.
[15]刘萍,骆学新.肠益方联合XELOX化疗方案对老年晚期结直肠癌患者近期疗效及对血清SDC2、SEPT9和免疫功能的影响[J].中国老年学杂志,2022,42(5):1085-1087.










