急性肺栓塞患者呼吸支持策略的研究进展论文
2026-04-15 17:09:15 来源: 作者:xuling
摘要:本文系统梳理了肺栓塞患者呼吸支持策略的最新研究进展,涵盖经鼻高流量氧疗和无创正压通气、有创机械通气以及静脉-动脉体外膜肺氧合等主要支持方式,并深入探讨其临床选择依据,为临床决策提供参考。
[摘要]急性肺栓塞是常见的心血管急症,严重威胁患者健康和生存。合并呼吸衰竭是导致患者预后不良的主要因素之一。呼吸支持是肺栓塞综合治疗的重要环节,然而,不恰当的呼吸支持策略可能加重右心衰竭,进而加剧血流动力学不稳定。目前针对肺栓塞患者(尤其是高危人群)的最佳呼吸支持策略,在临床实践中仍存在认识不足与决策争议。为此,本文系统梳理了肺栓塞患者呼吸支持策略的最新研究进展,涵盖经鼻高流量氧疗和无创正压通气、有创机械通气以及静脉-动脉体外膜肺氧合等主要支持方式,并深入探讨其临床选择依据,为临床决策提供参考。
[关键词]肺栓塞;呼吸支持;经鼻高流量氧疗;有创机械通气;静脉-动脉体外膜肺氧合
急性肺栓塞(acute pulmonary embolism,APE)是急性肺动脉阻塞引起的循环呼吸衰竭综合征,是心血管死亡的第三大常见原因[1],高危肺栓塞常表现为心脏停搏、梗阻性休克及严重低氧血症等致命表现,患者常在入院前死亡。APE的病理生理机制主要包括血流动力学改变、右心功能障碍及呼吸功能不全。肺循环本身为低阻力系统,右心室对后负荷的突然增加极为敏感。当肺血管阻塞超过50%时,右心室后负荷急剧升高、导致右心室扩张、室壁张力增加、收缩功能降低,室间隔左移进一步影响左心室充盈,导致每搏输出量减少和全身低血压[2]。此外,通气/血流比例失调、低氧血症、肺泡死腔增加、肺内分流及呼吸肌疲劳均可导致呼吸功能不全[3]。而右心衰竭进一步加重低氧,低氧性呼吸衰竭与右心衰竭是APE主要致死原因之一。对于APE合并低氧血症,呼吸支持应阶梯化管理:从常规氧疗开始,无效时可依次考虑经鼻高流量氧疗(high-flow nasal cannula,HFNC)、无创正压通气(non-invasive positive pressure ventilation,NIPPV)、有创机械通气(invasive mechanical ventilation,IMV)及静脉-动脉体外膜肺氧合(venous-arterial extracor-poreal membrane oxygenation,VA-ECMO)等。需注意,机械通气可能加重心肺不稳定,因此应贯彻“肺保护”及“右心功能保护”策略。本文旨在综述最新进展,探讨此类患者呼吸支持策略的优化。以下是APE的呼吸支持方式,具体阐述如下。
1 HFNC支持模式
HFNC作为一种呼吸支持模式,其生理学原理在于通过输送高流量(20~80 L/min)气体,精准调控并维持恒定的吸入氧浓度[(fraction of inspired oxy-gen,FiO2)21%~100%],同时可将气体加温湿化(温度37℃以及相对湿度100%[4-6]。不仅能迅速提升动脉血氧分压(arterial oxygen partial pressure,PaO2),还能有效冲刷鼻咽部解剖死腔,减少CO 2重复吸入,并在呼气相产生轻度正压[约2.7~7.4 cmH2O(1 cmH2O=0.098 kPa)][7],促进肺泡复张,增加呼气末肺容量和肺顺应性,改善通气血流匹配,同时显著降低呼吸做功、呼吸频率,湿化气道改善黏膜纤毛清除功能,避免气道黏膜的损伤[5-6]。研究显示,HFNC能改善APE合并急性低氧性呼吸衰竭(acute hypoxaemic respiratory failure,AHRF)患者的呼吸窘迫症状、生命体征和动脉血气参数、氧合、降低呼吸肌做功、提高舒适度等[3,8]。与NIPPV相比,HFNC的耐受性、舒适度更好,患者可自由进食、说话。右心保护方面,HFNC不会明显增加胸腔内压,即可提升氧饱和度[1],适度的呼气末正压(positive end-expiratory pressure,PEEP)可减轻肺水肿,同时避免因为正压通气、胸腔压力增加导致肺实质内压力升高,增加肺血管阻力和右心室后负荷,从而降低加重右心衰竭及低血压、休克风险,因此不推荐优先使用NIPPV或IMV用于APE患者[9-10]。HFNC已被证明能降低AHRF患者的再插管率和死亡率[11],且对血流动力学影响较小,可安全作为溶栓前的桥接治疗,稳定氧合、为溶栓或抗凝治疗赢得更多时间,避免气管插管。
HFNC的参数设置包括[12-13]:①FiO2设置以达到目标血氧饱和度(I型呼吸衰竭:92%~96%;Ⅱ型呼吸衰竭或高碳酸风险:88%~92%),快速纠正缺氧后应下调FiO2以减少氧毒性。②流量设置:肺栓塞患者应避免过高PEEP,避免过高的流速。推荐初始流量30~40 L/min,存在明显CO2潴留或低氧时,可逐步增至患者耐受的最大流量(通常45~55 L/min或更高)。③温度设置:推荐初始温度34℃(不耐受、敏感患者可31℃),气管切开/插管患者可设37℃。HFNC过程中对接受抗凝或溶栓的肺栓塞患者,需特别警惕并监测鼻腔及气道出血风险[14]。
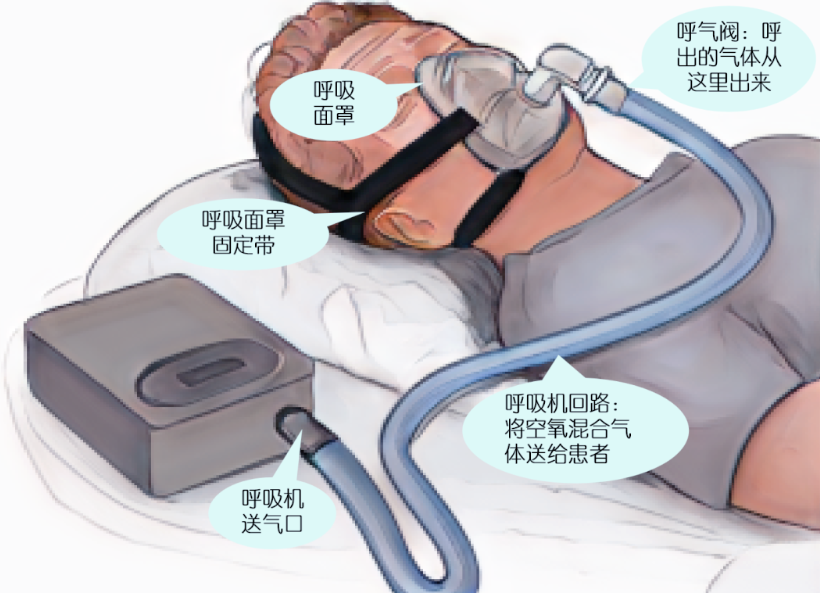
2 NIPPV支持模式
NIPPV通过鼻罩、口鼻罩、全面罩或头罩等无创接口提供正压呼吸支持,无需进行气管插管或气管切开等侵入性操作[15]。该通气方式包括持续气道正压(continuous positive airway pressure,CPAP)和双水平气道正压(bi-phasic positive airway pressure,BiPAP)两种模式。CPAP在吸气与呼气相均维持恒定正压、促进肺泡复张并提高功能残气量;BiPAP则分别设定吸气相气道正压(inspiratory positive air-way pressure,IPAP)和呼气相气道正压(expiratory positive airway pressure,EPAP),其中IPAP用于增加潮气量,EPAP则防止呼气相肺泡塌陷。PEEP和EPAP在核心定义上高度相似,但不能完全等同或随意替换[16]。
NIPPV适用于因低氧血症和/或高碳酸血症引起的急性呼吸衰竭[17],能避免插管和有创机械通气相关风险,减少并发症,并可用于拔管后呼吸支持[18]。对充血性心力衰竭、心源性肺水肿患者,NIPPV通过优化心肺交互作用,有效改善临床症状,降低心率和呼吸频率,并提高血氧饱和度,疗效优于常规治疗[19]。与HFNC相比,NIPPV能提供更高的呼气末压力,进一步改善氧合;其中BiPAP模式在减轻患者的吸气努力,增加潮气量和跨肺驱动压力方面更具优势[18]。然而,NIPPV并非适用于所有人群,使用不当可能导致血流动力学不稳定,高碳酸血症或呼吸性酸中毒等风险[20]。
对血流动力学稳定的肺栓塞患者,若优先尝试HFNC后,氧合无改善,应升级至NIPPV。目前关于NIPPV在肺栓塞所致AHRF患者中应用的研究尚不充分。部分研究显示,对于轻度至中度右心室功能不全患者,HFNC与NIPPV疗效相当;但在重度右心室功能障碍患者中,应优先考虑NIPPV以优化氧合并降低插管风险[21]。其机制在于提高气道正压,改善氧合、减轻低氧性肺血管收缩,并通过降低呼吸功及调节胸腔内压力,减轻右心室前负荷[22]。
在参数设置方面,CPAP模式建议从较低压力开始,逐步调节PEEP和压力支持水平(5~15 cmH2O),目标使呼吸频率<25次/min,缓解呼吸窘迫和过度吸气努力[23-24]。BiPAP模式则建议以理想体质量6~8 mL/kg的潮气量目标,控制呼吸频率<25次/min,常用参数设置PEEP 5~10 cmH2O,压力支持12~16 cmH2O,流量触发2 L/min,优化升压时间以提升耐受性[25]。
3 IMV支持模式
IMV通过建立人工气道(如气管插管或气切导管)进行正压通气,可保障气道安全,输送100%FiO2,并采用PEEP预防肺不张,降低二氧化碳分压(允许性低碳酸血症策略可减轻右心室后负荷),从而维持生命体征,为外科或介入手术创造条件[3]。约6%~36%的高危肺栓塞患者需要接受机械通气[26]。目前,对于APE继发呼吸衰竭患者,尚无明确的插管呼吸支持指征标准,而低氧饱和度与早期临床恶化密切相关。
急性高危肺栓塞常伴右心功能障碍、肺动脉高压及ARF,为稳定病情常需要麻醉、气管插管和有创机械通气,然而,IMV中高跨肺压(如过强自主呼吸、高潮气量或不合理PEEP)可增加肺血管阻力(pulmonary vascular resistance,PVR)及右心室后负荷,而高胸膜压则降低右心室前负荷,二者协同作用可能引起肺血管血流与压力波动,加剧血管剪切力与微血管损伤,从而恶化右心衰竭和低氧,增加肺损伤风险[27-28]。右心室收缩功能障碍直接影响左心室充盈与每搏输出量,是APE主要死因[3]。麻醉诱导及插管期间易出现血流动力学不稳定,尤其见于右心室功能不全患者[29]。其机制是麻醉药物可致血管扩张、右心室前负荷下降、全身及冠状动脉灌注降低,部分药物还具有负性肌力作用,其中丙泊酚的使用与APE的不良结局相关[3,30]。对于右心衰竭合并肺动脉高压所致AHRF,清醒状态下经支气管镜引导(配合口咽局部麻醉)插管可提高成功率[31]。此外,机械通气的通气压力可能影响肺栓塞患者右向左分流,导致氧合指数(PaO2/FiO2)难以改善[32]。因此,APE患者应采用“肺保护及右心保护性通气”策略,即根据右心室功能调整通气参数[32]。APE动物实验显示,降低PEEP、过度通气以实现低碳酸血症与碱中毒,并提高FiO2,可降低平均肺动脉压(mean pulmonary arterial pressure,
mPAP)和PVR[27],从而改善右心室射血分数(right ventricle ejection fraction,RVEF)。撤除PEEP可降低mPAP和PVR,而增加PEEP(如增至20 cmH2O)除导致mPAP和PVR升高,还可能导致右心室射血分数、心输出量下降及低血压,引发右心室-肺循环解耦[33]。对于血流动力学不稳定肺栓塞,可暂时撤除PEEP,但需重新滴定PEEP以防止肺不张所致肺静脉阻力升高[33-34]。
肺保护性通气推荐小潮气量(4~8 mL/kg理想体重)、维持平台压(plateau pressure,Pplat)≤30 cmH2O(1 cmH2O=0.098 kPa)、驱动压<15 cmH2O,以降低呼吸功耗,减轻呼吸机相关肺损伤及肺血管损伤,FiO2宜<0.60以降低氧中毒风险[35-36]。右心室保护性通气则强调Pplat<27 cmH2O、驱动压<18 cmH2O和PEEP≤10 cmH2O,并通过调节呼吸频率维持动脉血二氧化碳分压(partial pressure of car-bon dioxide in arterial blood,PaCO2)<48 mmHg,避免高呼吸频率所致内源性PEEP[36]。俯卧位虽能减轻右心室负荷、改善通气,其在肺栓塞中的应用尚待研究。此外,肺栓塞严重指数、急性生理与慢性健康评分和简化急性生理评分在预测有创通气肺栓塞患者住院死亡率方面优于序贯器官衰竭评分(Sequential Organ Failure Assessment,SOFA)[37]。
机械通气还可能影响肺血管的纤溶活性,纤溶酶原激活物抑制剂1(plasminogen activator inhibitor-1,PAI-1)作为血管内皮损伤标志物,可抑制纤溶、促进血液高凝[38]。需要呼吸机辅助的患者,其PAI-1水平显著高于无需辅助的患者。研究表明,采用高潮气量、高PEEP、高氧浓度或导致低碳酸血症的机械通气策略,会提升肺组织PAI-1水平,与肺损伤加重相关[39-40]。在肺栓塞患者中,PAI-1水平升高与全因死亡风险呈正相关[41]。
此外,需警惕撤机相关肺水肿。在撤机过程中,通气由正压变为负压,胸腔内压力降低使静脉回流增加;对于右心功能不全的患者,右心室扩大可通过心室间相互依赖机制造成室间隔左移,进而导致心输出量减少、肺水肿等后果[42]。因此,建议对机械通气的肺栓塞患者在通气期间及撤机过程中,使用超声心动图密切监测右心功能。
4 ECMO支持模式
约70%的肺栓塞相关死亡发生在症状出现后的最初几小时内,对于血流动力学不稳定或发生心搏骤停的高危PE患者,有效治疗选择有限[43]。若初始治疗无效、出现难治性休克或心搏骤停前状态,可考虑采用VA-ECMO,以迅速稳定循环,减轻右心室负荷、改善右心功能(如缓解心肌缺血与功能障碍),同时改善肺水肿及氧合,为实现血栓清除治疗争取时间[44]。与VA-ECMO不同,静脉-静脉体外循环膜肺氧合(venovenous extracorporeal mem-brane oxygenation,VV-ECMO)无法有效降低右心室压力,因其回流血量仍依赖右心室产生足够的跨肺血流。因此,VV-ECMO不仅对高危肺栓塞患者治疗效果有限,还可能加重右心室功能障碍[45]。研究表明,SOFA评分可整合神经、血液、肝、肾及循环等多系统功能进行综合评估。若患者在48 h后出现高乳酸血症且SOFA评分上升,其住院死亡率显著增加。建议在ECMO治疗前48 h内连续性进行SOFA评分,以早期预测死亡风险[46]。另有研究显示,将ECMO与溶栓为基础的再灌注策略(包括全身溶栓、导管导向或外科取栓)联用应用,可显著降低并发症并提高生存率[47]。
高危肺栓塞患者启动ECMO的血流动力学标准包括:严重低血压(收缩压<90 mmHg)或对药物维持(如血管加压药、正性肌力药)的心搏骤停。超声心动图提示RVEF<30%,表现为右心衰竭伴低心输出量,且对正性肌力药及血管加压药无反应。呼吸标准为:即使采取高PEEP、俯卧位或吸入血管扩张剂等策略,仍存在严重低氧血症(PaO2/FiO2<100)或严重酸中毒(pH<7.2),伴乳酸>4 mmol/L,或进行性高碳酸血症(PaCO2>50 mmHg),提示通气不足与呼吸性酸中毒未能纠正[48]。目前仅少数医院具备开展VA-ECMO的条件,其成功实施依赖于包括ECMO专科医师和护士在内的多学科团队。然而即便在没有心脏外科支持的医疗中心,由重症监护室专家主导的ECMO会诊团队可成功完成VA-ECMO插管,救治高危肺栓塞患者[49]。
5小结
维持APE患者生命体征稳定,是后续治疗得以实施的重要基础。多数APE患者的低氧血症和低碳酸血症可通过鼻导管或面罩吸氧纠正。若低氧血症持续不能纠正,相较于NIPPV,更推荐采用HFNC,目标为将氧饱和度维持在90%以上。当患者出现严重低氧血症、呼吸衰竭或血流动力学不稳定,或上述情况并存时,应考虑行气管插管及有创机械通气。然而,机械通气可能显著影响APE合并右心衰竭患者的血流动力学:高潮气量、高PEEP可能增加肺血管阻力、降低右心室前负荷,并加重三尖瓣反流。因此,机械通气期间,应以最大限度减少其对血流动力学的干扰为目标。为防止插管后低血压甚至心搏骤停,建议提前建立有效的静脉通路,并备好血管加压药物。尤其对大面积肺栓塞的患者,PEEP的使用需格外谨慎,因其与急性右心室衰竭均与较高死亡率相关。对于药物治疗无效的高危肺栓塞患者,VA-ECMO可提供有效的机械辅助支持,快速稳定病情,为挽救生命创造机会。肺栓塞的呼吸支持策略应基于危险分层、合并症情况,并结合呼吸功能及右心功能的动态监测,进行个体化参数调整。多学科协作(涵盖呼吸危重症科、急诊科、ECMO团队、介入放射科、心脏内/外科、血管外科、临床药学科及超声科等)是提高救治成功率的关键。
综上所述,肺栓塞患者的机械通气应以肺保护为核心,在改善氧合与保护右心功能之间取得平衡。从传统氧疗到VA-ECMO,不同层级的呼吸支持手段各有特点,核心目标是在纠正低氧的同时减轻右心室负荷,通过个体化的镇静与通气策略,实现安全、有效的呼吸支持。
[参考文献]
[1]ROULEAU SG,CASEY SD,KABRHEL C,et al.Man-agement of high-risk pulmonary embolism in the emer-gency department:A narrative review[J].Am J Emerg Med,2024,79:1-11.
[2]YURIDITSKY E,LYHNE MD,HOROWITZ JM,et al.Critical care management of acute pulmonary embolism[J].J Intensive Care Med,2025,9:8850666241311512.
[3]LEE ES,BALTSEN CD,STUBBLEFIELD WB,et al.In-tubation and mechanical ventilation inPatients with acute pulmonary embolism:A scoping review[J].J Intensive Care Med,2026,41(1):3-11.
[4]ZHOU Y,NI Z,NI Y,et al.Comparison of actual perfor-mance in the flow and fraction of inspired O2 among dif-ferent high-flow nasal cannula devices:A bench study[J].Can Respir J,2021:6638048.
[5]中华医学会麻醉学分会五官科麻醉学组.经鼻高流量吸氧在五官科麻醉气道管理中应用专家共识(2025版)[J].中华医学杂志,2025,105(12):878-887.
[6]黄宇光,左明章,鲍红光,等.经鼻高流量氧疗临床麻醉规范应用专家共识(2023版)[J].临床麻醉学杂志,2023,39(8):881-887.
[7]李静静,马武华.经鼻高流量氧疗的应用与研究进展[J].国际麻醉学与复苏志,2022,43(8):866-871.
[8]MARWAH V,SHAFIN BABU PS,KATOCH CDS,et al.Effectiveness of high flow nasal cannula oxygen therapy in patients of acute pulmonary thromboembolism with acute hypoxemic respiratory failure[J].Med J Armed Forces India,2022,78(4):448-453.
[9]PÉREZ-NIETO OR,GÓMEZ-OROPEZA I,QUINTERO-LEYRA A,et al.Hemodynamic and respiratory support in pulmonary embolism:A narrative review[J].Front Med(Lausanne),2023,10:1123793.
[10]KOSTURA M,SMALLEY C,KOYFMAN A,et al.Right heart failure:A narrative review for emergency clinicians[J].Am J Emerg Med,2022,58:106-113.
[11]FREEMAN H,VRANAS KC,TUTHILL S,et al.High-flow nasal cannula liberation:Who,when,and how?[J].Chest,2025,168(5):1152-1161.
[12]LI J,ALBUAINAIN FA,TAN W,et al.The effects of flow settings during high-flow nasal cannula support for adult subjects:A systematic review[J].Crit Care,2023,27(1):78.
[13]RUAN SY,KUO YW,HUANG CT,et al.Effect of flow rates of high-flow nasal cannula on extubation out-comes:A randomized controlled trial[J].Chest,2024,167(5):1388-1396.
[14]VEIGA VC,SILVA LMCJ,SADYÉRR,et al.Epistaxis as a complication of high-flow nasal cannula therapy in adults[J].Rev Bras Ter Intensiva,2021,33(4):640-643.
[15]PANZUTI G,PISANI L,NAVA S.Bridging the gap:The role of non-invasive respiratory supports in wean-ing from invasive mechanical ventilation[J].J Clin Med,2025,14(20):7443.
[16]ROBERTS A.Understanding the principles of non-invasive positive pressure ventilation[J].Nurs Stand,2021,36(8):61-66.
[17]RITTAYAMAI N,PRAVARNPAT C,SRILAM W,et al.Safety and efficacy of noninvasive ventilation for acute respiratory failure in general medical ward:A prospec-tive cohort study[J].J Thorac Dis,2023,15(10):5466-5474.
[18]FRAT JP,GRIECO DL,DE JONG A,et al.Noninva-sive respiratory supports in ICU[J].Intensive Care Med,2025,51(8):1476-1489.
[19]ZHANG X,DONG Y,DIAO D,et al.A meta-analysis on the efficacy of noninvasive positive pressure ventila-tion combined with pressure support ventilation in treat-ing chronic heart failure[J].Clin Cardiol,2025,48(1):e70041.
[20]ASLAN SIRAKAYA H,FERRÁNDEZ AT,ESQUINAS AM,et al.Adverse events in non-invasive ventilation ap-proaches:Systematic review[J].Thorac Res Pract,2025,26(6):340-348.
[21]PELAIA C,ARMENTARO G,LUPIA C,et al.Effects of high-flow nasal cannula on right heart dysfunction in pa-tients with acute-on-chronic respiratory failure and pul-monary hypertension[J].J Clin Med,2023,12(17):5472.
[22]YU L,CHEN X,WANG X,et al.Efficacy and safety of high-flow nasal cannula versus noninvasive ventilation for pulmonary arterial hypertension-associated acute re-spiratory failure:A retrospective cohort study stratified by the severity of right ventricular dysfunction[J].Medi-cine(Baltimore),2025,104(27):e43185.
[23]GRIECO DL,MENGA LS,CESARANO M,et al.Effect of helmet noninvasive ventilation vs high-flow nasal oxy-gen on days free of respiratory support in patients with COVID-19 and moderate to severe hypoxemic respira-tory failure:The henivot randomized clinical trial[J].Jama-J Am Med Assoc,2021,325(17):1731-1743.
[24]DUAN J,LIU X,SHU W,et al.Low versus high posi-tive end expiratory pressure in noninvasive ventilation for hypoxemic respiratory failure:A multicenter random-ized controlled trial[J].Intensive Care Med,2025,51(5):861-869.
[25]CESARANO M,GRIECO DL,MICHI T,et al.Helmet noninvasive support for acute hypoxemic respiratory failure:Rationale,mechanism of action and bedside ap-plication[J].Ann Intensive Care,2022,12(1):94.
[26]KOBAYASHI T,PUGLIESE S,SETHI SS,et al.Con-temporary management and outcomes of patients with high-risk pulmonary embolism[J].J Am Coll Cardiol,2024,83(1):35-43.
[27]BALTSEN CD,ELLEGAARD MS,NØRHOLT C,et al.Mechanical ventilation in acute pulmonary embolism:A randomized,experimental,crossover study[J].Eur Heart J Acute Cardiovasc Care,2025,14(8):455-462.
[28]SHAH N,KATIRA BH.Role of cardiopulmonary interac-tions in development of ventilator-induced lung injury-experimental evidence and clinical Implications[J].Front Physiol,2023,14:1228476.
[29]MILLINGTON SJ,AISSAOUI N,BOWCOCK E,et al.High and intermediate risk pulmonary embolism in the ICU[J].Intensive Care Med,2024,50(2):195-208.
[30]CHERFAN P,ABOU ALI AN,ZAGHLOUL MS,et al.Propofol administration during catheter-directed inter-ventions for intermediate-risk pulmonary embolism is associated with major adverse events[J].J Vasc Surg Ve-nous Lymphat Disord,2021,9(3):621-626.
[31]JOHANNES J,BERLIN DA,PATEL P,et al.A tech-nique of awake bronchoscopic endotracheal intubation for respiratory failure in patients with right heart failure and pulmonary hypertension[J].Crit Care Med,2017,45(9):e980-e984.
[32]YUSUFF H,CHAWLA S,SATO R,et al.Mechanisms of acute right ventricular injury in cardiothoracic surgi-cal and critical care settings:Part 2[J].J Cardiothorac Vasc Anesthesia,2023,37(11):2318-2326.
[33]WOOD G,MADSEN TL,KIM WY,et al.Increasing levels of positive end-expiratory pressure cause step-wise biventricular stroke work reduction in a porcine model[J].Anesthesiology,2024,140(2):240-250.
[34]COLLINO F,RAPETTI F,VASQUES F,et al.Positive end-expiratory pressure and mechanical power[J].Anes-thesiology,2019,130(1):119-130.
[35]DELLWEG D,LEPPER PM.Technical aspects and in-novations in non-invasive and invasive ventilation[J].Pneumologie,2024,78(2):120-130.
[36]KALLET RH.Mechanical ventilation in ARDS:Ouo va-dis?[J].Resp Care,2022,67(6):730-749.
[37]DEVESA NETO V,CORREIA J,FIUZA J,et al.Pre-diction of in-hospital mortality in patients with acute pulmonary embolism requiring invasive mechanical ven-tilation:Comparison of risk scores[J].Eur Heart J Acute Cardiovasc Care,2023,12(Suppl 1)zuad036.105.
[38]CIVIRJIC C,DIACONU N,GROSU A,et al.Investiga-tion of plasminogen activator inhibitor-1(PAI-1)4G/5G promoter polymorphism and other thrombophilia genes in patients with acute pulmonary embolism[J].Eur Heart J,2023,44(Supple2)ehad655.1954.
[39]BAUMANN P,GRECO F,L'ABATE P,et al.Lung-borne systemic inflammation in mechanically ventilated infant rats due to high PEEP,oxygen,and hypocapnia[J].Am J Transl Res,2022,14(1):343-354.
[40]REN JM,WANG GF,BI J,et al.High tidal volume me-chanical ventilation exacerbates pulmonary injury via upregulation of PAI-1 expression in rats[J].Hereditas,2025,162(1):129.
[41]ROSSI V,MEIER D,WANG Y,et al.Interleukin 21,plasminogen activator inhibitor 1 and fractalkine improve risk stratification in elderly patients with pulmonary em-bolism[J].Eur Heart J,2024,45(Supple1)ehae666.2207.
[42]JOZWIAK M,TEBOUL JL.Heart-Lungs interactions:The basics and clinical implications[J].Ann Intensive Care,2024,14(1):122.
[43]ABDULAZIZ S,KAKAR V,KUMAR PG,et al.Me-chanical circulatory support for massive pulmonary em-bolism[J].J Am Heart Assoc,2025,14(1):e036101.
[44]ELMADHOUN O,ESMAEILZADEH S,MERREN MP,et al.Extracorporeal membrane oxygenation in pulmo-nary embolism:Current evidence and evolving data[J].J Cardiothorac Vasc Anesth,2025,39(6):1556-1563.
[45]GOLDBERG JB,GIRI J,KOBAYASHI T,et al.Surgi-cal management and mechanical circulatory support in high-risk pulmonary embolisms:Historical context,cur-rent status,and future directions:A scientific statement from the american heart association[J].Circulation,2023,147(9):e628-e647.
[46]LAIMOUD M,ALANAZI M.The validity of SOFA score to predict mortality in adult patients with cardio-genic shock on venoarterial extracorporeal membrane oxygenation[J].Crit Care Res Prac,2020:3129864.
[47]FARMAKIS IT,SAGOSCHEN I,BARCO S,et al.Ex-tracorporeal membrane oxygenation and reperfusion strategies in high-risk pulmonary embolism hospitaliza-tions[J].Crit Care Med,2024,52(10):e512-e521.
[48]BARAN C,KAYAN A,BARAN CS,et al.Algorithm of high-risk massive pulmonary thromboembolism with ex-tracorporeal membrane oxygenation[J].J Clin Med,2024,13(22):6822.
[49]PRASAD NK,BOYAJIAN G,TRAN D,et al.Veno-arterial extracorporeal membrane oxygenation for pulmo-nary embolism after systemic thrombolysis[J].Semin Thorac Cardiovasc Surg,2022,34(2):549-557.










