氨基酰化酶 1 激活 AKT 以及 ERK 通路促进骨肉瘤细胞上皮-间质转化论文
2026-04-15 11:45:44 来源: 作者:xuling
摘要:目的探究氨基酰化酶1(aminoacylase 1,ACY1)激活蛋白激酶B(protein kinase B,AKT)以及胞外信号调节激酶(extracellular signal-regulated kinase,ERK)通路促进骨肉瘤(osteosarcoma,OS)细胞上皮-间质转化(epithelial-mesenchymal transition,EMT)的机制。
[摘要]目的探究氨基酰化酶1(aminoacylase 1,ACY1)激活蛋白激酶B(protein kinase B,AKT)以及胞外信号调节激酶(extracellular signal-regulated kinase,ERK)通路促进骨肉瘤(osteosarcoma,OS)细胞上皮-间质转化(epithelial-mesenchymal transition,EMT)的机制。方法采用实时荧光定量PCR和蛋白质印迹法检测成骨细胞系hFOB 1.19与OS细胞系(Saos-2、U2OS、HOS、MG-63)中ACY1的表达水平。通过慢病毒构建ACY1沉默的Saos-2细胞(shACY1组,以shNC组为对照)和ACY1过表达的MG-63细胞(ACY1组,以Vector组为对照),借助CCK-8、克隆形成、划痕愈合及Transwell侵袭实验分析ACY1对OS细胞增殖、迁移和侵袭的影响,蛋白质印迹法检测EMT标志蛋白(N-cadherin、Vimentin、E-cadherin)及通路相关蛋白表达;构建荷瘤裸鼠模型,验证ACY1沉默和过表达对体内肿瘤生长、EMT及AKT和ERK通路的作用。结果OS细胞系(Saos-2、U2OS、HOS、MG-63)中ACY1的mRNA和蛋白水平显著高于成骨细胞系hFOB 1.19,差异均有统计学意义(P均<0.05)。与shNC组相比,shACY1组细胞的ACY1蛋白的水平、细胞活力、增殖、迁移、侵袭能力、N-cadherin、Vimentin水平更低,AKT1和ERK1/2蛋白磷酸化水平明显下调;而ACY1组与Vector组相比,上述指标均更高,差异均有统计学意义(P均<0.05)。shACY1组E-cadherin水平高于shNC组,ACY1组E-cadherin水平低于Vector组,差异均有统计学意义(P均<0.05)。裸鼠实验中,shACY1组肿瘤质量、肿瘤组织中N-cadherin、Vimentin蛋白水平及AKT1/ERK1/2磷酸化水平低于shNC组,ACY1组的上述指标高于Vector组,差异均有统计学意义(P均<0.05)。裸鼠实验中,shACY1组E-cadherin水平高于shNC组,ACY1组E-cadherin水平低于Vector组,差异均有统计学意义(P均<0.05)。结论ACY1在OS细胞中上调且激活AKT和ERK通路,促进EMT。
[关键词]骨肉瘤;氨基酰化酶1;上皮-间质转化
骨肉瘤(osteosarcoma,OS)是一种好发生于儿童和青少年的恶性肿瘤。现阶段,化疗药物联合手术治疗可使部分患者保留患病肢体,并提高5年生存率[1]。然而,转移与复发仍是导致OS预后不良的重要因素,发生转移的OS患者生存率仅为20%[2],分析OS转移机制对寻找生物标志物和治疗靶点具有重要意义。上皮-间质转化(epithelial-mesenchymal transition,EMT)是指细胞与邻近细胞的紧密黏附、极性和上皮结构丧失并获得间质表型,其特征是迁移能力、侵袭性和迁移能力增强,EMT是OS获得转移能力的重要途径[3]。氨基酰化酶1(aminoacylase 1,ACY1)是一种锌结合金属酶,主要存在于细胞质中,在哺乳动物组织中广泛表达。ACY1通过催化N-酰化氨基酸水解为L-氨基酸和酰基,从而调节蛋白质稳定性[4]。研究表明ACY1在人类癌症中发挥作用,ACY1在肺癌中过表达且与免疫抑制相关[5]。在肝细胞癌中,ACY1能够通过调节转化生长因子β1促进EMT[6]。值得注意的是,转化生长因子β1是诱导OS细胞EMT的重要通路[7]。然而,ACY1是否会促进OS细胞的EMT则仍不清楚。据此,本研究分析ACY1对OS细胞以及EMT的影响,并探究其作用机制。
1材料与方法
1.1细胞培养与转染
将人成骨细胞系hFOB 1.19(美国ATCC公司)与人OS细胞系Saos-2、U2OS、HOS和MG-63(美国ATCC公司)培养于DMEM培养基(含10%胎牛血清及1%谷氨酰胺),环境条件设置为37℃、5%CO 2。根据1.2和1.3的方法分别检测hFOB 1.19、Saos-2、U2OS、HOS和MG-63细胞中ACY1 mRNA和蛋白水平。
依据ACY1表达水平筛选实验细胞:选取ACY1相对高表达的Saos-2细胞用于沉默实验,选取ACY1相对低表达的MG-63细胞用于过表达实验。将Saos-2细胞分为shNC组和shACY1组,针对Saos-2细胞的沉默实验,设计3种sh-ACY1序列(sh-ACY1-1、sh-ACY1-2、sh-ACY1-3)并将其分别插入pGMLV-SC5载体,转染Saos-2细胞后通过检测筛选沉默效率最高的sh-ACY1序列,用于后续shACY1组的构建。shNC组细胞转染包含sh-NC的pGMLV-SC5载体,作为对照。将MG-63细胞分为空载体(Vector)组和ACY1组。针对MG-63细胞的过表达实验,构建ACY1 pcDNA 3.1过表达载体,以空载体(Vector)作为对照,分别转染MG-63细胞构建ACY1组和Vector组。sh-ACY1和ACY1 pcDNA 3.1的转染方法如下:转染体系包含1.5×105个细胞、慢病毒载体(感染复数=10)和聚凝胶(5μg/mL)。转染24 h后通过检测ACY1的mRNA及蛋白水平评估转染效率。
1.2实时荧光定量PCR(RT-qPCR)
裂解细胞萃取总RNA并通过逆转录cDNA试剂盒(美国Thermo Fisher Scientific公司)合成cDNA。采用SYBR Green PCR预混液(瑞士Roche公司)与PCR检测系统进行qPCR实验。PCR循环程序:95℃预变性10 min;94℃下15 s、60℃下1 min进行40个循环;最终60℃延伸1 min后4℃保存。采用比较循环阈值法分析RNA表达,以GAPDH作为内参基因。引物序列见表1。
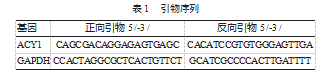
1.3蛋白质印迹法(Western blot)
使用BCA试剂盒测定总蛋白浓度,通过SDS-PAGE(恒定电压110 V,电泳100 min)进行蛋白分离,随后转膜至PVDF膜(恒定电压90 V,转膜90 min)。用5%脱脂牛奶封闭PVDF膜1 h,加入1∶500稀释的一抗(美国Abcam公司)4°C孵育过夜。随后以1:5 000稀释的二抗(sc-516102、sc-2357,美国Santa Cruz Biotechnology公司)室温孵育2 h。最后采用Pierce™ECL化学发光底物(美国Thermo Fisher公司)于ChemiDoc MP成像系统(美国Bio-Rad公司)检测蛋白条带。检测的蛋白包括ACY1蛋白、EMT标志蛋白(N-cadherin、Vimentin、E-cadherin)、蛋白激酶B(protein kinase B,AKT)通路与胞外信号调节激酶(extracellular signal-regulated kinase,ERK)通路及其他通路激活相关蛋白。
1.4 CCK-8检测细胞活力
将细胞以每孔1×104个细胞(100μl)的密度接种于96孔板。培养48 h后,每孔加入10μl CCK-8试剂(中国碧云天公司),37℃继续孵育2 h。使用酶标仪(瑞士Tecan Infinite M200)在450 nm波长处测量光密度值。
1.5克隆形成实验
将500个细胞接种于6孔板每孔中。培养48 h后,用甲醇固定细胞集落,0.5%结晶紫染色20 min。在显微镜下观察并计数细胞集落。
1.6划痕愈合实验
将1×106个细胞接种于6孔板,培养至90%融合度。用200μl移液器吸头划痕后洗涤细胞,继续培养24 h。使用倒置显微镜(日本奥林巴斯IX71)拍摄划痕区域图像。
1.7 Transwell侵袭实验
将1×105个细胞接种于铺有基质胶(8μm孔径,美国BD Biosciences公司)的Transwell上室。下室加入完全培养基作为化学引诱剂。48 h后取出Transwell装置,洗涤后使用20%甲醇固定细胞,0.2%结晶紫染色,通过倒置显微镜(日本奥林巴斯IX71)观察。
1.8裸鼠异种移植瘤模型
4周龄、雄性、体质量为16~18 g的BALB/c裸鼠购自北京维通利华公司,在咸宁市第一人民医院的实验动物中心SPF级屏障设施内,标准条件下(12/12 h明暗循环,自由进食饮水)饲养。裸鼠分组1(n=4):shNC组和shACY1组,分别利用shNC组与shACY1组的Saos-2细胞构建荷瘤裸鼠模型;裸鼠分组2(n=4):Vector组和ACY1组,分别利用Vector组和ACY1组的MG-63细胞构建荷瘤裸鼠模型。每组裸鼠皮下注射1×106个相应细胞,分别注射到无特定病原体级4周龄BALB/c裸鼠腋下。注射28d后处死裸鼠,取出肿瘤组织进行称重与拍照。本实验经咸宁市第一人民医院伦理委员会批准(No.012-202511-02)并在实验过程中最大限度减轻动物痛苦。
1.9统计方法
使用GraphPad Prism 7统计学软件进行统计分析,组间比较采用两独立样本t检验。P<0.05为差异有统计学意义。
2结果
2.1成骨细胞系hFOB 1.19与OS细胞系中ACY1 mRNA和蛋白水平比较
OS细胞U2OS、Saos-2、HOS和MG-63中ACY1 mRNA和蛋白的表达水平高于成骨细胞hFOB 1.19,差异均有统计学意义(P均<0.05),见图1。
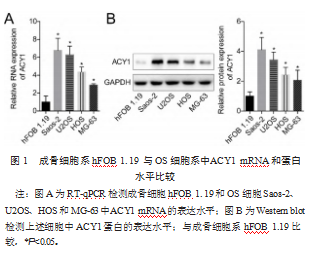
U2OS、HOS和MG-63中ACY1 mRNA的表达水平;图B为Western blot检测上述细胞中ACY1蛋白的表达水平;与成骨细胞系hFOB 1.19比较,*P<0.05。
2.2 ACY1沉默与过表达对OS细胞ACY1蛋白水平、细胞活力及增殖能力的影响分析
shACY1组的ACY1蛋白的水平低于shNC组,ACY1组的ACY1蛋白水平高于Vector组,差异均有统计学意义(P均<0.05),见图2A、图2B。shACY1组的细胞活力低于shNC组,ACY1组的细胞活力高于Vector组,差异均有统计学意义(P均<0.05),见图2C、图2D。shACY1组的增殖能力低于shNC组,ACY1组的增殖能力高于Vector组,差异均有统计学意义(P均<0.05),见图2E、图2F。
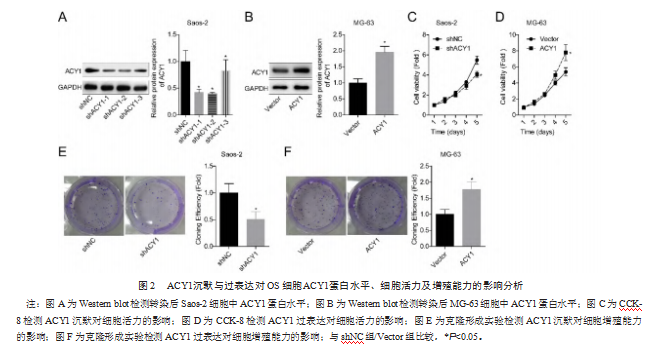
2.3 ACY1沉默与过表达对OS细胞迁移和侵袭能力的影响分析
shACY1组细胞迁移能力与细胞侵袭能力低于shNC组,ACY1组细胞迁移能力与细胞侵袭能力高于Vector组,差异均有统计学意义(P均<0.05),见图3。
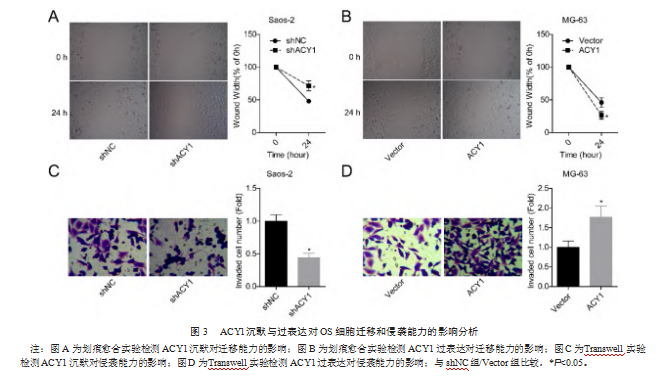
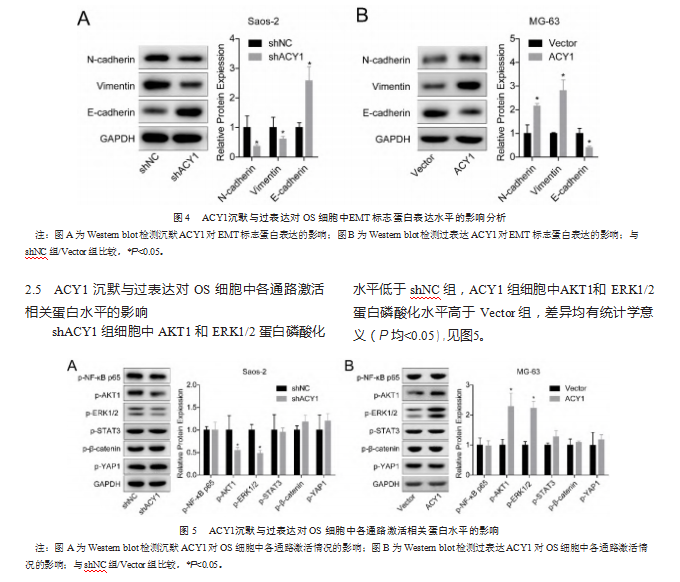
2.4 ACY1沉默与过表达对OS细胞中EMT标志蛋白表达水平的影响分析
shACY1组细胞中N-cadherin和Vimentin蛋白水平低于shNC组,E-cadherin蛋白水平高于shNC组,差异均有统计学意义(P均<0.05),见图4A。ACY1组细胞中N-cadherin和Vimentin蛋白水平高于Vector组,E-cadherin蛋白水平低于Vector组,差异均有统计学意义(P均<0.05),见图4B。
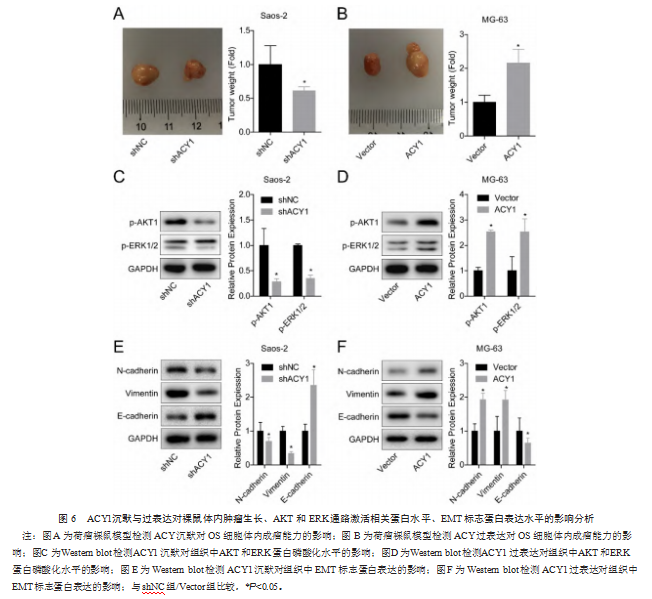
2.6 ACY1沉默与过表达对裸鼠体内肿瘤生长、AKT和ERK蛋白磷酸化水平、EMT标志蛋白表达水平的影响分析
shACY1组的肿瘤质量小于shNC组,ACY1组的肿瘤质量高于Vector组,差异均有统计学意义(P均<0.05),见图6A、图6B。shACY1组肿瘤组织中AKT1和ERK1/2蛋白磷酸化水平低于shNC组,ACY1组肿瘤组织中AKT1和ERK1/2蛋白磷酸化水平高于Vector组,差异均有统计学意义(P均<0.05),见图6C、图6D。shACY1组肿瘤组织中N-cadherin和Vi⁃mentin蛋白水平低于shNC组,E-cadherin蛋白水平显著高于shNC组;ACY1组肿瘤组织中N-cadherin和Vimentin蛋白水平高于Vector组,E-cadherin蛋白水平低于Vector组,差异均有统计学意义(P均<0.05),见图6E、图6F。
3讨论
转移是导致OS患者预后不良的主要原因,对于发生转移和复发的OS患者,放化疗效果有限,死亡率高[8]。因此,研究OS细胞增殖与转移的机制具有重要意义。
在正常机体内,ACY1蛋白在肾脏和脑中表达,主要以蛋白酶形式定位于细胞质,ACY1能够水解细胞内蛋白质N端肽段的α-酰化氨基酸,且有研究表明ACY1功能失调可能引发自闭症与惊厥[9]。ACY1水平与多种肿瘤相关,但是在不同癌症中ACY1的作用可能不同,如在结直肠癌中,ACY1过表达且高水平ACY1与结直肠晚期TNM分期、淋巴结转移、血管侵犯阳性及低生存率显著相关;体外实验也证实沉默ACY1可显著抑制HCT116细胞增殖并诱导细胞凋亡[10]。GUO M等[11]的研究发现ACY1在前列腺癌中上调,且高水平的ACY1与不良预后有关。而在神经母细胞瘤中,靶向抑制ACY-1能够促进神经母细胞瘤细胞的迁移和侵袭[12]。肾透明细胞癌组织中ACY1的表达均下调,体外提高ACY1蛋白水平会促进肾透明细胞癌的细胞活力和迁移能力[13]。但是ACY1在OS中的作用仍不清楚。本研究结果显示OS细胞系中ACY1上调,且沉默ACY1导致细胞增殖、迁移和侵袭能力均减弱,而过表达ACY1显著促进MG-63细胞的增殖、迁移和侵袭。这初步提示ACY1在OS中发挥促癌作用。
本研究探讨ACY1在OS中的调控机制,结果显示沉默ACY1显著抑制EMT并降低AKT1和ERK1/2蛋白磷酸化水平,而过表达ACY1则促进EMT,并升高了AKT1和ERK1/2蛋白磷酸化水平。AKT与ERK均是受体酪氨酸激酶下游信号通路中的关键蛋白,研究表明激活AKT通路能够显著促进OS细胞的EMT[14]。而抑制ERK通路则会导致OS细胞的EMT能力显著减弱[15]。此外,过往研究表明ACY1具有参与细胞内信号转导的作用,CHEN H等[16]的研究显示ACY1可通过激活AKT通路促进非小细胞肺癌进展。也有研究显示ACY1的升高会促进胶质母细胞瘤中ERK蛋白磷酸化[17]。本研究的动物实验结果显示,ACY1具有激活OS肿瘤组织中AKT和ERK通路的作用,提示ACY1会激活AKT和ERK通路并促进OS细胞EMT,提高OS细胞迁移和侵袭能力。
本研究也存在一些不足之处,首先关于ACY1在OS中的临床表达特点和与病理学的关系仍需要进一步研究,关于ACY1调控AKT和ERK通路的具体机制也需要进一步探索,这也是后续研究重点。
综上所述,ACY1在OS细胞中上调且激活AKT和ERK通路促进EMT,这可能促进OS进展并成为治疗的新靶点。
[参考文献]
[1]BRAY F,LAVERSANNE M,SUNG H,et al.Global cancer statistics 2022:GLOBOCAN estimates of inci⁃dence and mortality worldwide for 36 cancers in 185 countries[J].CA Cancer J Clin,2024,74(3):229-263.
[2]ZHOU C,LI H,ZENG H,et al.Incidence trends,overall survival,and metastasis prediction using multiple ma⁃chine learning and deep learning techniques in pediatric and adolescent population with osteosarcoma and Ew⁃ing/s sarcoma:Nomogram and webpage[J].Clin Transl Oncol,2025,27(5):2327-2338.
[3]PATRAS,CU AV,T,ARCĂE,LOZNEANU L,et al.The role of epithelial-mesenchymal transition in osteosar⁃coma progression:From biology to therapy[J].Diagnostics,2025,15(5):644-657.
[4]AL-MALIKI MJH,ALLAHYARI M,ABBASI A,et al.Hyperglycemia correlated with elevated circulating ami⁃noacylase 1 in patients with pre-diabetes and type 2 dia⁃betes[J].J Diabetes Metab Disord,2025,24(1):139.
[5]XU J,YUAN L,WU H,et al.Sargentodoxa cuneata sup⁃presses lung adenocarcinoma progression by enhancing cytotoxic CD8+T activity through the ACY1/ARG2 inter⁃action[J].Cytotechnology,2025,77(5):185.
[6]WEI X,LI J,XIE H,et al.Proteomics-based identification of the tumor suppressor role of aminoacylase 1 in hepato⁃cellular carcinoma[J].Cancer Lett,2014,351(1):117-125.
[7]LI AA,ZHANG Y,LI F,et al.The mechanism of VCP-mediated metastasis of osteosarcoma based on cell au⁃tophagy and the EMT pathway[J].Clin Transl Oncol,2023,25(3):653-661.
[8]SU Z,HUANG F,YIN C,et al.Clinical model of pulmo⁃nary metastasis in patients with osteosarcoma:A new multiple machine learning-based risk prediction[J].J Or⁃thop Surg,2023,31(2):10225536231177102.
[9]HAEGER G,JOLMES T,OYEN S,et al.Novel recombi⁃nant aminoacylase from paraburkholderia monticola ca⁃pable of N-acyl-amino acid synthesis[J].Appl Microbiol Biotechnol,2024,108(1):93.
[10]SHI H,HAYES MT,KIRANA C,et al.Overexpression of aminoacylase 1 is associated with colorectal cancer progression[J].Hum Pathol,2013,44(6):1089-1097.
[11]GUO M,LIANG S,GUAN Z,et al.Prostate cancer and metabolic syndrome:Exploring shared signature genes through integrative analysis of bioinformatics and clini⁃cal data[J].Discov Oncol,2025,16(1):698.
[12]SUN J,ZHANG X,CHEN Z,et al.MiR-1271-5p pro⁃motes the growth and migration of neuroblastoma cells by regulating ACY-1[J].Transl Cancer Res,2024,13(7):3397-3406.
[13]WANG G,LI H,HOU Y.LncRNA MAGI2-AS3 inhib⁃its tumor progression and angiogenesis by regulating ACY1 via interacting with transcription factor HEY 1 in clear cell renal cell carcinoma[J].Cancer Gene Ther,2022,29(5):585-596.
[14]ZHOU R,WU H,YOU H,et al.ESPN activates ZEB 1-mediated EMT through the PI3K/AKT/mTOR axis to promote osteosarcoma metastasis[J].J Transl Med,2025,23(1):527.
[15]XIA K,ZHENG D,WEI Z,et al.TRIM26 inhibited os⁃teosarcoma progression through destabilizing RACK1 and thus inactivation of MEK/ERK signaling[J].Cell Death Dis,2023,14(8):529.
[16]CHEN H,WANG W,XIAO C,et al.ACY1 regulating PTEN/PI3K/AKT signaling in the promotion of non-small cell lung cancer progression[J].Ann Transl Med,2021,9(17):1378-1389.
[17]ZOU L,WANG W,HUANG W,et al.FYN-mediated phosphorylation of BCKDK at Y 151 promotes GBM pro⁃liferation by increasing the oncogenic metabolite N-acetyl-L-alanine[J].Heliyon,2024,10(15):e33663.










