M1/M2 型巨噬细胞在牙周炎骨破坏中的作用及可能机制论文
2026-04-15 10:21:38 来源: 作者:xuling
摘要:目的分析牙周炎骨破坏中M1/M2型巨噬细胞所发挥的作用以及可能的作用机制。方法2025年3—10月齐齐哈尔医学院医学技术学院临床病原教研室选取6~8周龄C57BL/6小鼠6只,构建牙周炎动物模型。
[摘要]目的分析牙周炎骨破坏中M1/M2型巨噬细胞所发挥的作用以及可能的作用机制。方法2025年3—10月齐齐哈尔医学院医学技术学院临床病原教研室选取6~8周龄C57BL/6小鼠6只,构建牙周炎动物模型。模型构建成功后处死小鼠,分离双侧上颌骨标本,经组织学染色处理后,观察骨组织破坏形态及程度。对制备的石蜡切片进行组织学染色及免疫组化检测,检测巨噬细胞表面标志物分化抗原簇68(cluster of differen⁃tiation 68,CD68)、分化抗原簇86(cluster of differentiation 86,CD86)及分化抗原簇163(cluster of differentiation,CD163)的表达情况。另从小鼠骨髓中分离单核细胞,体外诱导分化为原代M1、M2型巨噬细胞;收集诱导成功的M1、M2型巨噬细胞条件培养基,将两种巨噬细胞分别与成骨细胞进行共培养,实验分组设为对照组(MC组)、M 1型巨噬细胞共培养组(MC-M 1组)及M2型巨噬细胞共培养组(MC-M2组)。培养结束后提取各组细胞总蛋白,采用蛋白质印迹法检测成骨细胞中runt相关转录因子2(runt-related transcription factor 2,Runx2)、骨钙素(osteocalcin,Ocn)的蛋白表达水平。结果牙周炎动物模型组织标本显示,牙槽骨呈现病理损伤:骨组织排列紊乱、结构完整性破坏,骨小梁稀疏且连续性中断,骨量减少,符合牙周炎典型病理改变特征。免疫组织化显示,骨吸收表面可见大量巨噬细胞浸润,骨吸收周缘M1和M2型巨噬细胞浸润。经蛋白质印迹法检测发现,M 1、M2型巨噬细胞上清刺激成骨细胞后,成骨细胞中Runx2和Ocn表达减少。结论M 1、M2型巨噬细胞均能抑制成骨细胞分化关键因子Runx2与Ocn的表达,从而干扰成骨过程、促进牙周炎骨破坏。其中,M 1型巨噬细胞的抑制作用强于M2型,表明其可能是驱动牙周炎性骨丧失的关键效应细胞。
[关键词]牙周炎;骨破坏;巨噬细胞
牙周炎的发生与发展与巨噬细胞存在着紧密联系[1-3]。巨噬细胞具有不同类型,其中M 1型巨噬细胞可激活持续性炎症反应,能够分泌肿瘤坏死因子α(tumor necrosis factor-α,TNF-α)、白细胞介素6(interleukin 6,IL-6)等促炎细胞因子,同时还可分泌活性氧,进而激活持续性炎症反应,最终导致牙周组织受损。M2型巨噬细胞能够分泌白细胞介素10等多种抗炎因子,以及血管内皮生长因子、血小板衍生生长因子等生长因子,可清除炎症并促进组织修复。巨噬细胞具备清除人体炎症以及修复组织的功能。上述两种巨噬细胞的动态平衡与牙周炎的进展密切相关[4-5]。M 1型巨噬细胞会引发牙槽骨吸收,而M2型巨噬细胞通过分泌骨保护素等分子,抑制破骨细胞的分化与活化,促进骨生成。基于此,本研究通过构建牙周炎动物模型,剖析上述细胞在牙周炎骨破坏中的作用及潜在机制。
1材料与方法
1.1实验材料
2025年3—10月齐齐哈尔医学院医学技术学院临床病原教研室选取6只6~8周龄C57BL/6小鼠为实验动物,小鼠购自南京大学模式动物研究所,雌雄各3只。所有实验小鼠均健康无病,体质量均维持在20 g左右。本研究经齐齐哈尔医学院附属第二医院实验动物伦理委员会批准[伦科审(2025)02第028号-01]。采用丝线结扎法构建小鼠牙周炎模型,建模前对所有小鼠腹腔注射0.2%戊巴比妥钠(剂量为0.3 mL/100 g)行麻醉处理,随后以5-0无菌丝线结扎右上颌第二磨牙,结扎时将丝线尽量探入龈沟内以避免松脱。建模完毕后,所有小鼠均常规给予标准鼠粮及饮水,饲养于SPF级动物房内,保持饲养环境洁净卫生,每周更换垫料2次。每日密切观察小鼠的精神状态、进食情况及牙周组织外观表现,待小鼠出现典型牙周炎症状时,对其行CT扫描检测,若影像学结果显示伴发明显牙槽骨重度吸收,则判定牙周炎模型构建成功。
1.2实验方法
1.2.1骨组织破坏情况观察建模后将小鼠连续饲养7 d,观察确认结扎丝线无脱落,随后对小鼠行腹腔麻醉,待麻醉生效后采用脱颈法处死。解剖小鼠并完整分离双侧上颌骨组织,置于4%多聚甲醛溶液中固定,妥善保存备用。取固定后的上颌骨组织标本进行组织学染色,具体操作流程如下:先将制备好的组织石蜡切片进行脱蜡、水化处理;随后采用苏木精溶液染色5 min,染色结束后用蒸馏水充分冲洗;经盐酸酒精进行分化处理,再以蒸馏水冲洗;之后采用返蓝液进行返蓝处理,继而用伊红溶液染色5 min;染色完成后对切片进行梯度脱水、透明化处理,最后滴加中性树胶封片。封片完成后,在光学显微镜下观察切片,记录并分析牙周炎模型小鼠骨组织的病理损伤情况。牙周炎典型病理特征表现为:牙龈上皮结构完整性破坏,上皮组织向根方显著迁移、增殖;上皮下纤维结缔组织呈病理性增生改变;局部组织内可见大量炎症细胞浸润;牙槽嵴高度明显降低。
1.2.2巨噬细胞浸润情况观察采用免疫组织化学染色法检测石蜡切片中牙周组织内分化抗原簇68(cluster of differentiation 68,CD68)、分化抗原簇86(cluster of differentiation 86,CD86)及分化抗原簇163(cluster of differentiation,CD163)的表达情况。石蜡切片后脱蜡水化:将制备好的组织石蜡切片依次进行脱蜡、梯度酒精水化处理,随后置于磷酸盐缓冲液中,摇床振荡洗涤3次,3 min/次。抗原修复:将切片浸入柠檬酸修复液中,连同烧杯置于水浴加热装置内加热15 min;自然冷却后,转入磷酸盐缓冲液中摇床振荡洗涤3次,3 min/次。内源性过氧化物酶阻断:向每张切片滴加50μl 3%过氧化氢溶液,置于37℃恒温箱内孵育15 min,以阻断内源性过氧化物酶活性;之后将切片移入磷酸盐缓冲液吐温缓冲液中,摇床振荡洗涤3次,3 min/次。封闭与一抗孵育:滴加山羊血清进行封闭,37℃孵育15 min;倾去封闭液,每张切片滴加50μl一抗工作液(CD68、CD86、CD163抗体),置于4℃冰箱中孵育过夜。二抗孵育:次日将切片取出,室温复温1 h,随后转入磷酸盐缓冲液吐温缓冲液中摇床振荡洗涤3次,3 min/次;每张切片滴加50μl快捷型酶标羊抗鼠/抗兔免疫球蛋白G聚合物,37℃孵育15 min,再次以磷酸盐缓冲液吐温缓冲液摇床振荡洗涤3次,3 min/次。显色与复染:滴加二氨基联苯胺显色剂,室温下孵育10 s,待切片出现特异性染色后,立即用自来水充分冲洗终止显色;将切片浸入苏木素染液中进行细胞核复染,时间10 min;自来水冲洗后,经1%盐酸乙醇分化、碳酸锂溶液返蓝。脱水封片与观察:将切片依次进行梯度酒精脱水、透明处理,中性树胶封片;待封片剂完全干燥后,在光学显微镜下观察染色结果,记录并分析牙周炎模型小鼠骨组织内巨噬细胞的浸润程度与分布特征。
1.2.3巨噬细胞诱导与条件培养基制备小鼠经麻醉处理后采用脱颈法处死,无菌条件下解剖并分离四肢,转移至超净工作台剔除四肢骨周围附着的肌肉组织,用含3%双抗的磷酸盐缓冲液冲洗,配置含3%胎牛血清的DMEM高糖培养基进行骨髓腔冲洗,收集混悬以2 000 rpm,12.5 cm半径进行离心处理,时间20 min,从小鼠骨髓中分离单核细胞,分别用脂多糖/干扰素-γ和白细胞介素4诱导,获得原代M1、M2型巨噬细胞,用于后续实验。对上述细胞进行培养,观察细胞生长情况,待细胞长至60%~70%时,添加20 ng/mL干扰素-γ、20 ng/mL白细胞介素4+白细胞介素13分别分化为M 1、M2。实施24 h的刺激,之后弃掉上清,添加新鲜的DMEM高糖,再培养24 h,采集上清,以2 000 rpm,12.5 cm半径进行离心,时间20 min,离心完毕后,获得M1、M2型巨噬细胞条件培养基。
1.2.4成骨细胞共培养与蛋白检测将诱导分化获得M 1和M2型巨噬细胞与成骨细胞实施上下室共培养,之后实施超声裂解。处理完毕后上离心机进行离心处理,以12 000 r/min转速,12.5 cm半径离心10 min,将上清转移至新的EP管中,测定样本浓度,加入蛋白上样缓冲液煮沸,待其冷却后放入-80℃保存备用。分别设置MC(对照组),M 1型巨噬细胞共培养组(MC-M 1组)及M2型巨噬细胞共培养组(MC-M2组),按照上述方式提取细胞蛋白,通过蛋白质印迹法检测方式,分析成骨细胞中runt相关转录因子2(runt-related transcription factor 2,Runx2)、骨钙素(osteocalcin,Ocn)的表达水平。
1.3观察指标
采集动物模型组织标本,进行组织学染色及免疫组化检测,观察检测结果,分析牙周炎后对动物模型骨组织的破坏情况,以及组织中巨噬细胞的浸润情况。获得M1、M2型巨噬细胞,与成骨细胞共培养,检测成骨细胞中Runx2、Ocn的表达水平,统计蛋白质印迹法检测结果。
2结果
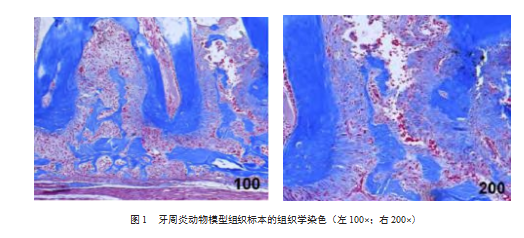
2.1牙周炎动物模型组织标本的组织学染色检测结果
组织学染色结果显示,牙周炎模型小鼠的牙槽骨呈现病理损伤:骨组织排列紊乱、结构完整性破坏,骨小梁稀疏且连续性中断,骨量减少,符合牙周炎典型病理改变特征。见图1。
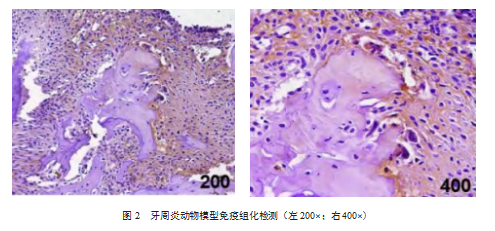
2.2牙周炎动物模型组织标本的免疫组化检测结果
免疫组织化学染色结果显示,牙周炎模型小鼠牙槽骨吸收区域呈现明显的巨噬细胞浸润现象:骨吸收表面及周围组织中,巨噬细胞表面标志物CD68、CD86及CD163均呈阳性表达,且阳性细胞主要集中分布于骨吸收周缘及炎症浸润区域。见图2。
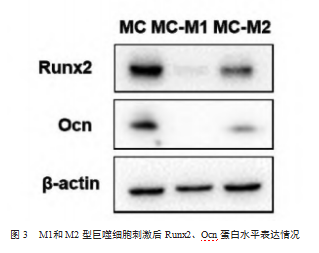
2.3 M1型和M2型巨噬细胞中CD68和CD163蛋白表达水平
经蛋白质印迹法结果显示,M 1、M2型巨噬细胞刺激成骨细胞后,成骨细胞中Runx2和Ocn表达水平明显减少。M2型巨噬细胞刺激后,成骨细胞中Runx2和Ocn表达水平下调为0.45、0.31,M 1型巨噬细胞下调更明显,下调为0.11、0.05。见图3。
3讨论
牙周炎的治疗目标是消除炎症,恢复牙周组织的健康与功能。临床治疗中多使用局部或全身抗菌药物,控制感染,以减轻炎症反应[6-8]。巨噬细胞在牙周炎的进展中扮演着关键角色,巨噬细胞可分为M 1型和M2型,分别具有促炎和抗炎功能[9-10]。M 1型巨噬细胞可激活持续的炎症反应,而M2型巨噬细胞则清除炎症并修复组织,二者的动态平衡与牙周炎的进展密切关联。本研究建立了牙周炎动物实验模型,采集牙周炎动物模型组织标本进行组织学染色,可观察到牙槽骨存在严重破坏,排列情况紊乱,骨量明显减少。经免疫组化,可观察到牙槽骨吸收明显,骨吸收表面可见大量巨噬细胞浸润,骨吸收周缘M1和M2型巨噬细胞浸润。经蛋白质印迹法检测发现,巨噬细胞上清刺激成骨细胞后,成骨细胞中Runx2和Ocn表达减少。M 1型巨噬细胞被激活后,会大量分泌促炎细胞因子。这些因子不仅直接损伤牙周膜成纤维细胞和成骨细胞,还能募集例如中性粒细胞等更多的炎症细胞至病变部位,进而形成恶性循环,持续放大炎症反应,M 1型巨噬细胞通过分泌TNF-α、白细胞介素1β、IL-6等促炎因子,激活核因子κB(nuclear factor-κB,NF-κB)等通路,发挥出促进炎症反应的作用[11-12]。M 1型巨噬细胞还可以通过表达RANKL,激活RANK/RANKL/OPG信号通路,引起骨破坏。M2型巨噬细胞的作用机制与M1型巨噬细胞存在一定的差异,M2型巨噬细胞可以分泌抗炎因子,在缓解人体炎症反应方面具有一定的作用,通过分泌OPG等分子,进而对破骨细胞产生积极的影响,对其分化以及活化过程均产生明显的抑制,最终达到促进骨形成的效果。NF-κB信号通路与上述两种巨噬细胞之间均存在一定的联系,通过对该通路的抑制,对M2型巨噬细胞的活化具有一定的促进作用。
综上所述,通过本研究发现,巨噬细胞与牙周炎骨破坏之间存在一定的关系,M 1和M2能抑制成骨细胞中Runx2和Ocn的表达,且M 1型起到的抑制作用更为明显。本研究为牙周炎治疗提供新思路,未来可积极研究开发靶向M 1型巨噬细胞的抑制剂(如NF-κB抑制剂)和M2型巨噬细胞的激动剂(如STAT6激动剂),以调控巨噬细胞的平衡。并应用一定的免疫调节剂以促进M2型巨噬细胞的活化,减轻炎症反应,促进组织修复。结合基础治疗、药物治疗和手术治疗,综合调控M1/M2型巨噬细胞的平衡,提高治疗效果。受研究时间限制,本研究对M1、M2型巨噬细胞在牙周炎骨破坏中的作用与具体机制未予以深入分析,未来需予以进一步深入研究。
[参考文献]
[1]付岚清,郝新宇,钱文博,等.基础治疗对重度牙周炎患者龈沟液内中性粒细胞胞外诱捕网形成的影响研究[J].华西口腔医学杂志,2025,43(1):46-52.
[2]李垚,刘帅,刘志芳.慢性牙周炎患者龈沟液菌群多样性及其与炎症因子水平的相关性[J].口腔医学研究,2025,41(9):788-794.
[3]李*远.载二氢卟吩e6纳米粒介导光动力疗法诱导巨噬细胞凋亡治疗牙周炎的基础实验研究[J].应用激光,2025,45(7):188-196.
[4]苑舒月,刘春艳,刘冰等.巨噬细胞的极化与牙周炎[J].中国组织工程研究,2023,27(17):2699-2707.
[5]冯梅婷,鲁嘉韦,罗礼君,等.基于转录组学分析ADORA3在牙周炎中的表达及调控[J].口腔医学研究,2023,39(7):613-618.
[6]李涛,曲晓东,黎松龄,等.M 1型、M2型巨噬细胞极化相关因子在重度慢性牙周炎患者牙龈组织中的表达及其临床意义[J].中国现代医学杂志,2023,33(4):11-16.
[7]张娟,刘依萍,曹士盛,等.应用拉曼光谱技术对伴2型糖尿病慢性牙周炎患者龈下菌斑的研究[J].中国医科大学学报,2023,52(12):1113-1118.
[8]杨靖梅,周子亮,吴亚菲,等.基于网络药理学和分子对接技术探究姜黄素治疗牙周炎的作用机制[J].华西口腔医学杂志,2023,41(2):157-164.
[9]刘学忠,詹学国,刘家畅.牙龈组织中巨噬细胞M 1/M2极化相关因子的表达对重度慢性牙周炎患者的临床意义[J].宁夏医学杂志,2024,46(8):680-683.
[10]籍辰,张文娟,关宁,等.M 1型巨噬细胞对慢性牙周炎模型小鼠免疫状态的影响[J].吉林大学学报(医学版),2020,46(6):1137-1142,后插2.
[11]张洁,田艾.M2巨噬细胞参与骨再生相关信号通路的作用与机制[J].中国组织工程研究,2023,27(2):314-321.
[12]朱天啸,解杨,王嘉,等.棕榈酸在炎性因素下巨噬细胞M 1极化进程中的作用[J].实用口腔医学杂志,2023,39(3):300-306.










