多发性骨髓瘤患者应用含硼替佐米的联合化疗方案后治疗无反应的影响因素论文
2026-03-18 15:53:17 来源: 作者:xuling
摘要:LMR≥2.60、IL-32≥63.02 ng/L、HMGB1≥216.92 pg/mL均为MM患者应用含硼替佐米的联合化疗方案后治疗无反应的危险因素。
【摘要】目的:分析多发性骨髓瘤(MM)患者应用含硼替佐米的联合化疗方案后治疗无反应的影响因素。方法:回顾性分析2021年9月至2024年9月该院收治的185例MM患者的临床资料。收集患者一般资料,并检测实验室指标,根据应用含硼替佐米的联合化疗方案后治疗反应情况将其分为治疗有反应组和治疗无反应组,采用Logistic回归分析MM患者应用含硼替佐米的联合化疗方案后治疗无反应的影响因素。结果:185例MM患者应用含硼替佐米的联合化疗方案后治疗无反应38例,发生率为20.54%;两组性别、年龄、体质量指数、M蛋白类型、血红蛋白、白蛋白、β2-微球蛋白、血小板计数、乳酸脱氢酶占比比较,差异均无统计学意义(P>0.05);治疗无反应组国际分期系统(ISS)分期为Ⅲ期、淋巴细胞与单核细胞比值(LMR)≥2.60、白细胞介素-32(IL-32)≥63.02 ng/L、高迁移率族蛋白B1(HMGB1)≥216.92 pg/mL占比均高于治疗有反应组,差异有统计学意义(P<0.05);Logistic回归分析结果显示,LMR≥2.60、IL-32≥63.02 ng/L、HMGB1≥216.92 pg/mL均为MM患者应用含硼替佐米的联合化疗方案后治疗无反应的危险因素(OR>1,P<0.05)。结论:LMR≥2.60、IL-32≥63.02 ng/L、HMGB1≥216.92 pg/mL均为MM患者应用含硼替佐米的联合化疗方案后治疗无反应的危险因素。
【关键词】多发性骨髓瘤;硼替佐米;化疗;治疗无反应;影响因素
多发性骨髓瘤(MM)主要以血钙升高、肾功能不全、贫血、骨痛为典型症状[1]。硼替佐米是治疗MM的一线化疗药物,可延长患者无进展生存期[2],但由于MM的恶性程度较高,且具有高度异质性,常导致原发性或继发性耐药,20%~30%的患者出现早期治疗无反应[3]。因此早期识别治疗反应不佳的高危患者,并优化治疗策略,对改善患者预后至关重要。本文分析MM患者应用含硼替佐米的联合化疗方案后治疗无反应的影响因素。
1资料与方法
1.1一般资料回顾性分析2021年9月至2024年9月185例本院收治的185例MM患者的临床资料。纳入标准:符合MM诊断标准[4];首诊首治;完成硼替佐米+地塞米松+来那度胺化疗4个疗程;临床资料完整。排除标准:合并胰腺癌、乳腺癌、胃癌等其他恶性肿瘤;合并肝、肾功能不全;有化疗、放疗史;有免疫抑制剂、激素等药物长期使用史;合并浆细胞白血病及高钙血症。
1.2方法
1.2.1一般资料收集查阅医院电子病历系统,收集患者性别、年龄(≥60岁、<60岁)、体质量指数(BMI)(≥24 kg/m2,<24 kg/m2)、国际分期系统(ISS)分期(Ⅰ期、Ⅱ期、Ⅲ期)、M蛋白类型[免疫球蛋白(Ig)G型、IgA型、IgD型、轻链型]。
1.2.2实验室指标检测采集患者清晨空腹外周静脉血5 mL,取其中2 mL采用全自动血液分析仪检测血红蛋白(Hb)、血小板计数(PLT)、淋巴细胞与单核细胞比值(LMR);取剩余3 mL,以3000 r/min,离心半径10 cm,离心10 min,取上层血清,采用免疫比浊法检测白蛋白(ALB)水平,采用速率法检测乳酸脱氢酶(LDH)水平,采用电化学发光免疫分析法检测β2-微球蛋白(β2-MG)水平,采用酶联免疫吸附试验检测白细胞介素-32(IL-32)、高迁移率族蛋白B1(HMGB1)水平。
1.2.3治疗反应判定[4]严格完全缓解(sCR):满足完全缓解(CR)的基础上,血清游离轻链比值正常,骨髓中无克隆性浆细胞;CR:血清/尿免疫固定电泳均呈阴性,浆细胞瘤消失,骨髓中浆细胞比例<5%;非常好的部分缓解(VGPR):血清蛋白电泳检测不到M蛋白或M蛋白降低≥90%,且尿M蛋白<100 mg/24 h;部分缓解(PR):血清M蛋白减少≥50%,24 h尿M蛋白减少≥90%或降至<200 mg/24 h,无新骨质病变;疾病稳定(SD):不符合上述标准,但也未达到疾病进展(PD)标准;PD:血清M蛋白或尿M蛋白增加≥25%,出现新病变,循环浆细胞增加≥50%。将sCR、CR、VGPR、PR纳入治疗有反应,将SD、PD纳入治疗无反应。
1.3观察指标(1)统计MM患者应用含硼替佐米的联合化疗方案后治疗反应情况,将其分为治疗有反应组和治疗无反应组。(2)MM患者应用含硼替佐米的联合化疗方案后治疗无反应的单因素分析。(3)MM患者应用含硼替佐米的联合化疗方案后治疗无反应的Logistic回归分析。
1.4统计学处理采用SPSS 25.0统计学软件处理数据,计量资料以(x—±s)表示,采用t检验,计数资料以率(%)表示,采用χ2检验,多因素分析采用Logistic回归分析,以P<0.05为差异有统计学意义。
2结果
2.1 MM患者应用含硼替佐米的联合化疗方案后治疗反应情况185例MM患者应用含硼替佐米的联合化疗方案后治疗无反应38例,发生率为20.54%;治疗有反应147例。
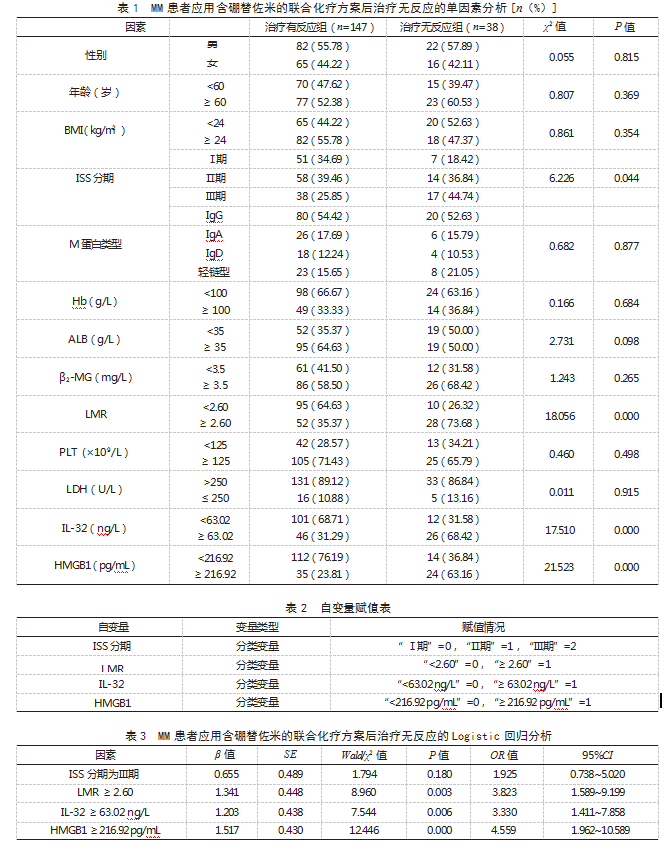
2.2 MM患者应用含硼替佐米的联合化疗方案后治疗无反应的单因素分析两组性别、年龄、BMI、M蛋白类型、Hb、ALB、β2-MG、PLT、LDH占比比较,差异均无统计学意义(P>0.05);治疗无反应组ISS分期为Ⅲ期、LMR≥2.60、IL-32≥63.02 ng/L、HMGB1≥216.92 pg/mL占比均高于治疗有反应组,差异有统计学意义(P<0.05)。见表1。
2.3 MM患者应用含硼替佐米的联合化疗方案后治疗无反应的Logistic回归分析将MM患者应用含硼替佐米的联合化疗方案后治疗反应情况作为因变量(治疗无反应=1,治疗有反应=0),将表1中P<0.05的因素作为自变量,赋值见表2。Logistic回归分析结果显示,LMR≥2.60、IL-32≥63.02 ng/L、HMGB1≥216.92 pg/mL均为MM患者应用含硼替佐米的联合化疗方案后治疗无反应的危险因素(OR>1,P<0.05)。见表3。
3讨论
含硼替佐米的联合化疗方案是治疗MM患者的常用方法,可抑制肿瘤细胞血管生成,限制肿瘤细胞生长和扩散[5-6]。但MM患者体内因存在异质性癌细胞群,可导致治疗反应存在差异。
本研究结果显示,185例MM患者应用含硼替佐米的联合化疗方案后治疗无反应38例,发生率为20.54%。提示MM患者应用含硼替佐米的联合化疗方案后治疗无反应的情况较多。
本研究Logistic回归分析结果显示,LMR≥2.60、IL-32≥63.02 ng/L、HMGB1≥216.92 pg/mL均为MM患者应用含硼替佐米的联合化疗方案后治疗无反应的危险因素。分析原因:(1)LMR≥2.60。单核细胞在肿瘤微环境中可为MM细胞提供营养成分,并可抑制免疫反应,造成MM细胞逃逸,进而降低患者对硼替佐米治疗的反应性[7-8]。此外,单核细胞在肿瘤微环境中可极化为具有免疫抑制功能的M2样肿瘤相关巨噬细胞,并通过分泌抑制性细胞因子,诱导T细胞功能衰竭,进而削弱硼替佐米诱导的肿瘤细胞清除效果[9]。而淋巴细胞是抗肿瘤免疫和化疗药物(包括硼替佐米)发挥细胞毒性作用的关键执行者,其水平降低可削弱免疫监视功能,限制硼替佐米的抗肿瘤免疫效力。因此,LMR可综合反映淋巴细胞与单核细胞的变化,其水平升高不仅促进MM恶性进展,还可直接抑制效应免疫细胞的功能,降低MM细胞对硼替佐米的敏感性,导致治疗无反应。(2)IL-32≥63.02 ng/L。IL-32主要在活化的T细胞和自然杀伤细胞中产生,可促进炎症反应发生,同时可影响自然杀伤细胞功能和树突状细胞的成熟[10]。IL-32水平升高可使核因子κB水平升高,而核因子κB高表达的转录产物又可诱导IL-32表达,从而建立持续的高炎症和强生存信号状态,以增强肿瘤细胞的耐药性[11],进而导致MM患者早期治疗无反应[12]。同时IL-32水平升高还可使硼替佐米与高表达的热休克蛋白结合,增强机体的耐药性,进一步导致治疗无反应[13]。(3)HMGB1≥216.92 pg/mL。HMGB1是一种非组蛋白DNA结合蛋白,可在细胞内参与DNA复制、重组、转录和修复,参与多种生理和病理过程[14]。HMGB1主要通过激活Janus激酶/信号转导与转录激活因子通路,促进MM细胞增殖,同时可与细胞表面的糖基化终产物受体结合,促进MM细胞的生长和转移[15]。同时,HMGB1水平升高可激活磷脂酰肌醇3激酶-Ⅲ复合物,驱动自噬体形成,而被激活的自噬体可清除由硼替佐米累积的毒性蛋白聚集体,缓解内质网应激,进而帮助MM细胞逃逸,导致治疗无反应[16]。此外,HMGB1还可识别并结合DNA损伤位点,通过增强DNA修复能力,使肿瘤细胞存活于化疗药物造成的基因组不稳定性环境中[17],进而增加MM患者治疗无反应发生风险。
综上所述,LMR≥2.60、IL-32≥63.02 ng/L、HMGB1≥216.92 pg/mL均为MM患者应用含硼替佐米的联合化疗方案后治疗无反应的危险因素。
参考文献
[1]邓晶晶,王桐桐,陈文明.多发性骨髓瘤诊疗进展[J].中华内科杂志,2024,63(2):209-212.
[2]李建梅,晋艳玲.硼替佐米、来那度胺结合地塞米松治疗多发性骨髓瘤的有效率及安全性[J].昆明医科大学学报,2023,44(6):120-125.
[3]陈慧玲,马成成,柴晔,等.基于硼替佐米治疗反应及BTK表达水平建立非初治多发性骨髓瘤临床预测模型[J].中国实验血液学杂志,2022,30(4):1139-1143.
[4]中国医师协会血液科医师分会,中华医学会血液学分会,中国医师协会多发性骨髓瘤专业委员会.中国多发性骨髓瘤诊治指南(2020年修订)[J].中华内科杂志,2020,59(5):341-346.
[5]毛沛沛,杨琛.硼替佐米联合地塞米松、来那度胺化疗方案治疗多发性骨髓瘤的疗效和安全性评价[J].实用癌症杂志,2023,38(3):502-506.
[6]曹慧,黄来全,汪琼,等.来那度胺联合硼替佐米、地塞米松治疗多发性骨髓瘤的效果及对免疫功能的影响研究[J].中国医药导报,2024,21(8):119-122.
[7]陈小双,高正杰,高攀科,等.LMR、PNI与多发性骨髓瘤患者化疗反应及预后的关系[J].中华全科医学,2023,21(12):2022-2026.
[8]王豪言,孙晓白,李梦一,等.多发性骨髓瘤患者首次治疗部分缓解时NLR、MLR与预后的关系[J].山东医药,2023,63(8):1-5.
[9]CHEN S,WANG M,LU T,et al.JMJD6 in tumor-associated macrophage regulates macrophage polarization and cancer progression via STAT3/IL-10 axis[J].Oncogene,2023,42(37):2737-2750.
[10]沈佳坤,郑林,董慧娟,等.多发性骨髓瘤患者血清IL-32、IL-37、sIL-2R水平及临床意义[J].实用中西医结合临床,2024,24(13):92-95.
[11]ZHAO H,WU L,YAN G,et al.Inflammation and tumor progression:signaling pathways and targeted intervention[J].Signal Transduct Target Ther,2021,6(1):263.
[12]温少瑾,杨焕莹,孙凤歧,等.NF-κB信号通路与多发性骨髓瘤发病机制的相关性及靶向治疗作用的研究进展[J].西部中医药,2024,37(7):97-102.
[13]苗玉迪,胡星星,李艳春,等.血清IL-17、IL-32、IL-33、IL-37联合检测对初治多发性骨髓瘤患者早期治疗反应性的预测价值[J].现代生物医学进展,2022,22(22):4279-4284.
[14]王娟,曾爱明,梁树芬.血清HMGB1、sRAGE在初诊多发性骨髓瘤的诊断、疗效监测及预后中的价值[J].中国实验血液学杂志,2022,30(2):493-500.
[15]田颖,王根杰,胡青竹,等.血清高迁移率族蛋白B1、β2-微球蛋白、乳酸脱氢酶及白细胞介素-6在多发性骨髓瘤中的表达及相关性[J].癌症进展,2023,21(22):2529-2532.
[16]YANG B,LI G,WANG S,et al.Tumor-associated macrophages/C-X-C motif chemokine ligand 1 promotes breast cancer autophagy-mediated chemoresistance via IGF1R/STAT3/HMGB1 signaling[J].Cell Death Dis,2024,15(10):743.
[17]DANGERFIELD J,MUKHERJEE A,REH W,et al.High-Mobility Group Box Protein 3(HMGB3)Facilitates DNA interstrand crosslink processing and double-strand break repair in human cells[J].Genes(Basel),2025,16(9):1044.










