动态增强磁共振成像联合弥散加权成像检查诊断乳腺癌的效能论文
2026-03-04 14:55:19 来源: 作者:xuling
摘要:经Spearman相关性分析结果显示,Kep、Ktrans、Ve水平与乳腺癌分化程度均呈负相关(r<0,P<0.05),ADC值与乳腺癌分化程度呈正相关(r>0,P<0.05)。结论:DCE-MRI联合DWI检查诊断乳腺癌的效能高于二者单项检查。
【摘要】目的:观察动态增强磁共振成像(DCE-MRI)联合弥散加权成像(DWI)检查诊断乳腺癌的效能。方法:选取2021年3月至2024年1月该院收治的168例疑似乳腺癌患者进行前瞻性研究,以病理活检结果为金标准,统计病理检查结果,比较DCE-MRI、DWI单项及联合检查诊断乳腺癌的效能,比较不同分化程度乳腺癌患者DCE-MRI定量参数[速率常数(Kep)、容量转移常数(Ktrans)、血管外细胞外间隙容积比(Ve)]、DWI参数[表观扩散系数(ADC)]水平,分析DCE-MRI定量参数水平、DWI参数水平与乳腺癌分化程度的相关性。结果:以病理活检结果为金标准,168例疑似乳腺癌患者中阳性84例,其中低分化17例,中分化37例,高分化30例;阴性84例。DCE-MRI检查结果显示,阳性71例,阴性97例;DWI检查结果显示,阳性71例,阴性97例;联合检查结果显示,阳性83例,阴性85例。DCE-MRI、DWI联合检查诊断乳腺癌的灵敏度、阴性预测值均高于二者单项检查,漏诊率低于二者单项检查,DCE-MRI、DWI联合检查诊断乳腺癌的准确度高于DCE-MRI检查,差异有统计学意义(P<0.05)。高分化患者Kep、Ktrans、Ve水平均低于中、低分化患者,且中分化患者低于低分化患者,高分化患者ADC值均高于中、低分化患者,且中分化高于低分化患者,差异有统计学意义(P<0.05)。经Spearman相关性分析结果显示,Kep、Ktrans、Ve水平与乳腺癌分化程度均呈负相关(r<0,P<0.05),ADC值与乳腺癌分化程度呈正相关(r>0,P<0.05)。结论:DCE-MRI联合DWI检查诊断乳腺癌的效能高于二者单项检查。
【关键词】动态增强磁共振成像;弥散加权成像;检查;乳腺癌;诊断
乳腺癌是临床常见恶性肿瘤,乳腺上皮过度增殖是引发乳腺癌的主要病理机制[1-2],及早明确诊断并积极干预,对改善乳腺癌患者的预后极为重要[3]。病理活检具有较高的诊断准确性,但其存在创伤性,临床应用存在局限性。动态增强磁共振成像(DCE-MRI)检查可准确反映病灶血流动力学特点,观察病变部位微循环病理变化,具有无创、灵敏度高等优势[4-5]。弥散加权成像(DWI)检查可通过检测人体组织内水分子扩散运动观察乳腺组织微观结构变化[6]。本文观察DCE-MRI联合DWI检查诊断乳腺癌的效能。
1资料与方法
1.1一般资料选取2021年3月至2024年1月本院收治的168例疑似乳腺癌患者进行横断面研究。纳入标准:因乳腺肿块就诊,伴有局部疼痛或乳头溢液,部分患者存在乳头内陷、橘皮征;首次就诊;依从性好,检查配合度高;女性。排除标准:存在其他恶性肿瘤;哺乳或妊娠期;存在自身免疫性疾病;存在语言障碍、精神疾病,无法正常沟通。其中年龄23~67岁,平均(45.06±10.89)岁;体质量47~75 kg,平均(60.59±6.42)kg。
1.2方法嘱患者保持俯卧位,双乳自然下垂,测量时抑制脂肪信号,以减少伪影。使用Skyra 3.0T磁共振系统(德国西门子),于患者入院后行DCE-MRI及DWI检查,选取乳腺专用线圈。
DCE-MRI检查:先行MRI平扫,参数设置:层厚4 mm,层间距0.4 mm,视野(FOV)340,矩阵358×448,激发次数2次,重复时间(TR)、回波时间(TE)分别为3580 ms、70 ms,层数29。而后行增强扫描,参数设置:层厚1 mm,层间距0.1 mm,激发次数1次,FOV 340,TR、TE分别为4.49 ms、1.68 ms;应用乳腺容积成像序列行增强扫描,在出现蒙片后,于手背静脉处注射Gd-DTPA对比剂(0.2 mmol/kg),速率2.5 mL/s,并行3D动态增强扫描。避开出血、钙化、坏死区域,于病灶实质区选择感兴趣区(ROI),通过Mean Cure绘制时间-信号强度曲线(TIC)。
DWI检查:单次激发自旋回波,SE-EPI序列参数:层厚4 mm,层间距0.4 mm,TR、TE分别为4800 ms、65 ms,矩阵220×96,FOV 340,层数为24,激发次数4次,获取表观扩散系数(ADC)等数据,并于ADC图上手动勾画ROI区,测量3次取均值。
图像后处理:上传原始数据及图像至工作站并构建伪彩图,由2名5年以上经验影像学医师分别判读结果,对有争议病例,需协商后给出一致结论。DCE-MRI、DWI联合检查中任意一种诊断为阳性则为阳性。
1.3观察指标(1)以病理活检结果为金标准,统计病理检查结果。(2)比较DCE-MRI、DWI单项及联合检查诊断乳腺癌的效能。(3)比较不同分化程度乳腺癌患者DCE-MRI定量参数[速率常数(Kep)、容量转移常数(Ktrans)、血管外细胞外间隙容积比(Ve)]及DWI参数水平。(4)分析DCE-MRI定量参数、DWI参数水平与乳腺癌分化程度的相关性。
1.4统计学方法应用SPSS 21.0软件进行统计学分析,计量资料以(x±s)表示,两组间比较采用t检验,多组间比较采用单因素方差分析,计数资料以率(%)表示,采用χ2检验,采用Spearman相关性分析,以P<0.05为差异有统计学意义。
2结果
2.1病理检查结果以病理活检结果为金标准,168例疑似乳腺癌患者中阳性84例,其中低分化17例,中分化37例,高分化30例;阴性84例。
2.2 DCE-MRI、DWI单项及联合检查诊断乳腺癌的结果DCE-MRI检查结果显示,阳性71例,阴性97例;DWI检查结果显示,阳性71例,阴性97例;联合检查结果显示,阳性83例,阴性85例。见表1。
2.3 DCE-MRI、DWI单项及联合检查诊断乳腺癌的效能比较DCE-MRI、DWI联合检查诊断乳腺癌的灵敏度、阴性预测值均高于二者单项检查,漏诊率低于二者单项检查,DCE-MRI、DWI联合检查诊断乳腺癌的准确度高于DCE-MRI检查,差异有统计学意义(P<0.05)。见表2。
2.4不同分化程度乳腺癌患者DCE-MRI定量参数、DWI参数水平比较高分化患者Kep、Ktrans、Ve水平均低于中、低分化患者,且中分化患者低于低分化患者,高分化患者ADC值均高于中、低分化患者,且中分化高于低分化患者,差异有统计学意义(P<0.05)。见表3。
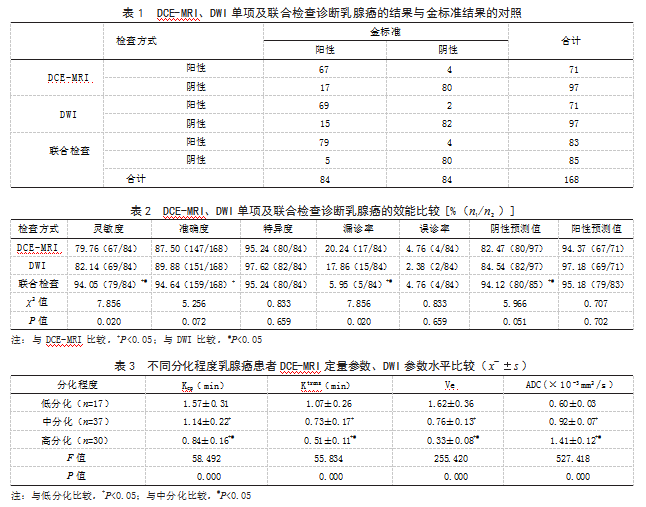
2.5 DCE-MRI定量参数、DWI参数水平与乳腺癌分化程度的相关性经Spearman相关性分析结果显示,Kep、Ktrans、Ve水平与乳腺癌分化程度均呈负相关(r<0,P<0.05),ADC值与乳腺癌分化程度呈正相关(r>0,P<0.05)。见表4。
3讨论
乳腺癌临床表现常为无痛性的肿块,病灶多不规则[7]。DCE-MRI检查可根据乳腺肿块形态及组织内毛细血管的血流动力学特征评估恶性程度[8-9]。DWI检查属无创检查方式中的一种,可准确描述目标组织、器官的微观解剖结构[10]。
本研究结果显示,DCE-MRI、DWI联合检查诊断乳腺癌的灵敏度、阴性预测值均高于二者单项检查,漏诊率低于二者单项检查,DCE-MRI、DWI联合检查诊断乳腺癌的准确度高于DCE-MRI检查。分析原因为乳腺癌癌细胞增殖能力较强,代谢异常旺盛导致细胞核扩大、细胞密度增大、细胞外间隙减小,对水分子活动产生一定限制,DWI检查则多表现为ADC低信号、病灶周围皮肤增厚水肿及病灶侧血管增多增粗,但DWI对细微的病灶结构无法清晰显示,且空间分辨率不高、磁场要求较高[11-12]。DCE-MRI检查中Kep为造影剂交换率,该数值随着对比剂通过速度加快而增大;Ktrans可将乳腺癌局部微血管渗透状况及血流清晰显示;Ve与细胞环境活跃程度密切相关,可反映肿瘤血管外细胞容积。乳腺癌由于新生毛细血管增多,血管密度增加,通透性异常改变,血管外肿瘤细胞间隙增加,从而导致Kep、Ktrans、Ve水平异常升高[13-14]。DCE-MRI、DWI联合检查二者相互协同作用,从而提高诊断效能。
本研究结果同时显示,高分化患者Kep、Ktrans、Ve水平均低于中、低分化患者,且中分化患者低于低分化患者,高分化患者ADC值均高于中、低分化患者,且中分化高于低分化患者,经Spearman相关性分析结果显示,Kep、Ktrans、Ve水平与乳腺癌分化程度均呈负相关,ADC值与乳腺癌分化程度呈正相关。分析原因为乳腺癌肿瘤细胞分化程度越低则恶性程度越高,其肿瘤组织血管密度不断增加,促使毛细血管数量增加,导致微循环血容量增大、流速加快,故而Kep、Ktrans、Ve水平升高[15-16]。同时乳腺癌肿瘤细胞间隙则会变窄,导致水分子扩散运动受限程度增加,故而ADC值越低[17]。
综上所述,DCE-MRI联合DWI检查诊断乳腺癌的效能高于二者单项检查。
参考文献
[1]雷少元,郑荣寿,张思维,等.乳腺癌发病率和死亡率的全球模式:一项基于人群的2000-2020年肿瘤登记数据分析研究[J].癌症,2022,41(7):324-335.
[2]李佳圆.中国乳腺癌危险因素研究现况及其风险预测模型研究展望[J].中国循证医学杂志,2020,20(7):745-748.
[3]乔俊娅,温生宝.r-fov IVIM与r-fov DWI模型参数早期预测乳腺癌新辅助化疗疗效价值的比较[J].中国CT和MRI杂志,2024,22(3):89-92.
[4]陈志远,庞艺.MRI动态增强扫描联合弥散加权成像在乳腺良恶性病变鉴别诊断中的应用分析[J].影像研究与医学应用,2023,7(5):101-103.
[5]李美芹,刘莹,赵凡,等.IVIM-DWI联合DCE-MRI对乳腺癌Nottingham指数的预测价值[J].放射学实践,2023,38(12):1548-1553.
[6]付子文,杨华.MRI增强扫描联合DWI检测在乳腺癌诊断中的应用[J].影像科学与光化学,2020,38(3):540-545.
[7]李健斌,江泽飞.2021年中国临床肿瘤学会乳腺癌诊疗指南更新要点解读[J].中华医学杂志,2021,101(24):1835-1838.
[8]马国津,李佳晶,崔金利.乳腺癌DCE-MRI与超声、钼靶X线的对比研究及诊断价值分析[J].影像科学与光化学,2024,42(6):669-676.
[9]钱振,张金平,汤永祥,等.DCE-MRI与超声和钼靶X线在乳腺癌诊断价值对比[J].现代科学仪器,2024,41(5):227-231.
[10]何瑞红,李立,钱伟军.DCE-MRI、多b值DWI结合CA153、CEA对乳腺癌及肿块型浆细胞性乳腺炎的鉴别诊断价值研究[J].中国CT和MRI杂志,2023,21(6):89-92.
[11]武兵,朱慧,沙德厚,等.DWI联合血清糖类抗原153、125及癌胚抗原诊断乳腺癌的价值研究[J].医学影像学杂志,2021,31(8):1326-1329.
[12]张林波,吴静,高洁,等.DCE-MRI、T2WI及DWI联合诊断乳腺癌的价值观察[J].中国CT和MRI杂志,2024,22(5):106-108.
[13]王洁,唐文伟,田忠甫,等.乳腺癌DCE-MRI参数及ADC与病理分子预后标记物的相关性分析[J].磁共振成像,2021,12(3):76-79.
[14]杨林巧.动态增强磁共振成像定量参数应用于乳腺癌早期诊断及病情评估中的价值研究[J].影像研究与医学应用,2024,8(12):70-72.
[15]崔䶮,刘永波,曹钢.DCE-MRI时间-信号曲线联合扩散加权成像技术在乳腺癌不同分期评估中的价值[J].中国CT和MRI杂志,2023,21(4):91-93.
[16]刘文霞,贡琦,刘利,等.DCE-MRI直方图定量参数联合DWI在乳腺癌早期诊断中的应用价值[J].中国CT和MRI杂志,2025,23(1):106-108.
[17]龚俊峰,李晓燕,王永杰.对比增强能谱乳腺X线成像、MRI动态增强联合DWI评估不同乳腺癌分子分型的价值研究[J].磁共振成像,2020,11(12):1170-1173.










