脊髓损伤后神经干细胞迁移和分化的微环境调控机制及促进再生策略论文
2026-02-26 16:46:47 来源: 作者:xuling
摘要:脊髓损伤(spinal cord injury,SCI)是高负担神经系统创伤,全球发病率高,交通事故为主要病因。SCI病理生理含原发性机械损伤与继发性炎症、氧化应激等连锁反应;神经干细胞凭自我更新、多向分化等特性,通过替代受损细胞、分泌营养因子、调节免疫及促血管生成参与修复。
[摘要]脊髓损伤(spinal cord injury,SCI)是高负担神经系统创伤,全球发病率高,交通事故为主要病因。SCI病理生理含原发性机械损伤与继发性炎症、氧化应激等连锁反应;神经干细胞凭自我更新、多向分化等特性,通过替代受损细胞、分泌营养因子、调节免疫及促血管生成参与修复。脊髓损伤后微环境中,细胞外基质、细胞因子/生长因子、炎症因子(急慢性期呈促抑双重效应)通过信号通路调控神经干细胞迁移分化。目前神经干细胞治疗面临存活分化效率、来源安全性等问题,深入研究微环境调控机制与再生策略,对推动SCI治疗意义重大。
[关键词]脊髓损伤;神经干细胞;微环境调控;迁移分化;炎症反应;修复策略
脊髓损伤(spinal cord injury,SCI)是严重神经系统创伤,全球每年每百万人约15~40人患病,美国每年新增1.2万人、累计超28万人,中国因交通、建筑行业发展及人口老龄化,发病率亦上升[1]。其主要病因中,交通事故占比超50%,此外还有高处坠落、运动损伤、暴力等。神经干细胞具有自我更新、多向分化及低免疫原性特点,可通过对称或不对称分裂维持细胞量,在特定条件下分化为神经元、星形胶质细胞和少突胶质细胞,移植后能迁移至损伤部位替代受损细胞,还可旁分泌脑源性神经营养因子(brain-derived neurotrophic factor,BDNF)、神经生长因子(nerve growth factor,NGF)等调节微环境,为SCI治疗带来希望[2]。但目前神经干细胞在体内的存活率、分化效率,以及来源、移植方式、时机和长期安全性等问题仍待解决,深入研究其迁移分化的微环境调控机制与再生策略意义重大。
1 SCI的病理生理机制
SCI病理生理过程复杂,主要分为原发性损伤与继发性损伤两个阶段。原发性损伤为外力直接作用于脊髓所致的即刻损伤,常见于车祸、高处坠落、暴力撞击等场景,可引发脊柱骨折、脱位,骨折片刺入脊髓或脊髓受强烈震荡,导致脊髓组织瞬间遭受严重机械性破坏,神经元与神经纤维受损、神经传导通路中断,损伤平面以下运动、感觉及自主神经功能随即出现障碍[3]。继发性损伤在原发性损伤基础上发生,是一系列复杂病理生理变化引发的进一步损伤,可持续数小时至数周。原发性损伤后,神经元与神经胶质细胞膜完整性被破坏,细胞内离子稳态失衡,大量钙离子内流激活多种酶,引发细胞内级联反应,导致细胞代谢紊乱,最终细胞凋亡或坏死;同时神经胶质细胞损伤会削弱其对神经元的支持、营养与保护作用,加重神经元损伤[2,4-5]。炎症反应是继发性损伤的关键环节:损伤后损伤部位免疫细胞迅速活化,释放肿瘤坏死因子α(tumor necrosis factor-α,TNF-α)、白细胞介素1β(interleukin 1β,IL-1β)等炎性细胞因子,一方面吸引更多免疫细胞聚集,放大炎症反应,另一方面破坏血-脊髓屏障,增加血管通透性,引发脊髓组织水肿,压迫神经细胞加重功能损伤,还会促使一氧化氮等神经毒性物质释放,直接损伤神经元与神经纤维[5-7]。氧化应激同样是继发性损伤的重要因素:SCI后组织缺血缺氧,线粒体功能受损,产生大量活性氧(reactive oxygen species,ROS);ROS氧化活性极强,可攻击细胞膜脂质、蛋白质及核酸等生物大分子,引发脂质过氧化反应,破坏细胞膜结构与功能,导致细胞损伤死亡,还会激活细胞凋亡信号通路,促进神经元与神经胶质细胞凋亡,且其产生的自由基与炎性细胞因子相互作用,加剧炎症反应形成恶性循环,进一步加重SCI[4,7]。详细机制见图1。
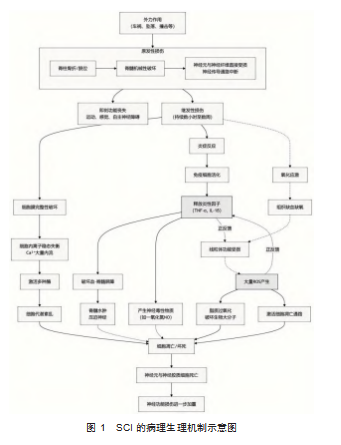
2神经干细胞在SCI修复中的作用机制
2.1替代受损细胞
SCI后,大量的神经元和神经胶质细胞受损或死亡,导致神经传导通路中断和神经功能障碍。神经干细胞具有多向分化潜能,在适宜的微环境中,能够分化为神经元、星形胶质细胞和少突胶质细胞,从而替代受损的细胞,填补组织缺损,重建神经环路。研究表明,将神经干细胞移植到SCI部位后,它们可以在局部微环境的诱导下,向神经元方向分化,并与周围的神经元建立突触连接,形成功能性的神经回路[8]。例如,在一些动物实验中,通过将标记的神经干细胞移植到SCI的大鼠模型中,发现这些干细胞能够成功分化为成熟的神经元,并在损伤部位存活和整合,部分恢复了脊髓的运动和感觉功能。这些分化而来的神经元不仅能够传递神经信号,还能对周围的神经组织起到支持和营养作用,促进神经功能的恢复。少突胶质细胞能够形成髓鞘,包裹神经元的轴突,提高神经信号的传导速度。在SCI后,少突胶质细胞受损,髓鞘脱失,导致神经传导功能障碍[7,9]。神经干细胞分化产生的少突胶质细胞可以重新形成髓鞘,修复受损的神经纤维,恢复神经传导功能。
2.2分泌细胞因子
神经干细胞具有旁分泌功能,能够分泌多种细胞因子和神经营养因子,这些生物活性物质在SCI修复中发挥着重要作用。神经干细胞可以分泌BDNF、NGF、胶质细胞源性神经营养因子(glial cell line-derived neurotrophic factor,GDNF)等神经营养因子。这些因子能够促进神经元的存活、生长和分化,增强轴突的再生能力,抑制神经元的凋亡。BDNF可以与神经元表面的受体结合,激活下游的信号通路,促进神经元的存活和轴突的生长;GDNF对多巴胺能神经元具有特异性的营养作用,能够促进其存活和分化,在SCI的治疗中,有助于保护和修复受损的神经细胞。神经干细胞还能分泌血管内皮生长因子(vascular endothelial growth factor,VEGF)、碱性成纤维细胞生长因子(basic fibroblast growth factor,bFGF)等促进血管生成的因子[10-11]。这些因子可以刺激血管内皮细胞的增殖和迁移,促进新生血管的形成,改善损伤部位的血液供应,为神经细胞提供充足的氧气和营养物质,有利于神经组织的修复和再生。在SCI后,局部组织缺血缺氧,血管生成不足,影响神经细胞的存活和功能恢复。神经干细胞分泌的血管生成因子能够促进血管新生,改善局部微循环,为神经再生创造良好的微环境[3,6]。
2.3调节免疫反应
SCI后,机体的免疫系统被激活,引发炎症反应。适度的炎症反应有助于清除损伤部位的坏死组织和病原体,但过度的炎症反应会导致神经细胞的进一步损伤,不利于SCI的修复。神经干细胞在调节免疫反应方面具有独特的作用。神经干细胞可以通过分泌抗炎性细胞因子,如转化生长因子β(transforming growth factor-β,TGF-β)、白细胞介素10(interleukin 10,IL-10)等,抑制炎症细胞的活化和炎性细胞因子的释放,减轻炎症反应对神经组织的损伤[12-13]。TGF-β能够抑制巨噬细胞和T淋巴细胞的活性,减少TNF-α、IL-1β等炎性细胞因子的分泌,从而降低炎症反应的强度;IL-10可以抑制单核细胞和巨噬细胞的功能,减少炎性介质的产生,发挥抗炎作用。神经干细胞还能调节免疫细胞的分化和功能,促进免疫细胞向抗炎表型转化。研究发现,神经干细胞可以诱导巨噬细胞从促炎的M 1型向抗炎的M2型转化,M2型巨噬细胞能够分泌抗炎性细胞因子,促进组织修复和再生[7]。此外,神经干细胞还可以通过与免疫细胞直接接触,调节免疫细胞的信号通路,抑制免疫细胞的过度活化,维持免疫微环境的平衡[14]。
2.4促进血管生成
血管生成对于SCI后的组织修复和功能恢复至关重要。充足的血液供应能够为损伤部位提供必要的氧气和营养物质,带走代谢废物,促进神经细胞的存活和再生。神经干细胞在促进血管生成方面发挥着积极的作用。神经干细胞可以分泌多种血管生成因子,如前文提到的VEGF、bFGF等。VEGF是一种特异性作用于血管内皮细胞的生长因子,它能够与血管内皮细胞表面的受体结合,激活下游的信号通路,促进血管内皮细胞的增殖、迁移和管腔形成,从而诱导新生血管的生成。bFGF也具有促进血管内皮细胞增殖和分化的作用,它可以刺激血管内皮细胞合成和分泌细胞外基质(extra-cellular matrix,ECM),为血管生成提供支持结构,同时还能促进血管平滑肌细胞的增殖和迁移,稳定新生血管[6-7]。除了分泌血管生成因子,神经干细胞还可以通过与血管内皮细胞相互作用,直接参与血管生成过程。研究表明,神经干细胞能够与血管内皮细胞形成紧密的联系,促进内皮细胞的聚集和排列,形成血管样结构[3]。神经干细胞还可以分泌ECM蛋白和黏附分子,为血管生成提供适宜的微环境,增强血管内皮细胞的黏附能力,促进血管的稳定和成熟[8-9]。
3 SCI后微环境对神经干细胞迁移和分化的调控机制
3.1微环境组成及对神经干细胞的影响因素
SCI后的微环境是由ECM、细胞因子、生长因子、炎症因子等构成的复杂动态系统,各成分相互作用共同影响神经干细胞的迁移和分化。其中,ECM作为重要组成部分,不仅为神经干细胞提供物理支撑,还通过与细胞表面受体作用传递化学信号,其含有的胶原蛋白、层粘连蛋白、纤连蛋白、蛋白聚糖等形成三维网络,为神经干细胞附着、迁移和分化奠定基础,且不同成分作用有差异,如层粘连蛋白可促进神经干细胞向神经元分化,纤连蛋白对其迁移至关重要;细胞因子和生长因子是调节神经干细胞增殖、分化、迁移和存活的关键小分子蛋白质,NGF、BDNF、GDNF等能促进神经干细胞向神经元分化并增强其存活与迁移能力,白细胞介素、干扰素等细胞因子则通过调节炎症反应间接影响神经干细胞,且各类细胞因子与生长因子间存在协同或拮抗作用;炎症因子也是微环境重要成分,SCI后免疫系统激活使炎症细胞大量浸润并释放TNF-α、IL-1β等,损伤早期适量炎症因子可促进神经干细胞增殖迁移以助修复,后期过度炎症反应则会产生神经毒性、抑制分化甚至诱导凋亡,还能通过调节细胞因子和生长因子的表达活性间接影响神经干细胞,此外,微环境中的酸碱度、氧化还原状态、细胞间相互作用等因素,也会对神经干细胞的迁移和分化产生影响[6-9]。
3.2 ECM与神经干细胞的相互作用
ECM是由多种蛋白质和糖类构成的复杂网络结构,在SCI后的微环境中,既为神经干细胞提供物理支撑,又能通过与神经干细胞表面整合素受体相互作用,激活细胞内信号传导通路,进而调控神经干细胞的迁移和分化。其主要成分包括胶原蛋白、层粘连蛋白、纤连蛋白等:胶原蛋白含量最丰富,凭借高稳定性和机械强度为神经干细胞提供坚实支撑;层粘连蛋白可与神经干细胞表面整合素α6β1受体结合,激活丝裂原活化蛋白激酶(mitogen-activated protein kinase,MAPK)信号通路,促进其向神经元分化;纤连蛋白能与整合素α5β1受体结合,参与细胞黏附、迁移和增殖过程,调节神经干细胞迁移行为[5,7]。当整合素受体与ECM相应配体结合后,会引发构象变化,激活粘着斑激酶、磷脂酰肌醇-3激酶(phosphatidylinositol-3 kinase,PI3K)等信号分子,进一步激活MAPK、PI3K-Akt等下游通路——MAPK通路中激活的MAPK可磷酸化Elk-1、c-Jun等转录因子,调控相关基因表达,PI3K-Akt通路则能促进神经干细胞存活、增殖并调节其迁移分化。在SCI修复研究中,向损伤部位植入含特定ECM成分的生物材料可营造有利微环境,如将含层粘连蛋白的水凝胶植入SCI大鼠模型,能显著增强神经干细胞迁移分化能力、改善修复效果,这表明合理调控ECM与神经干细胞的相互作用,有望成为SCI治疗的新策略[11-12]。
3.3细胞因子和生长因子的信号传导通路
SCI后,微环境中的细胞因子和生长因子通过与神经干细胞表面特异性受体结合,激活复杂信号传导通路,精细调控神经干细胞的迁移、分化、增殖与存活。其中,NGF与酪氨酸激酶受体A结合,引发酪氨酸激酶受体A二聚化与自身磷酸化,招募生长因子受体结合蛋白2和鸟苷酸交换因子激活小G蛋白Ras,进而激活MAPK通路(含细胞外信号调节激酶、c-Jun氨基末端激酶、p38 MAPK),磷酸化Elk-1、c-Jun等转录因子调节相关基因表达,同时还能激活PI3K-Akt通路,促进神经干细胞存活、迁移并向神经元分化以重建神经传导通路[6-8]。BDNF与酪氨酸激酶受体B结合后,同样促使酪氨酸激酶受体B二聚化与自身磷酸化,激活MAPK、PI3K-Akt及磷脂酶Cγ通路,分别实现促存活分化、抑凋亡促增殖迁移、调节细胞内钙离子浓度影响分化迁移的作用,外源性给予BDNF可显著改善SCI神经功能。此外,GDNF结合相关受体激活通路促神经干细胞向多巴胺能神经元分化,bFGF和表皮生长因子结合受体激活通路维持神经干细胞干性并促增殖,这些因子间还存在协同或拮抗作用,共同维持微环境平衡与神经干细胞正常功能[11-13]。
3.4炎症反应对神经干细胞迁移和分化的双重效应
SCI后,炎症反应作为机体自然防御反应,对神经干细胞迁移和分化呈急性促、慢性抑的双重效应,且两阶段差异显著。急性炎症期(损伤后数小时至数天内),免疫细胞快速浸润并释放TNF-α、IL-1β、白细胞介素6等炎性细胞因子:TNF-α上调神经干细胞表面趋化因子受体,增强其对趋化因子的敏感性以促进向损伤部位迁移;IL-1β通过激活MAPK信号通路,推动神经干细胞向神经元分化,同时炎症反应还能清除坏死组织与病原体,为神经干细胞营造清洁微环境。而在慢性炎症期(损伤后数天至数周及更久),持续炎症形成神经毒性微环境:高水平TNF-α、IL-1β抑制神经干细胞增殖分化,阻碍其向神经元和少突胶质细胞分化,还诱导其表达Bax等促凋亡蛋白以增加凋亡率;一氧化氮等神经毒性物质损伤神经干细胞功能,且慢性炎症会促使胶质瘢痕形成,瘢痕中星形胶质细胞分泌的硫酸软骨素蛋白聚糖等抑制性分子,进一步阻碍神经干细胞迁移,使其难以抵达损伤部位发挥修复作用[12-14]。
4结语
综上所述,SCI作为高负担神经系统创伤,其病理生理进程涵盖原发性机械损伤与继发性炎症、氧化应激等连锁反应,神经干细胞凭借替代受损细胞、分泌营养因子、调节免疫及促血管生成等机制,成为修复关键力量。SCI后微环境中,ECM通过受体信号调控细胞行为,细胞因子/生长因子依托特异性通路精准作用,炎症反应则在急慢性期呈现促抑双重效应,共同影响神经干细胞迁移分化。
[参考文献]
[1]ANJUM A,YAZID MD,FAUZI DAUD M,et al.Spinal cord injury:Pathophysiology,multimolecular interac-tions,and underlying recovery mechanisms[J].Int J Mol Sci,2020,21(20):7533.
[2]ELI I,LERNER DP,GHOGAWALA Z.Acute traumatic spinal cord injury[J].Neurol Clin,2021,39(2):471-488.
[3]AHUJA CS,NORI S,TETREAULT L,et al.Traumatic spinal cord injury-repair and regeneration[J].Neurosur-gery,2017,80(3S):S9-S22.
[4]HU X,XU W,REN Y,et al.Spinal cord injury:Molecu-lar mechanisms and therapeutic interventions[J].Signal Transduct Target Ther,2023,8(1):245.
[5]KIRSHBLUM S,SNIDER B,EREN F,et al.Characteriz-ing natural recovery after traumatic spinal cord injury[J].J Neurotrauma,2021,38(9):1267-1284.
[6]IZZY S.Traumatic spinal cord injury[J].Continuum(Min-neap Minn),2024,30(1):53-72.
[7]ECKERT MJ,MARTIN MJ.Trauma:Spinal cord injury[J].Surg Clin North Am,2017,97(5):1031-1045.
[8]CHAY W,KIRSHBLUM S.Predicting outcomes after spinal cord injury[J].Phys Med Rehabil Clin N Am,2020,31(3):331-343.
[9]STERNER RC,STERNER RM.Immune response follow-ing traumatic spinal cord injury:Pathophysiology and therapies[J].Front Immunol,2023,13:1084101.
[10]FAN B,WEI Z,YAO X,et al.Microenvironment Imbal-ance of Spinal Cord Injury[J].Cell Transplant,2018,27(6):853-866.
[11]KJELL J,OLSON L.Rat models of spinal cord injury:From pathology to potential therapies[J].Dis Model Mech,2016,9(10):1125-1137.
[12]QUADRI SA,FAROOQUI M,IKRAM A,et al.Recent update on basic mechanisms of spinal cord injury[J].Neurosurg Rev,2020,43(2):425-441.
[13]SUNSHINE MD,BINDI VE,NGUYEN BL,et al.Oxy-gen therapy attenuates neuroinflammation after spinal cord injury[J].J Neuroinflammation,2023,20(1):303.
[14]COFANO F,BOIDO M,MONTICELLI M,et al.Mesen-chymal stem cells for spinal cord injury:Current op-tions,limitations,and future of cell therapy[J].Int J Mol Sci,2019,20(11):2698.










