塞利尼索联合地塞米松治疗复发性多发性骨髓瘤的效果论文
2026-02-26 16:08:21 来源: 作者:xuling
摘要:在复发性MM治疗期间,使用塞利尼索联合地塞米松具有较好疗效,能够提升总反应率,改善血沉、M蛋白、β2微球蛋白水平,调节患者的免疫功能。
[摘要]目的探讨塞利尼索联合地塞米松治疗复发性多发性骨髓瘤(multiple myeloma,MM)患者的应用价值。方法目的选取2022年1—12月曹县人民医院收治的80例复发性MM患者为研究对象,按治疗方法将其分为两组,对照组(n=40)行硼替佐米+地塞米松治疗,观察组(n=40)行硼替佐米+地塞米松+塞利尼索治疗。比较两组临床疗效、血沉、M蛋白、β2微球蛋白、细胞免疫功能及毒性反应发生情况。结果观察组总反应率为70.00%(28/40),高于对照组的47.50%(19/40),差异有统计学意义(χ2=4.178,P<0.05)。两组总有效率比较,差异无统计学意义(P>0.05)。观察组血沉、M蛋白、β2微球蛋白水平均低于对照组,观察组细胞免疫功能优于对照组,差异均有统计学意义(P均<0.05)。两组血液学、非血液学毒性反应发生情况比较,差异均无统计学意义(P均>0.05)。结论在复发性MM治疗期间,使用塞利尼索联合地塞米松具有较好疗效,能够提升总反应率,改善血沉、M蛋白、β2微球蛋白水平,调节患者的免疫功能。
[关键词]多发性骨髓瘤;首次复发;塞利尼索;地塞米松
多发性骨髓瘤(multiple myeloma,MM)是以克隆浆细胞异常增殖为主要特征的恶性疾病,老年人群的患病率较高,可致相关器官功能出现严重损伤[1-2]。MM高度依赖微环境,在基质细胞的保护作用下,常规治疗方法很难有效消除微小的残留病灶,故本病复发风险高。而相较于首诊MM患者,复发病例的治疗难度可随复发次数的增多而显著提升,故应谨慎决策复发性MM患者的治疗方案,并对用药过程进行严格管理。地塞米松为类固醇皮质激素,主要功效包括抗炎、免疫抑制等,既往常用于初诊MM患者[3]。塞利尼索属于核输出蛋白(exportin 1,XPO1)抑制剂,与既往常用药物的机制不同,本品可阻断肿瘤抑制蛋白与致癌蛋白的出核转运,具有增强免疫功能、抑制癌细胞的增殖等作用。本研究对塞利尼索与地塞米松治疗复发性MM患者的应用价值进行分析,现报道如下。
1资料与方法
1.1一般资料
目的选取2022年1—12月曹县人民医院收治的80例复发性MM患者为研究对象,按治疗方法将其分为两组,每组40例。对照组中男24例,女16例;年龄48~71岁,平均(56.17±5.84)岁。观察组中男22例,女18例;年龄49~72岁,平均(55.89±6.17)岁。两组患者一般资料比较,差异均无统计学意义(P均>0.05),具有可比性。本研究经曹县人民医院伦理委员会批准(2021120106)。
1.2纳入与排除标准
纳入标准:年龄30~80岁;符合MM的相关诊断标准[4],且为首次复发;Durie-Salmon分期为Ⅱ~Ⅲ期;临床资料完整;患者及家属均知情同意本研究。
排除标准:伴其他恶性肿瘤者;肝肾功能障碍者;伴其他血液系统疾病者;对本研究使用药物过敏者。
1.3治疗方法
对照组行硼替佐米+地塞米松治疗。第1、4、8、11天给予硼替佐米(国药准字H20173307;规格:3.5 mg)1.3 mg/m2,静脉注射;第1、2、4、5、8、9、11、12天给予地塞米松(国药准字H41022446;规格:1 mL∶2 mg)20 mg,静脉滴注。每个疗程21 d。
观察组行硼替佐米+地塞米松+塞利尼索治疗。第1、8、15、22、29天给予塞利尼索(国药准字HJ20210083;规格:20 mg)80 mg,口服;第1、8、15、22天给予硼替佐米1.3 mg/m2,静脉注射;第1、8、15、22、29天给予地塞米松20 mg,静脉滴注。每个疗程35 d。
两组均治疗3个疗程。
1.4观察指标
①比较两组临床疗效。两组连续治疗3个周期后进行疗效评价,参考MM的疗效标准[5],结果分为完全缓解(complete response,CR)、部分缓解(partial response,PR)、微小缓解(minor response,MR)、疾病复发/进展(progressive disease,PD),计算总体反应率及总有效率。评价标准:CR为血清、尿中单克隆M蛋白消失且持续6周以上,骨髓中浆细胞比例<5%。PR为血清中单克隆M蛋白减少≥50%,且持续6周以上,溶骨性病变大小及数量未增加,软组织浆细胞瘤大小降低>50%。MR为血清中单克隆M蛋白减少25%~<50%,24 h尿蛋白减少50%~<90%,溶骨性病变大小、数量未增加。PD为出现单克隆M蛋白水平增加、浆细胞异常增生、排除其他因素的高钙血症加重、残留骨病变扩大等任一情况。总体反应率=CR率+PR率,总有效率=CR率+PR率+MR率。
②比较两组治疗前后血沉、M蛋白、β2微球蛋白(β2-microglobulin,β2-MG)水平。检测方法:常规采集3 mL静脉血样,血清样本的离心参数:速度3 000 r/min、时间10 min、离心半径8 cm。血沉采用SD-100型动态血沉压积测试仪(上海三崴医疗设备有限公司)检测,M蛋白采用Mindray-BS-350S全自动生化仪(南京贝登医疗股份有限公司)检测,β2-MG采用酶联免疫吸附法检测。
③比较两组治疗前后细胞免疫功能。采集3 mL空腹静脉血,借助DxFLEX流式细胞仪(贝克曼库尔特)检测白细胞分化抗原簇4+(cluster of dif⁃ferentiation 4 receptors,CD4+)、白细胞分化抗原簇8+(cluster of differentiation 8 receptors,CD8+)、CD4+/CD8+。
④比较两组毒性反应发生情况。包括血液学毒性反应(中性粒细胞减少、血小板减少、贫血)与非血液学毒性反应(神经性疼痛、心脏事件、胃肠道反应)。血液学毒性反应发生率=血液学毒性反应发生例数/总例数×100%。非血液学毒性反应发生率=非血液学毒性反应发生例数/总例数×100%。
1.5统计方法
采用SPSS 25.0统计学软件处理数据,计量资料(血沉、M蛋白、β2-MG、细胞免疫指标)经S-W检验,符合正态分布,以(x-±s)表示,组间比较行两独立样本t检验。计数资料(临床疗效、毒性反应发生情况)以例数(n)和率(%)表示,组间比较行χ2检验。P<0.05为差异有统计学意义。
2结果
2.1两组患者临床疗效比较
治疗后,观察组总反应率高于对照组,差异有统计学意义(P<0.05)。两组总有效率比较,差异无统计学意义(P>0.05)。见表1。
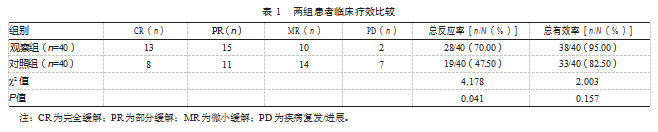
2.2两组患者血沉、M蛋白、β2-MG水平比较
治疗后,观察组血沉、M蛋白、β2-MG水平均低于对照组,差异均有统计学意义(P均<0.05)。见表2。
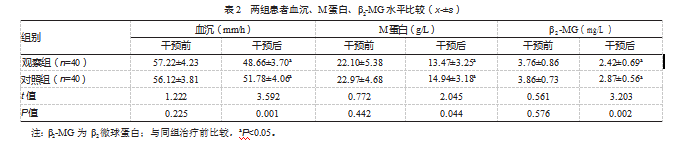
2.3两组患者细胞免疫功能比较
观察组CD4+、CD4+/CD8+水平高于对照组,CD8+水平低于对照组,差异均有统计学意义(P均<0.05)。见表3。
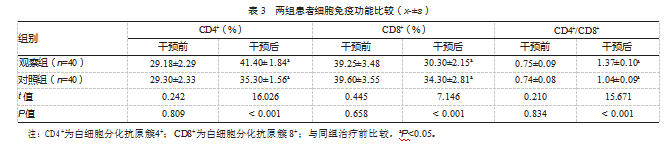
2.4两组患者毒性反应发生情况比较
两组血液学、非血液学毒性反应发生情况比较,差异均无统计学意义(P均>0.05)。见表4。
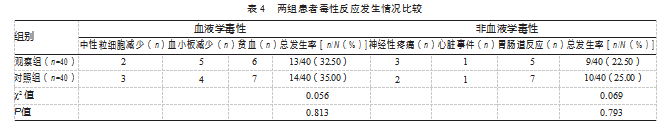
3讨论
免疫抑制微环境在MM疾病复发与病情进展过程中具有至关重要的作用,多种造血细胞、非造血细胞的分泌物可不同程度影响MM细胞的增殖与迁移过程[6-7]。MM复发可显著增加后续治疗难度,导致患者生存质量下降,相关研究指出,需重点关注疾病既往治疗方法、患者功能状态等相关因素,并尽快通过现有治疗方法,获得最佳缓解[8]。首次复发是对复发病例进行医疗干预的重要时间节点,与患者的整体获益、生存质量改善密切相关,故临床应谨慎选择治疗方法。硼替佐米+地塞米松是既往MM治疗的重要方法,但在MM复发病例中的应用效果不佳。塞利尼索是首款口服XPO1抑制剂,主要用于复发/难治性MM[9-11]。根据最新指南的推荐,对首次复发MM患者采用塞利尼索进行治疗,有助于降低疾病进展、死亡风险[12]。而现阶段关于塞利尼索临床应用的报道仍较少,缺乏足够的医学证据与临床用药数据,各类复发病例的治疗决策可能出现偏差。
本研究中,两组均用药3个周期,疗效评价结果显示,两组总反应率分别为70.00%、47.50%,观察组总反应率明显更高(P<0.05)。李莹等[11]对10例复发性MM患者的治疗效果进行分析,结果发现,采用塞利尼索方案的患者,总缓解率可达到70%;GASPARETTO C等[13]发现,采用塞利尼索进行治疗,患者的中位无进展生存期为15个月,总体缓解率达到78%,与本文结果相似。分析两组总反应率出现差异的原因,可能与塞利尼索能够发挥不同于其他药物的抗肿瘤作用机制有关。根据药品的药理分析结果,在多种与MM疾病进展有关的肿瘤抑制蛋白(tumor suppressor protein,TSP)中,塞利尼索均能够发挥显著抑制作用,促使XPO1停留于核内[14]。在抑制XPO1的基础上,激活发挥抗肿瘤作用,能够起到“双重保险”效果,致癌蛋白的表达水平也能够得到有效控制,细胞核内TSP积累减少,多种癌蛋白显著抑制,可致细胞周期停滞。本研究对两组短期内生化指标的检测数据进行比较,结果显示,观察组血沉、M蛋白、β2-MG水平低于对照组(P均<0.05),即增用塞利尼索后,患者的部分生化指标能够得到显著改善。本研究还发现,观察组CD4+、CD4+/CD8+水平高于对照组,CD8+水平低于对照组(P均<0.05)。本研究的细胞免疫指标对比结果提示,塞利尼索治疗对患者的免疫功能提升有积极作用,该优势可能对患者后续的生存质量产生重要影响。TAO Y等[15]发现,采用塞利尼索治疗方案的毒性较低,血液学相关不良反应的发生率为30%,与本文观察组患者的总发生率相近。本研究对象为曹县人民医院的患者,采用非随机抽样方法、样本量有限且随访时间短,研究结论外推性受限。因此未来仍需群体代表性的大样本队列研究加以验证。
综上所述,与硼替佐米+地塞米松治疗比较,增用塞利尼索治疗首次复发MM患者能够进一步提升总反应率,促进血沉、M蛋白、β2-MG等生化指标的下降,并对细胞免疫水平的改善有积极影响。
[参考文献]
[1]钱文斯,沈琳,谢彦晖.老年多发性骨髓瘤患者临床特征分析[J].老年医学与保健,2021,27(3):475-478.
[2]邵雯,周晓霜.合并肾功能损害的多发性骨髓瘤患者临床特征分析[J].临床肾脏病杂志,2020,20(4):282-286.
[3]邓书会,徐燕,隋伟薇,等.硼替佐米环磷酰胺和地塞米松联合诱导治疗初诊多发性骨髓瘤患者131例的临床研究[J].中国肿瘤临床,2022,49(20):1067-1072.
[4]中国医师协会血液科医师分会,中华医学会血液学分会,中国医师协会多发性骨髓瘤专业委员会.中国多发性骨髓瘤诊治指南(2017年修订)[J].中华内科杂志,2017,56(11):866-870.
[5]KUMAR S,PAIVA B,ANDERSON KC,et al.Interna⁃tional Myeloma Working Group consensus criteria for re⁃sponse and minimal residual disease assessment in mul⁃tiple myeloma[J].Lancet Oncol,2016,17(8):e328-e346.
[6]庄荟琳,廖爱军.XPO1抑制剂塞利尼索治疗多发性骨髓瘤的研究进展[J].实用药物与临床,2023,26(7):663-668.
[7]中国医师协会血液科医师分会,中华医学会血液学分会.中国多发性骨髓瘤诊治指南(2022年修订)[J].中华内科杂志,2022,61(5):480-487.
[8]HANSEN DK,SIDANA S,PERES LC,et al.Idecabta⁃gene vicleucel for relapsed/refractory multiple myeloma:Real-world experience from the myeloma CAR T consor⁃tium[J].J Clin Oncol,2023,41(11):2087-2097.
[9]陈琛,张秀莲.塞利尼索在复发难治性多发性骨髓瘤中的研究进展[J].安徽医药,2023,27(6):1061-1064.
[10]邝丽芬,房佰俊,陈文明,等.含塞利尼索方案治疗复发难治多发性骨髓瘤的疗效与安全性分析:一项中国多中心真实世界研究[J].临床血液学杂志,2022,35(9):626-632.
[11]李莹,王耀美,崔玉山,等.塞利尼索为基础方案治疗10例复发难治多发性骨髓瘤疗效观察[J].临床血液学杂志,2023,36(5):327-331.
[12]中华医学会血液学分会浆细胞疾病学组,中国医师协会多发性骨髓瘤专业委员会.中国首次复发多发性骨髓瘤诊治指南(2022年版)[J].中华血液学杂志,2022,43(10):810-817.
[13]GASPARETTO C,SCHILLER GJ,TUCHMAN SA,et al.Once weekly selinexor,carfilzomib and dexa⁃methasone in carfilzomib non-refractory multiple my⁃eloma patients[J].Br J Cancer,2022,126(5):718-725.
[14]GROSICKI S,SIMONOVA M,SPICKA I,et al.Once-per-week selinexor,bortezomib,and dexamethasone versus twice-per-week bortezomib and dexamethasone in patients with multiple myeloma(BOSTON):A ran⁃domised,open-label,phase 3 trial[J].Lancet,2020,396(10262):1563-1573.
[15]TAO Y,ZHOU H,NIU T.Safety and efficacy analysis of selinexor-based treatment in multiple myeloma,a meta-analysis based on prospective clinical trials[J].Front Pharmacol,2021,3(12):758992.










