电化学发光技术在甲状腺肿瘤诊断中的诊断效能论文
2026-02-26 15:28:59 来源: 作者:xuling
摘要:ECLIA与病理结果的Kappa值为0.819,RIA的Kappa值为0.428。结论ECLIA在甲状腺肿瘤诊断中具有更高的精准度和可靠性,为临床鉴别诊断提供了重要依据。
[摘要]目的本研究旨在探究电化学发光技术对甲状腺肿瘤的诊断效能。方法非随机选取2023年1月—2024年12月在天津医科大学肿瘤医院就诊的60例疑似甲状腺肿瘤患者作为研究对象。采用电化学发光免疫分析法(electrochemiluminescence immunoassay,ECLIA)和放射免疫测定法(radioimmunoassay,RIA)检测甲状腺相关指标,并以病理检查为金标准,比较两种方法的检测结果及诊断效能。结果病理检查结果显示,60例受检者中阳性40例,阴性20例。ECLIA检出真阳性36例;RIA检出真阳性30例。ECLIA的特异度、灵敏度、阴性预测值、阳性预测值以及准确度分别为95.00%(19/20)、90.00%(36/40)、82.61%(19/23)、97.30%(36/37)、91.67%(55/60),均高于RIA的70.00%(14/20)、75.00%(30/40)、58.33%(14/24)、83.33%(30/36)、73.33%(44/60),差异均有统计学意义(χ2=4.924,6.545,6.407,4.722,6.984;P均<0.05)。ECLIA与病理结果的Kappa值为0.819,RIA的Kappa值为0.428。结论ECLIA在甲状腺肿瘤诊断中具有更高的精准度和可靠性,为临床鉴别诊断提供了重要依据。
[关键词]电化学发光技术;甲状腺肿瘤;促甲状腺激素;游离三碘甲腺原氨酸;诊断效能
甲状腺肿瘤作为内分泌系统常见疾病,近年来其发病率呈显著上升趋势,准确及时地诊断甲状腺肿瘤对于患者治疗方案的制定和预后改善至关重要[1]。目前,临床中甲状腺肿瘤的诊断依赖于多种手段,包括超声检查、细针穿刺活检以及血清学标志物检测等[2]。其中,血清学标志物检测因其操作简便、创伤小、可重复性高等优势,在甲状腺肿瘤的筛查及辅助诊断中发挥着不可或缺的作用。相关血清学指标,在甲状腺的生理功能调节以及甲状腺疾病的发生发展过程中呈现出特征性变化,常被用于甲状腺疾病的诊断与鉴别诊断[3]。传统的放射免疫测定法(radioimmunoassay,RIA)在很长一段时间内是检测这些血清学标志物的常用方法,为甲状腺疾病的诊断提供了重要依据[4]。然而,RIA存在试剂有效期短、检测灵敏度和特异度有限等缺点,在一定程度上限制了其临床应用。电化学发光免疫法(electrochemiluminescent immunoassay,ECLIA)分析是一种基于电化学发光反应和免疫反应的新型检测技术,具有检测速度快、灵敏度高、特异度强、线性范围宽等诸多优点。该技术已在多个领域得到广泛应用。因此,本研究旨在通过对比ECLIA与RIA对甲状腺肿瘤相关血清学标志物的检测结果,评估ECLIA在甲状腺肿瘤诊断中的效能,现报道如下。
1资料与方法
1.1一般资料
非随机选取天津医科大学肿瘤医院2023年1月—2024年12月在天津医科大学肿瘤医院就诊的60例疑似甲状腺肿瘤患者作为研究对象。采用ECLIA和RIA检测甲状腺相关指标,并以病理检查为金标准,比较两种方法的检测结果及诊断效能。研究对象中男22例,女38例;年龄25~65岁;平均(45.2±8.5)岁。本研究经天津医科大学肿瘤医院伦理委员会审核批准(20220913)。患者及家属对本研究均知情同意,且签署知情同意书。
1.2纳入与排除标准
纳入标准:超声检查提示甲状腺结节直径≥1cm或伴有钙化、边界不清等恶性特征;首次就诊未接受过甲状腺相关治疗。
排除标准:合并严重肝肾功能不全者;患有自身免疫性甲状腺疾病者(如桥本甲状腺炎);妊娠期或哺乳期女性。
1.3检测方法
ECLIA检测:使用罗氏Cobas e601电化学发光免疫分析仪及配套试剂盒(罗氏诊断,德国),检测指标包括甲状腺激素(thyroid hormone,TSH)、游离三碘甲腺原氨酸(free triiodothyronine,FT3)、游离甲状腺素(free thyroxine,FT4)、甲状腺球蛋白(thyro-globulin,Tg)、抗甲状腺球蛋白抗体(anti-thyroglobulin antibody,A-TG)、抗甲状腺过氧化物酶抗体(anti-thyroid peroxidase antibody,A-TPO),参考值:TSH:0.27~4.2μIU/mL、FT3:3.1~6.8 pmol/L、FT4:12~22 pmol/L、Tg:3.5~77μg/L、A-TG:0~115 IU/mL、A-TPO:0~34 IU/mL。2项检测结果超出上述参考值范围即判定为阳性。
RIA检测:使用SN-695B型γ放射免疫计数器(上海原子核研究所)及试剂盒(北京北方生物技术研究所),操作步骤严格按照说明书进行。参考值:TSH:0.3~5.0μIU/mL、FT3:2.8~7.1 pmol/L、FT4:11~23 pmol/L、Tg:2.0~80μg/L、A-TG:0~120 IU/mL、A-TPO:0~35 IU/mL。2项检测结果超出上述参考值范围即判定为阳性。
检测方法:所有患者于清晨空腹采集静脉血5 mL,离心半径8 cm,3 000 r/min离心10 min分离血清,分别采用ECLIA与RIA检测上述指标。ECLIA检测按试剂盒说明书配制电化学发光反应试剂(含标记抗体、发光底物等),平衡至室温,将血清样本、校准品及质控品分别加入反应孔,与包被抗原/抗体的磁珠充分孵育,形成抗原-抗体复合物。通过磁场吸附磁珠,去除未结合物质,重复洗涤3次。加入电化学发光底物,在电极作用下触发发光反应,仪器记录发光强度,根据校准曲线计算样本浓度。RIA检测准备放射性同位素标记抗原、特异性抗体及分离试剂,核对放射活度符合标准。将血清样本、标记抗原与抗体混合,37℃孵育2 h,使抗原与抗体竞争性结合。加入分离试剂,离心后弃上清,测量沉淀中放射性强度。根据标准曲线计算样本中待测物浓度,放射性强度与待测物浓度呈负相关。
1.4观察指标
以病理检查为金标准,比较ECLIA和RIA两种检测方法的检测结果,及灵敏度、特异度、准确度、阳性预测值、阴性预测值诊断效能指标。
1.5统计方法
采用SPSS 24.0统计学软件处理数据,诊断结果、诊断效能为计数资料,以例数(n)和率(%)表示,组间比较行配对χ2检验。一致性分析采用Kappa检验,Kappa≥0.75为一致性极好。P<0.05为差异有统计学意义。
2结果
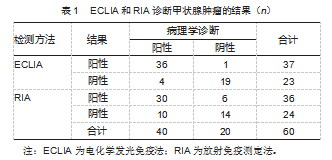
2.1 ECLIA和RIA诊断甲状腺肿瘤的结果
病理检查结果显示,60例受检者中阳性40例,阴性20例。ECLIA检出真阳性36例;RIA检出真阳性30例。见表1。
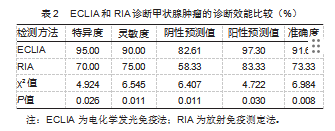
2.2 ECLIA和RIA诊断甲状腺肿瘤的诊断效能比较
ECLIA的特异度、灵敏度、阴性预测值、阳性预测值以及准确度均高于RIA,差异均有统计学意义(P均<0.05)。ECLIA与病理结果的Kappa值为0.819,RIA的Kappa值为0.428。见表2。
3讨论
甲状腺肿瘤近年发病率呈持续上升趋势,早期鉴别结节良恶性是临床诊疗的关键环节。目前临床常用的超声、细针穿刺细胞学检查及传统血清标志物,在诊断中存在一定局限性,尤其对意义不明确的非典型病变、微小癌灶及髓样癌等特殊病理类型的鉴别能力不足。ECLIA作为超敏检测技术,可精准定量BRAF V600E突变相关蛋白、miR-221/222、CK19等新兴标志物,且兼具检测速度快、抗干扰能力强等优势。但当前该技术在不同病理类型甲状腺肿瘤的诊断效能、微小癌检测灵敏度、与分子病理检查的协同应用及术后动态监测等方面,仍需进一步研究。
ECLIA是基于电化学发光原理的免疫测定技术,具有较高的灵敏度和特异度。通过标记物在电极表面的发光反应来检测抗原-抗体复合物的形成,从而实现对目标分子的定量分析[5]。而RIA则是利用放射性同位素标记的抗原或抗体与待测样本中的相应分子竞争结合,通过测量放射性强度来间接反映待测分子的浓度[6]。两种检测原理的本质差异可能导致在检测灵敏度和准确度上存在差异。ECLIA通常采用全自动化学发光免疫分析仪进行检测,操作简便、耗时短,且人为影响因素较少[7]。RIA多为手工操作,耗时较长,且易受操作过程中的不可控因素影响,导致检测结果的精密度和稳定性稍差[8]。这种自动化程度的差异也可能影响两种方法的检测结果。在样本处理和分析过程中,ECLIA和RIA可能存在不同的操作细节和条件设置,如样本采集、储存、预处理以及分析参数的设置等[9-10]。这些差异可能导致两种方法在检测同一指标时产生不同的结果。
本研究显示,60例受检者中阳性40例,阴性20例。ECLIA检出真阳性36例;RIA检出真阳性30例。ECLIA的特异度、灵敏度、阴性预测值、阳性预测值以及准确度均高于RIA(P均<0.05)。ECLIA与病理结果的Kappa值为0.819,表明一致性极好;RIA的Kappa值为0.428,一致性中等。分析原因:ECLIA借助电化学发光反应达成信号的高效放大。标记物在电极激发后,与共反应剂进行能量转移,产生稳定且高强度的特异性发光信号。此信号无需外部光源激发,有效避免了背景光的干扰,并且发光强度与待测物浓度呈现良好的线性关系,检测下限可低至皮克(pg)至飞克(fg)级别。与此同时,磁珠包被技术增加了抗原-抗体的结合表面积,提高了反应效率。通过磁场辅助洗涤去除非特异性吸附物,显著降低了背景噪声,使得微量疾病标志物能够被精准检测,进而实现真阳性病例的高效检出[11-12]。在特异度方面,ECLIA采用高亲和力单克隆或多克隆抗体,确保抗原-抗体反应的高度专一性,减少交叉反应;其非放射性标记体系避免了同位素半衰期及辐射背景的干扰,可精准区分健康人群与患者,大幅降低误诊风险[13-14]。ECLIA通过多水平校准品建立标准化曲线,配合仪器内置实时质控程序,保障反应条件的高度稳定性,结果变异系数CV通常<5%;且其对甲状腺肿瘤特异性标志物的微量变化检测能力,与病理组织形态学及标志物表达的生物学关联性更强,故Kappa值显示极好一致性;而RIA因受同位素干扰、抗体交叉反应较多等因素影响,结果稳定性与特异性较弱,Kappa值仅为0.428,一致性中等,进一步凸显了ECLIA在甲状腺肿瘤诊断中的技术优越性[15]。
综上所述,ECLIA通过高灵敏度和特异度的检测,能更精准地反映甲状腺肿瘤患者的血清指标变化,在肿瘤鉴别中具有显著优势,为临床诊断提供了可靠依据。但本研究具有一定局限性,临床中甲状腺肿瘤患者病情进展差异显著,对于浸润较深甚至转移至其他组织器官的复杂患者群体,并未探究该技术的应用效果,且研究样本量偏小,可能影响研究结果的普适性。未来应纳入亚组深入探究,凸显该技术在不同疾病分级患者群体中的应用效果。
[参考文献]
[1]汤加,徐辰,周春刚.甲状腺肿瘤患者免疫检验中使用电化学发光免疫测定技术的临床效果研究[J].当代临床医刊,2023,36(5):74-75.
[2]朱金矿,王施君.电化学发光免疫测定技术检验TPOAB、TGAB及甲状腺球蛋白的价值[J].中国医疗器械信息,2023,29(6):1-3,93.
[3]詹子雄.电化学发光分析仪进行化学发光免疫测定用于甲状腺肿瘤诊断的临床价值[J].中国医疗器械信息,2023,29(23):109-111.
[4]樊小虎,于卫华,江宣陵.超声造影联合血清DKK-1、Gal-1对分化型甲状腺肿瘤的诊断价值及其与TNM分期、肿瘤恶性程度相关性分析[J].临床和实验医学杂志,2023,22(7):757-762.
[5]邵俊峰.甲状腺肿瘤免疫检测中应用CLIA测定法的价值分析[J].系统医学,2024,9(16):32-34,38.
[6]吴贤文.化学发光免疫法在甲状腺肿瘤生物标志物检测中的应用效果分析[J].生物化工,2019,5(4):76-77,80.
[7]孙鑫,刘业海,郑美娟.甲状腺乳头状癌患者外周血Treg细胞和NK细胞检测及其临床意义[J].临床与实验病理学杂志,2025,41(1):23-31.
[8]张淼,许丹晴,周力,等.影响分化型甲状腺癌术后促甲状腺激素抑制治疗疗效因素的研究进展[J].中国普通外科杂志,2024,33(6):1012-1017.
[9]候丽影,张国强,罗全勇.促甲状腺激素与分化型甲状腺癌关系的研究进展[J].中华核医学与分子影像杂志,2024,44(3):179-182.
[10]林岩松,杨辉,李小毅,等.重组人促甲状腺激素用于低中危分化型甲状腺癌患者的术后评估:Ⅰ期临床研究报告[J].中华核医学与分子影像杂志,2022,42(2):84-89.
[11]牛洁,葛明芹,任旖琳,等.甲状腺肿瘤患者血清炎性细胞因子表达情况及与甲状腺激素的相关性分析[J].中华内分泌外科杂志,2022,16(4):452-456.
[12]卢曼曼,冯其柱.术前血清促甲状腺激素与cN0单侧甲状腺微小乳头状癌中央区淋巴结转移相关性研究[J].国际外科学杂志,2022,49(9):627-632.
[13]唐瑾,张波.常规超声特征、超声造影参数及血清TSH、TgAb水平对甲状腺乳头状癌中央区淋巴结转移的预测价值[J].肿瘤研究与临床,2024,36(10):762-766.
[14]王雅迪,代文杰.低危分化型甲状腺癌术后促甲状腺素抑制治疗的研究进展[J].国际外科学杂志,2024,51(9):644-648.
[15]董家旭,宋美姿,毕讯.射频消融术联合TSH抑制治疗甲状腺微小乳头状癌的效果及生存预后分析[J/CD].中华普外科手术学杂志(电子版),2025,19(2):200-203.










