尼非卡兰与心导管射频消融术联合治疗室性心律失常患者的效果论文
2025-12-22 15:01:08 来源: 作者:xuling
摘要:NIF联合RFCA治疗VA可有效降低心肌损伤标志物水平,优化心电图参数及心率变异性,且并发症发生率较低,具有较高的临床应用价值。
[摘要]目的探讨尼非卡兰(nifekalant,NIF)联合心导管射频消融术(cardiac catheter radiofrequency ablation,RFCA)治疗室性心律失常(ventricular arrhythmia,VA)的临床疗效及安全性。方法目的选取2022年6月—2024年7月于红安县人民医院就诊的119例VA患者为研究对象,按不同治疗方法分为两组。对照组(n=59)行单纯RFCA治疗,研究组(n=60)在RFCA基础上加用NIF治疗。对比两组心肌损伤标志物、心电图参数、心率变异性以及并发症发生率。结果治疗后,研究组N末端脑钠肽前体、肌酸激酶同工酶MB水平低于对照组,差异均有统计学意义(P均<0.05)。治疗后,研究组心电图参数及心率变异性均优于对照组,差异均有统计学意义(P均<0.05)。研究组的并发症发生率为3.33%(2/60),低于对照组的13.56%(8/59),差异有统计学意义(χ2=4.041,P<0.05)。结论NIF联合RFCA治疗VA可有效降低心肌损伤标志物水平,优化心电图参数及心率变异性,且并发症发生率较低,具有较高的临床应用价值。
[关键词]尼非卡兰;心导管射频消融术;室性心律失常;心肌损伤标志物;心率变异性
室性心律失常(ventricular arrhythmia,VA)是临床常见的心律失常类型,包括室性早搏、室性心动过速(ventricular tachycardia,VT)及心室颤动(ven⁃tricular fibrillation,VF),可导致血流动力学障碍,严重者可诱发心源性猝死,是心血管疾病死亡的重要原因之一[1]。目前,VA的治疗手段主要包括药物治疗、心导管射频消融术(cardiac catheter radiofre⁃quency ablation,RFCA)及植入式心律转复除颤器。药物治疗以抗心律失常药物为主,但传统抗心律失常药物(如胺碘酮、普罗帕酮)存在疗效有限、长期应用可能引发心律失常风暴或脏器毒性等不足。RFCA通过靶向消除异常电活动病灶,已成为结构性心脏病相关VA的一线治疗手段,但部分患者因病灶定位困难、消融不彻底或心肌基质异常等原因,术后复发率仍较高[2]。此外,RFCA术中可能诱发短暂性心肌损伤或心律失常,需联合药物治疗以增强疗效并降低风险。尼非卡兰(nifekalant,NIF)是一种Ⅲ类抗心律失常药物,通过选择性阻断快速延迟整流钾电流延长心肌动作电位时程,兼具Ⅲ类和Ⅰb类药物特性,对VT/VF具有快速终止作用,且不显著延长QT间期,致心律失常风险较低[3]。本研究旨在探讨NIF与RFCA联合治疗VA患者的临床效果,为优化VA治疗方案提供理论依据。
1资料与方法
1.1一般资料
目的选取2022年6月—2024年7月于红安县人民医院就诊的119例VA患者为研究对象,按不同治疗方法分为两组。对照组(n=59)中,男36例,女23例;年龄26~73岁,平均(51.52±6.33)岁;冠状动脉粥样硬化性心脏病(简称冠心病)病程4~14年,平均(9.39±2.48)年;VA发病时间1~3 d,平均(2.12±0.36)d。研究组(n=60)中,男32例,女28例;年龄26~73岁,平均(50.89±7.24)岁;冠心病病程4~14年,平均(9.12±2.66)年;VA发病时间1~3 d,平均(2.09±0.38)d。两组患者一般资料对比,差异均无统计学意义(P均>0.05),具有可比性。本研究经红安县人民医院伦理委员会审核批准(2022030811)。患者对本研究知情,自愿签署知情同意书。
1.2纳入与排除标准
纳入标准:年龄为18~75岁;符合VA诊断标准[4],经12导联心电图、动态心电图或心内电生理检查确诊;既往未接受过RFCA治疗,或既往RFCA术后复发;左心室射血分数≥30%。
排除标准:合并严重器质性心脏病者;存在NIF过敏史或禁忌证者;合并恶性肿瘤、严重肝肾功能不全或血液系统疾病者;妊娠期或哺乳期女性;存在精神障碍无法配合治疗及随访者;正在参与其他药物临床试验或近3个月内使用过其他抗心律失常药物者。
1.3治疗方法
对照组行RFCA治疗:所有患者术前行24 h动态心电图监测,明确触发VF或特发性VT的靶室性期前收缩(premature ventricular contraction,PVC)形态、起源部位及耦合间期;经股静脉或锁骨下静脉置入6F四极电极导管至右心室心尖部及流出道,记录希氏束电图及心室电图,诱发VT/VF后标测最早激动点(腔内电图较体表提前QRS波≥25 ms)或碎裂电位区域,结合三维电解剖标测系统(如CARTO/Ensite)定位消融靶点。局部麻醉(1%利多卡因5~10 mL)后,行右侧股静脉穿刺,置入8F鞘管,植入His束电极导管;经右侧颈内静脉穿刺置入6F十极冠状静脉窦电极导管,用于监测左心室电活动;经股静脉鞘管送入3.5 mm冷盐水灌注消融导管(压力监测≥10 g),在三维标测系统引导下将导管头端贴靠靶点区域,行功率控制模式消融(温度≤50℃,功率30~40 W,冷盐水流速17~30 mL/min),消融终点为靶PVC消失或VT/VF无法诱发,且消融后观察30 min无复发。
研究组在行RFCA基础上加用NIF治疗。术后24 h复查心电图,确认无持续性心律失常及严重传导阻滞后,开始静脉注射注射用盐酸尼非卡兰(国药准字H20140113;规格:50 mg),按0.3 mg/kg剂量溶于20 mL生理盐水,经中心静脉通路缓慢推注(5 min内完成),2次/d(间隔12 h)。连续治疗14 d,用药期间持续心电监护。
1.4观察指标
①心肌损伤标志物。于治疗前后,清晨空腹采集静脉血5 mL,采用酶联免疫吸附法检测N末端脑钠肽前体(N-terminal pro-brain natriuretic peptide,NT-proBNP)、肌酸激酶同工酶MB(creatine kinase-MB,CK-MB)。②心电图参数。于治疗前后,应用心电图机(河南威世德医疗设备有限公司,豫械注准20222070114,型号规格:NED-01C)测定校正后的QT间期(corrected QT interval,QTc)、最小QT间期(minimum QT interval,QTmin)、QT间期离散度(QT interval dispersion,QTd)。③心率变异性。于治疗前后,采用动态心电图系统(山东朱氏药业集团有限公司,鲁械注准20242070584,型号规格:ZS-10-12A)测定NN节段窦性RR间期标准差(stan⁃dard deviation of average NN intervals,SDANN)、全程连续窦性RR间期标准差(standard deviation of Normal-to-Normal intervals,SDNN)指标。④并发症发生率。包括心动过缓、低血压、心力衰竭等。并发症发生率=并发症发生例数/总例数×100%。
1.5统计方法
采用SPSS 26.0统计学软件处理数据,心肌损伤标志物、心电图参数、心率变异性为计量资料,经Shapiro-Wilk检验符合正态分布,以(x-±s)表示,组间比较行两独立样本t检验,组内比较行配对样本t检验;并发症发生率为计数资料以例数(n)和率(%)表示,组间比较行χ2检验。P<0.05为差异有统计学意义。
2结果
2.1两组患者心肌损伤标志物比较
治疗后,研究组心肌损伤标志物低于对照组,差异均有统计学意义(P均<0.05)。见表1。
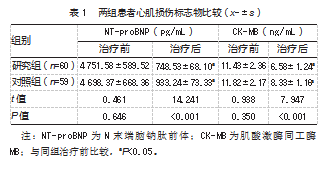
2.2两组患者心电图参数比较
治疗后,研究组心电图参数优于对照组,差异均有统计学意义(P均<0.05)。见表2。
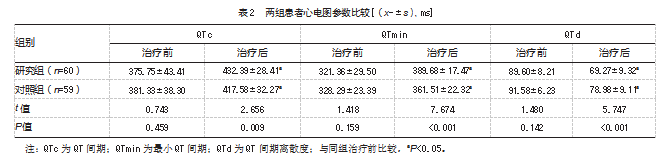
2.3两组患者心率变异性比较
治疗后,研究组心率变异性优于对照组,差异均有统计学意义(P均<0.05)。见表3。
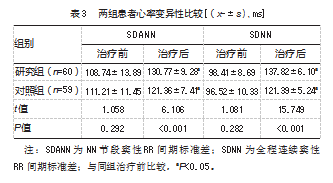
2.4两组患者并发症发生率比较
研究组的并发症发生率低于对照组,差异有统计学意义(P<0.05)。见表4。
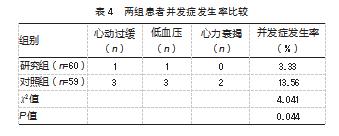
3讨论
VA是临床常见的心脏电活动紊乱,严重时可诱发心室颤动、心源性猝死,其治疗策略的优化始终是心血管领域的研究焦点。传统治疗方法包括药物治疗、电复律及植入式心律转复除颤器,但药物治疗存在不良反应多、疗效个体差异大的局限性,而植入型心律转复除颤器植入则面临感染、电极故障等风险。RFCA通过精准定位并消融异常心肌组织,成为根治VA的重要手段,但其对复杂心律失常的复发率仍较高;NIF作为Ⅲ类抗心律失常药物,可选择性延长心肌细胞动作电位时程,有效抑制折返机制,二者联合应用为VA的治疗提供了新思路[5]。
本研究结果显示,治疗后,研究组心肌损伤标志物低于对照组(P均<0.05)。NIF通过延长动作电位时程,降低心肌细胞复极离散度,减少因电生理紊乱导致的机械应力异常,从而减轻心肌细胞损伤;而RFCA直接消除心律失常起源点,减少异位激动对心肌的反复刺激,二者共同作用降低了心肌细胞因电-机械耦联失调引发的损伤[6-7]。此外,NIF可抑制急性缺血再灌注过程中离子通道的异常激活,进一步减轻消融术后局部心肌的氧化应激损伤,这在降低肌钙蛋白、肌酸激酶同工酶等标志物水平中发挥关键作用[8]。治疗后,研究组心电图参数优于对照组(P均<0.05)。NIF通过延长心肌细胞复极时间,纠正异常的心室复极顺序,使QT间期趋于正常化;同时,其对钠、钾通道的抑制作用可减慢传导速度,与射频消融术消除折返环的效果协同,有效减少了多源性室性早搏及VT的发生[9-10]。心电图参数的优化不仅反映了心律失常控制效果的提升,也提示心肌电活动的整体稳定性增强,降低了恶性心律失常的发生风险[11]。治疗后,研究组心率变异性优于对照组(P均<0.05)。NIF通过调节心肌细胞内离子稳态,减少儿茶酚胺敏感性,抑制交感神经的过度激活,同时增强迷走神经张力;射频消融术消除异位病灶后,降低了异常电活动对自主神经中枢的反馈刺激,使交感-迷走神经平衡得以恢复[12-13]。心率变异性的改善意味着心脏对内外环境变化的适应性增强,有助于降低心律失常复发及心源性猝死的风险。在安全性方面,研究组的并发症发生率低于对照组(P<0.05),与李双菲等[13]的研究结果“非卡兰组并发症发生率为2.7%低于胺碘酮组的17.7%(P<0.05)”一致。NIF不影响心肌收缩力,且无负性频率作用,减少了因血流动力学不稳定导致的术中风险;其延长动作电位时程的特性可降低消融术后局部心肌的电风暴发生率,为组织修复创造稳定的电生理环境。此外,药物对心肌细胞的保护作用也可能减轻消融术后局部炎症反应,降低心包填塞、房室传导阻滞等并发症的发生概率。
综上所述,NIF联合RFCA治疗VA可有效降低心肌损伤标志物水平,优化心电图参数及心率变异性,且并发症发生率较低,具有较高的临床应用价值。未来研究可进一步探索联合治疗的个体化方案,优化药物剂量与消融参数的匹配,以提升治疗精准性和患者远期预后。
[参考文献]
[1]尚冬升,李茂巍,马会勤,等.盐酸尼非卡兰联合心导管射频消融治疗室性心律失常患者的效果观察[J].医学理论与实践,2025,38(7):1125-1128.
[2]万云,丁静韵,卢媛,等.脉冲电场消融在持续性心房颤动中的应用进展[J].实用心电与临床诊疗,2025,34(1):6-10.
[3]李威,毛文军,陈超,等.射频消融和冷冻消融治疗心房颤动的差异性分析[J].浙江临床医学,2025,27(2):238-240.
[4]中华医学会心电生理和起搏分会,中国医师协会心律学专业委员会.室性心律失常中国专家共识基层版[J].中华心律失常学杂志,2022,26(2):106-126.
[5]常国栋,康永安,张红威,等.射频消融术治疗心力衰竭合并持续性心房颤动患者的效果观察[J].临床心身疾病杂志,2025,31(1):27-31.
[6]马廷琼,雷蕾,王炎.尼非卡兰在心房颤动中的应用进展[J].心血管病学进展,2024,45(8):677-680,701.
[7]屠静静,刘统,路营辉,等.尼非卡兰联合普罗帕酮对老年心律失常患者心率变异性及炎症反应的影响[J].实用心电学杂志,2024,33(4):374-378.
[8]孙驰,陈玲玲,孙静静,等.尼非卡兰在持续性心房颤动导管消融术中的应用观察[J].哈尔滨医科大学学报,2023,57(6):630-633.
[9]袁源,吴芳,姜兆磊,等.尼非卡兰控制心脏术后顽固性快速心房颤动的疗效及安全性研究[J].中国心血管病研究,2023,21(11):961-965.
[10]阳恩勇,张良.尼非卡兰转复左心功能不全患者预激综合征合并的心房扑动一例[J].中国心脏起搏与心电生理杂志,2023,37(4):370-371.
[11]罗卉.K+通道阻滞剂尼非卡兰联合酒石酸美托洛尔片对老年心律失常患者HRV的疗效[J].心血管康复医学杂志,2022,31(6):703-708.
[12]卢冬雪,何琦.尼非卡兰对阵发性房颤患者转复情况、复律时间及心室率变化的影响[J].黑龙江医学,2022,46(14):1704-1706.
[13]李双菲,李德才,王庆旭,等.尼非卡兰对心房颤动射频消融术后早期复发的疗效[J].中国心脏起搏与心电生理杂志,2021,35(5):439-442.










