卡瑞利珠单抗联合肝动脉化疗栓塞术治疗中晚期原发性肝癌患者的效果论文
2025-04-24 15:08:58 来源: 作者:xuling
摘要:卡瑞利珠单抗联合TACE治疗中晚期原发性肝癌患者可提高疾病控制率,改善血清学指标水平,降低肿瘤标志物水平,效果优于单纯TACE治疗,但会增高不良反应/并发症发生率。
【摘要】目的:观察卡瑞利珠单抗联合肝动脉化疗栓塞术(TACE)治疗中晚期原发性肝癌患者的效果。方法:选取2020—2022年该院收治的70例中晚期原发性肝癌患者进行前瞻性研究,采用随机数字表法将其分为对照组和观察组各35例。对照组给予TACE治疗,观察组在对照组基础上联合卡瑞利珠单抗治疗,比较两组临床疗效,治疗前后血清学指标[天冬氨酸氨基转移酶(AST)、丙氨酸氨基转移酶(ALT)、白蛋白(ALB)、总胆红素(TBIL)]、肿瘤标志物[甲胎蛋白(AFP)、癌胚抗原(CEA)、甲胎蛋白异质体L3(AFP-L3)]水平,以及不良反应/并发症发生率。结果:观察组疾病控制率为94.29%(33/35),高于对照组的77.14%(27/35),差异有统计学意义(P<0.05);两组客观缓解率比较,差异无统计学意义(P>0.05);治疗后,观察组AST、ALT、TBIL水平均低于对照组,ALB水平高于对照组,差异有统计学意义(P<0.05);治疗后,观察组AFP、CEA、AFP-L3水平均低于对照组,差异有统计学意义(P<0.05);观察组不良反应/并发症发生率为48.71%(17/35),高于对照组的25.71%(9/35),差异有统计学意义(P<0.05)。结论:卡瑞利珠单抗联合TACE治疗中晚期原发性肝癌患者可提高疾病控制率,改善血清学指标水平,降低肿瘤标志物水平,效果优于单纯TACE治疗,但会增高不良反应/并发症发生率。
【关键词】中晚期;原发性肝癌;肝动脉化疗栓塞术;卡瑞利珠单抗;肿瘤标志物;血清学指标
原发性肝癌发病率高、预后差,肝动脉化疗栓塞术(TACE)通过栓塞局部肿瘤血管,切断病灶血液及营养供给,使其缺血坏死,继而延缓肿瘤进展,但单纯TACE治疗效果仍有待提升[1-2]。卡瑞利珠单抗是人源化程序性细胞死亡受体-1(PD-1)单克隆抗体,通过激活体内T细胞,增强免疫系统对肿瘤的杀伤能力,已用于临床部分肿瘤的治疗中,且疗效理想[3-4]。本文观察卡瑞利珠单抗联合TACE治疗中晚期原发性肝癌患者的效果。
1资料与方法
1.1一般资料选取2020—2022年本院收治的70例中晚期原发性肝癌患者进行前瞻性研究。纳入标准:符合原发性肝癌诊断标准[5];肝功能Child-Pugh分级A、B级;巴塞罗那肝癌临床分期系统(BCLC)分期B、C期;美国东部肿瘤协作组(ECOG)评分<2分;预计生存时间>6个月。排除标准:入组前接受过本研究涉及的治疗方案;肝移植术后;合并其他部位肿瘤;伴心、肾功能受损;依从性低,无法顺利配合研究;伴活动性出血。患者及家属了解本研究内容并自愿签署知情同意书,且研究经本院医学伦理委员会审批通过(审批文号:2020188)。采用随机数字表法将其分为对照组和观察组各35例。对照组男20例,女15例;年龄45~68岁,平均(53.31±2.81)岁;肝功能Child-Pugh分级:A级20例,B级15例;BCLC分期:B期20例,C期15例;病灶位置:肝左叶10例,肝右叶14例,肝左右叶11例。观察组男24例,女11例;年龄45~70岁,平均(53.23±2.77)岁;肝功能Child-Pugh分级:A级23例,B级12例;BCLC分期:B期22例,C期13例;病灶位置:肝左叶12例,肝右叶13例,肝左右叶10例。两组一般资料比较,差异无统计学意义(P>0.05),有可比性。
1.2方法对照组采用TACE治疗。患者取仰卧位,消毒铺巾后,采用Seldinger法经股动脉穿刺,置入导管鞘,经血管造影辅助进入肝动脉,观察病灶血管分布情况,将栓塞药15 mL超液态碘化油(上海旭东海普药业有限公司,国药准字H31021603,10 mL)+50 mg注射用盐酸表柔比星[(北京协和药厂有限公司,国药准字H20143165,10 mg)]+20 mL氟尿嘧啶注射液[津药和平(天津)制药有限公司,国药准字H20237081,10 mL∶0.5 g)]+60 mg注射用顺铂[齐鲁制药(海南)有限公司,国药准字H20073652,10 mg],经导管灌注,在造影下观察病灶部位动脉血流情况,使用明胶海绵止血。
观察组在对照组基础上联合注射用卡瑞利珠单抗(苏州盛迪亚生物医药有限公司,国药准字S20190027,200 mg)静脉滴注治疗,200 mg/次,1次/3周,21 d为1个疗程,共治疗2个疗程。
1.3观察指标(1)比较两组临床疗效。靶病灶均消失,且维持4周以上,为完全缓解;靶病灶总径和较基线缩小>30%,且维持4周以上,为部分缓解;介于部分缓解与进展之间,为稳定;靶病灶总径和增大>20%或出现新病灶,为进展[6]。客观缓解率=(完全缓解+部分缓解)例数/总例数×100%,疾病控制率=(完全缓解+部分缓解+稳定)例数/总例数×100%。(2)比较两组治疗前后血清学指标水平。抽取患者空腹静脉血5 mL,3500 r/min离心15 min,离心半径10 cm,留取血清待检,采用日立7600全自动生化分析仪检测天冬氨酸氨基转移酶(AST)、丙氨酸氨基转移酶(ALT)、总胆红素(TBIL)水平,采用化学定量法检测白蛋白(ALB)水平。(3)比较两组治疗前后肿瘤标志物水平。抽取患者空腹静脉血5 mL,3000 r/min离心10 min,离心半径8 cm,留取血清待检,采用酶联免疫吸附法检测血清甲胎蛋白(AFP)、癌胚抗原(CEA)、甲胎蛋白异质体L3(AFP-L3)水平。(4)比较两组不良反应/并发症发生率。
1.4统计学方法应用SPSS 24.0软件进行统计学分析,计量资料以(x±s)表示,采用t检验,计数资料以率(%)表示,采用χ2检验,以P<0.05为差异有统计学意义。
2结果
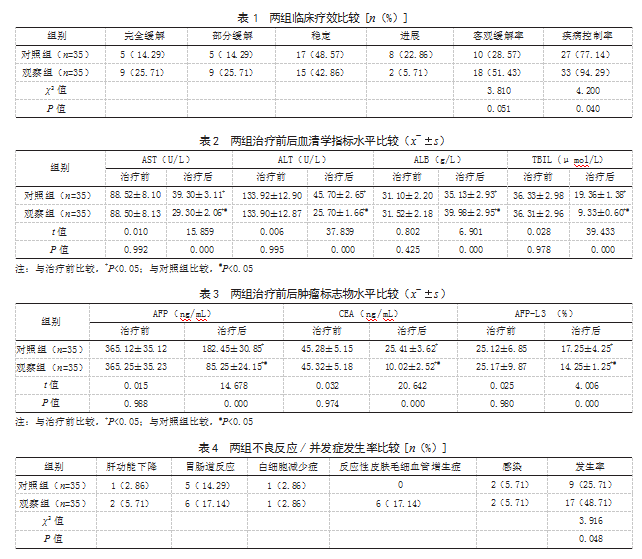
2.1两组临床疗效比较观察组疾病控制率为94.29%(33/35),高于对照组的77.14%(27/35),差异有统计学意义(P<0.05);两组客观缓解率比较,差异无统计学意义(P>0.05)。见表1。
2.2两组治疗前后血清学指标水平比较治疗前,两组AST、ALT、ALB、TBIL水平比较,差异均无统计学意义(P>0.05);治疗后,两组AST、ALT、TBIL水平均低于治疗前,且观察组低于对照组,两组ALB水平均高于治疗前,且观察组高于对照组,差异有统计学意义(P<0.05)。见表2。
2.3两组治疗前后肿瘤标志物水平比较治疗前,两组AFP、CEA、AFP-L3水平比较,差异均无统计学意义(P>0.05);治疗后,两组AFP、CEA、AFP-L3水平均低于治疗前,且观察组低于对照组,差异有统计学意义(P<0.05)。见表3。
2.4两组不良反应/并发症发生率比较观察组不良反应/并发症发生率为48.71%(17/35),高于对照组的25.71%(9/35),差异有统计学意义(P<0.05)。见表4。
3讨论
原发性肝癌发病机制复杂,可能与酗酒、肝炎病毒感染、遗传等因素相关,患者病情进展迅速,预后较差,因肿瘤病灶血供大多来自肝动脉,临床常采用TACE治疗,通过栓塞靶病灶动脉阻断血供,再配合局部灌注化疗药物,抗肿瘤效果显著,目前已广泛用于不可手术切除的中晚期肝癌患者的治疗[7-8]。但随着病情进展,病灶增多,包膜不完整,供血动脉增多,特别是较大体积的病灶,单纯TACE治疗无法完全栓塞,病灶残留、复发风险高,预后不理想[9-10]。
本研究结果显示,观察组疾病控制率高于对照组,血清AFP、CEA、AFP-L3水平均低于对照组。分析原因为卡瑞利珠单抗是PD-1抑制剂,可阻断PD-1蛋白与配体的相互作用,激活并重建机体固有免疫应答,使T细胞增殖、活化,改善T细胞耗竭,持续监视、杀灭肿瘤细胞,抑制其免疫逃逸,提高治疗效果[11-12]。本研究结果同时显示,治疗后,观察组AST、ALT、TBIL水平均低于对照组,ALB水平高于对照组。分析原因为卡瑞利珠单抗联合TACE治疗可发挥协同增效作用,利于控制疾病进展[13-14]。本研究结果还显示,观察组不良反应/并发症发生率高于对照组。分析原因为反应性皮肤毛细血管增生症为卡瑞利珠单抗特有的不良反应,卡瑞利珠单抗激活了免疫应答后,导致促血管生成因子与抑制因子的平衡被打破,引起毛细血管损伤,诱发反应性皮肤毛细血管增生症[15]。
综上所述,卡瑞利珠单抗联合TACE治疗中晚期原发性肝癌患者可提高疾病控制率,改善血清学指标水平,降低肿瘤标志物水平,效果优于单纯TACE治疗,但会增高不良反应/并发症发生率。
参考文献
[1]朱方,赵慧慧,蒋文,等.卡瑞利珠单抗治疗晚期非小细胞肺癌致内分泌系统不良反应临床观察[J].安徽医药,2023,27(9):1904-1908.
[2]李榕,李文利,袁国盛,等.肝动脉灌注化疗术联合靶免对比经动脉插管化疗栓塞术联合靶免治疗中晚期肝癌患者术后引起肝损伤的研究[J].中华肝脏病杂志,2023,31(11):1163-1168.
[3]李榕,李文利,胡晓云,等.RALOX-HAIC联合免疫检查点抑制剂及靶向药物治疗中晚期肝癌的疗效分析[J].中国肿瘤临床,2023,50(11):555-560.
[4]任鹏伟,韩英,周新民.肝细胞癌靶向/免疫治疗效果的预测指标[J].临床肝胆病杂志,2023,39(11):2705-2709.
[5]中国抗癌协会肝癌专业委员会,中华医学会肝病学分会肝癌学组,中国抗癌协会病理专业委员会,等.原发性肝癌规范化病理诊断指南(2015年版)[J].解放军医学杂志,2015,40(11):865-872.
[6]杨学宁,吴一龙.实体瘤治疗疗效评价标准-RECIST[J].循证医学,2004,4(2):85-90.
[7]应希慧,赖林强,陈丽,等.不同时间间隔的肝动脉化疗栓塞和射频消融联合治疗中晚期肝癌的预后分析[J].中华全科医学,2022,20(6):952-955.
[8]刘耀鸿,林宜圣,杨荣焕,等.仑伐替尼联合肝动脉化疗栓塞术对中晚期原发性肝癌患者近期疗效、T淋巴细胞免疫功能及预后的影响[J].临床误诊误治,2022,35(7):60-63.
[9]王静,贾建伟,苗静,等.肝动脉化疗栓塞联合金龙胶囊治疗血瘀郁结证中晚期肝癌疗效及对机体免疫功能的影响[J].山西医药杂志,2022,51(4):367-370.
[10]杨炜浩,仲斌演,杨飞,等.经动脉化疗栓塞联合卡瑞利珠单抗及酪氨酸激酶抑制剂治疗中晚期肝细胞癌的安全性及近期疗效[J].介入放射学杂志,2022,31(5):459-464.
[11]王学国,杨彦,李鹏,等.卡瑞利珠单抗联合安罗替尼和FOLFOX方案治疗晚期肝癌的临床研究[J].现代药物与临床,2022,37(7):1554-1559.
[12]王松,郭兴来,李祥祥,等.卡瑞利珠单抗治疗晚期肝癌合并乙型肝炎病毒感染的疗效观察[J].中国医师进修杂志,2023,46(11):1015-1020.
[13]杜尚云,翁莉,武敏.TACE联合卡瑞利珠单抗治疗中晚期原发性肝癌患者临床疗效研究[J].实用肝脏病杂志,2023,26(1):116-119.
[14]杨晶,张庆桥,魏宁,等.DEB-TACE联合卡瑞利珠单抗治疗中晚期肝癌的临床疗效及对肿瘤标志物和T淋巴细胞亚群的影响[J].现代生物医学进展,2023,23(18):3596-3600.
[15]付吕平,刘卫红,杨晨,等.卡瑞利珠单抗联合阿帕替尼治疗晚期肝癌的疗效与安全评价[J].河北医药,2022,44(24):3788-3790.










