铜绿假单胞菌的代替性治疗新策略论文
2026-04-10 17:36:45 来源: 作者:xuling
摘要:铜绿假单胞菌(Pseudomonas aeruginosa,PA)是一种条件致病菌,致病性强且具有多重耐药(multidrug resistance,MDR),严重威胁着临床环境。
摘要:铜绿假单胞菌(Pseudomonas aeruginosa,PA)是一种条件致病菌,致病性强且具有多重耐药(multidrug resistance,MDR),严重威胁着临床环境。文章探讨治疗PA感染的创新非抗生素策略,包括群体感应抑制、噬菌体疗法、免疫调控、纳米疗法等,为解决PA感染提供了新方向。
关键词:铜绿假单胞菌;噬菌体疗法;群体感应;纳米递送
1 PA的临床挑战
铜绿假单胞菌(Pseudomonas aeruginosa,PA)作为革兰氏阴性条件致病菌,是医院获得性感染的主要病原体。其临床管理面临双重挑战:一方面,因外排泵活化、生物膜形成等机制,PA具有多重耐药[1];另一方面,PA能适应医院营养胁迫、氧化应激等环境,并在医疗器械表面形成持久性生物膜,增加感染风险。近年来,PA患病率上升。2024年,WHO将PA列为高优先级耐药菌。开发针对MDR-PA的新型治疗策略势在必行。
2 PA代替性治疗新策略
2.1群体感应抑制
群体感应(quorum sensing,QS)系统是PA调控毒力因子表达的关键信号网络。已有研究发现(见表1),天然生物活性化合物作为植物源代谢物[2],具备抗氧化、抗肿瘤、抗炎及抗菌功能,在抑制PA的QS系统方面颇具潜力,可降低其毒力因子并阻止生物膜形成—PA的关键保护机制。

2.2噬菌体疗法
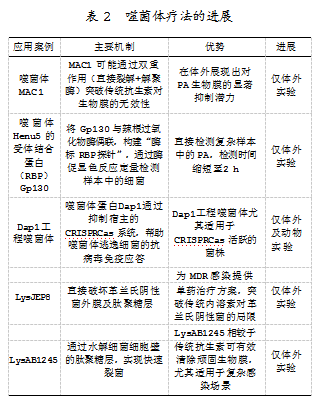
噬菌体是裂解细菌的病毒,其疗法优势显著:能在感染部位复制、高度特异性靶向细菌(不影响有益菌群)、副作用小、对耐药菌株有效、给药方便。作为抗生素替代品,噬菌体抗PA感染研究广泛,目前已发现137种针对假单胞菌属的噬菌体[3]。已有研究多探究噬菌体对慢性PA感染的疗效(见表2)[4]。相较于抗生素治疗,噬菌体疗法对PA生物膜有效且优势显著。
2.3免疫治疗策略
在免疫治疗中,单克隆抗体(monoclonal antibody,mAb)成为对抗PA感染的重要策略,尤其适用于无法从疫苗或传统抗生素中获益的高危个体。mAb通过直接靶向PA提供即时保护,与预防性疫苗联用可能效果更佳。其显著优势在于能解决生物膜内的抗生素耐药问题——开发出的mAb可破坏保护性生物膜,使PA及辅助病原体易受后续抗生素攻击(见表3)。
2.4纳米颗粒
纳米颗粒成为对抗PA的前沿(见表4)。其尺寸通常小于100 nm,体积小、比表面积高,适用于多种化学、生物及生物医学应用,能穿透细菌保护屏障,因具有治疗PA感染的潜力备受关注。PA外膜富含脂多糖、防御强大。目前,已找到使纳米颗粒进入PA细菌细胞壁的方法,但应用仍存在挑战—高表面积带来的反应性可致人体意外反应,并可能迁移至远处器官引发全身毒性。鉴于吸入纳米颗粒与肺部炎症及潜在心血管影响相关,用纳米颗粒治疗细菌性肺部感染时需谨慎。未来研究应聚焦材料选择、颗粒尺寸及给药剂量,优化疗效并降低临床风险。

3结论与未来方向
为应对PA耐药困境,需开拓创新路径。未来研究与治疗核心可聚焦新型辅助制剂的开发及联合策略,重点突破三大瓶颈:基于CRISPR干扰的时序特异性QS抑制剂、噬菌体-宿主互作全基因组预测模型,以及仿生纳米载体血-肺屏障穿透系统。通过多组学精准医疗,推动广谱抗菌向病原特异性治疗转变。
PA感染防控因细菌强适应性、耐药机制复杂及生物膜形成等,常规治疗受限。尽管抗生素与递送技术已经革新,但由于PA快速进化的耐药能力及全球抗生素滥用,替代疗法研发仍具紧迫性。群体感应抑制、噬菌体疗法等非抗生素策略前景可观,但转化应用仍有障碍。创新策略与传统抗生素联合(尤其针对免疫低下患者)具有显著潜力。
参考文献
[1]杨晓静,晏丹,江珍玉,等.铜绿假单胞菌获得性耐药机制研究进展[J].中国人兽共患病学报,2025,41(1):85-93.
[2]FAKHAR M,AHMED M,SABRI N A.Computational and experimental strategies for combating MBL P.aeruginosa(MBLPA)biofilms using phytochemicals:Targeting the quorum sensing network[J].Saudi Journal of Biological Sciences,2024,31(6):104001.
[3]KHEZRI A E,SKURNIK M,ZARRINI G.Pseudomonas aeruginosa bacteriophages and their clinical applications[J].Viruses,2024,16(7):1051.
[4]SINGH J,SOLOMON M,IREDELL J,et al.Overcoming Pseudomonas aeruginosa in Chronic Suppurative Lung Disease:Prevalence,Treatment Challenges,and the Promise of Bacteriophage Therapy[J].Antibiotics,2025,14(5):427.
[5]JUNYA O,JUMPEI F,KINOSHITA M,et al.Effects of the combination of anti-PcrV antibody and bacteriophage therapy in a mouse model of Pseudomonas aeruginosa pneumonia[J].Microbiology Spectrum,2024,12(12):e0178124.
[6]M A H,Emel S,C A M,et al.Development of an anti-Pseudomonas aeruginosa therapeutic monoclonal antibody WVDC-5244[J].Frontiers in Cellular and Infection Microbiology,2023,13:1117844.
[7]AKIOLA R D S,DJAMILA O,GRAZIA V,et al.Recent advances in therapeutic targets identification and development of treatment strategies towards Pseudomonas aeruginosa infections[J].BMC Microbiology,2023,23(1):86.
[8]Jason K,Margalida M,L H M,et al.Monoclonal antibodies against lipopolysaccharide protect against Pseudomonas aeruginosa challenge in mice[J].Frontiers in Cellular and Infection Microbiology,2023,13:1191806.
[9]Fernandes R S,Navarro C A F S D,Carrara E F M,et al.Synergistic activity between beta-lactams and igy antibodies against Pseudomonas aeruginosa in vitro[J].Molecular Immunology,2022,148:1-5.
[10]VARMA A,WARGHANE A,DHIMAN N K,et al.The role of nanocomposites against biofilm infections in humans[J].Frontiers in Cellular and Infection Microbiology,2023,13:1104615.
[11]丁妤亭.近红外光响应的纳米药物协同光热化学动力治疗在铜绿假单胞菌感染中的应用[D].合肥:安徽医科大学,2023.










