对2022年河北省高考化学第14题的评析论文
2023-09-14 17:30:52 来源: 作者:yeyuankang
摘要:2022年河北省高考化学试卷第14题是一道实验综合题,试题立意新颖,考查全面,对考生关键能力和学科素养的考查提供了很好的范例.
摘要:2022年河北省高考化学试卷第14题是一道实验综合题,试题立意新颖,考查全面,对考生关键能力和学科素养的考查提供了很好的范例.
关键词:河北高考;试题评析;高中化学
1试题呈现
题目某研究小组为了更准确检测香菇中添加剂亚硫酸盐的含量,设计了如下实验(实验装置如图1所示):
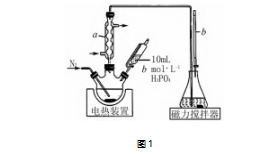
①向三颈烧瓶中加入10.00g的香菇样品和400mL水;锥形瓶中加入125mL水、1mL淀粉溶液,并预加0.3mL 0.01000mol·L-1的碘标准溶液,搅拌.
②以0.2L·min-1流速通氮气,再加入过量磷酸,加热并保持微沸,同时用碘标准溶液进行滴定,至终点时滴定消耗了1.00mL碘标准溶液.
③做空白实验,消耗了0.10mL碘标准溶液.
④用适量Na2 S2 O3替代香菇样品,重复上述步骤,测得SO2的平均回收率为95%.
已知:Ka1(H3 PO4)=7.1×10-3,Ka1(H2 SO3)=1.3×10-2
回答下列问题:
(1)装置图中仪器a、b的名称分别为____、_____
(2)三颈烧瓶适宜的规格为(填标号).
A.250mL B.500mL C.1000mL
(3)解释加入H3 PO4,能够生成SO2的原因:
(4)滴定管在使用前需要、洗涤、润洗;滴定终点时溶液的颜色为;滴定反应的离子方程式为.
(5)若先加磷酸再通氮气,会使测定结果(填“偏高”“偏低”或“无影响”).
(6)该样品中亚硫酸盐含量为mg·kg-1
(以SO2计,结果保留三位有效数字).
2试题解析
根据题意可知,实验原理为:先加过量的磷酸与香菇中的亚硫酸盐发生复分解反应,生成二氧化硫气体,再用氮气将二氧化硫气体排入到锥形瓶中被水吸收,最后用碘标准溶液滴定生成的二氧化硫,从而测出样品中亚硫酸盐含量.
(1)装置图中仪器a、b的名称分别为:球形冷凝管、酸式滴定管.
(2)实验中向三颈烧瓶中加入10.00g香菇样品,400 mL水,后来加入磷酸的体积不超过10 mL.加热时,三颈烧瓶中的液体量不能超过其容积的2/3,因此,选择三颈烧瓶适宜的规格为1000 mL,即选择C.
(3)题目中提供的弱酸的电离常数,在数据关系上有Ka1(H3 PO4)=7.1×10-3<Ka1(H2 SO3)=1.3×10-2,二者的一级电离常数接近,但是H3 PO4为难挥发性的酸,而H2 SO3不稳定易分解为SO2和水,SO2的溶解度随着温度升高而减小,SO2逸出后,促进了化学平衡H2 SO3⥫⥬SO2+H2 O向右移动,因此,加入H3 PO4能够生成SO2的原因为:加入H3 PO4后,溶液中存在化学平衡H2 SO3⥫⥬SO2+H2 O,SO2的溶解度随着温度升高而减小,SO2逸出后,促进了化学平衡H2 SO3⥫⥬SO2+H2 O向右移动.
(4)滴定管在使用之前需要先检查是否漏水,再进行洗涤和用待装溶液润洗;滴定前,锥形瓶溶液中的I2被SO2还原为I-,溶液变为无色,滴加终点时,过量的1滴或半滴标准碘液使淀粉溶液变为蓝色,且半分钟点之内不变色.因此,滴定终点时溶液为蓝色;滴定反应的离子方程式为I2+SO2+2H2 O═══2I-+4H++SO-.
(5)若先加磷酸再通氮气,则不能将装置中的空气及时排出,有部分亚硫酸盐和SO2被装置中的氧气氧化,这样在后面滴定过程中,碘的标准液的消耗量将会减少,因此会使测定结果偏低.

3核心素养视角下对试题的评析
本题的背景材料与生活密切相关,试题情境的创设立意新颖、熟而不俗.近年来,食品安全问题已引起人们的广泛关注,而食品中的添加剂则多为化学物质,研究添加剂的合理使用问题也正好与中学化学的教学活动十分贴近.学科核心素养“科学探究与创新意识”中指出:要引导学生发现和提出有探究价值的化学问题,能够根据探究的目的设计实验方案.善于发现生活中的问题,从化学视角进行思考,运用所学知识提出解决方案.这也体现了“科学态度与社会责任”的学科核心素养.本题中的第(3)问,要对比两种弱酸的电离常数,依据复分解反应原理,推理出加入H3 PO4,能够生成SO2的理论原因.这体现了“证据推理与模型认知”的学科核心素养.此问中,运用了平衡移动原理解释了产生SO2的原因,同样又体现出“变化观念与平衡思想”这一学科核心素养.
参考文献:
[1]杨文彬.高考必刷卷十年真题·化学[M].北京:开明出版社,2022.










