高效液相色谱技术在药物纯化过程中的优化论文
2025-04-17 17:39:29 来源: 作者:xuling
摘要:随着医药行业对纯度要求的不断提高,传统HPLC技术面临着分离效率和操作灵活性的双重挑战。优化HPLC技术可提高药物生产效率,降低成本,提高药品质量。然而,现有的HPLC优化研究集中在某一方面,缺少在药物纯化领域的深入探讨。
摘要:随着医药行业对纯度要求的不断提高,传统HPLC技术面临着分离效率和操作灵活性的双重挑战。优化HPLC技术可提高药物生产效率,降低成本,提高药品质量。然而,现有的HPLC优化研究集中在某一方面,缺少在药物纯化领域的深入探讨。因此,文章主要对HPLC技术在药物纯化过程中的系统优化展开深入探讨,以期为制药行业提供一套更高效、经济、稳定的药物纯化技术方案。
关键词:高效液相色谱;药物纯化;制药行业
随着新药物开发和复杂药物制备需求不断增长,传统纯化技术面临着效率低下、成本高昂和可持续性不足等诸多挑战。在此背景下,高效液相色谱(HPLC)技术,以其高分辨率、高灵敏度和高操作灵活性,被广泛应用于药物的分析与纯化。HPLC技术能够通过不同组分在移动相和固定相中的相对亲和力差异来实现物质的分离。该技术的优化很大程度上决定着药物分析的精确性,直接关系着纯化过程的效率和成本。然而,随着药物分子结构复杂性的增加,传统HPLC的应用已难以满足高效纯化的要求。
通过优化HPLC的梯度洗脱条件、温度、流速和柱选择等参数,可显著提高分离效率和分析速度。温度对HPLC分离效果具有显著影响,适当提高柱温有助于增强某些药物成分的峰形,从而提高分离效率和检测灵敏度[1]。因此,本文将集中探讨HPLC在药物纯化过程中的优化策略,以期提供更有效、经济的纯化解决方案,支持制药行业的可持续发展。
1 HPLC技术概述
1.1原理及组件
HPLC的核心原理在于不同化合物在移动相和固定相间的相互作用差异,而相互作用又会使各组分在色谱柱中以不同速率移动,从而实现分离。HPLC的主要组件及其功能如表1所示。
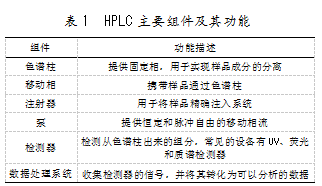
HPLC技术的优化涉及对表1中各组件的选择和配置的调整,需关注不同类型的色谱柱、调整移动相的组成,以及优化操作条件(如温度、流速等),以达到更高的分离效率和分析精度。在此操作下,HPLC将能被有效用于药物的纯化过程,满足不同的分析需求,从而在药物分析和质量控制中发挥更大作用[2]。
1.2应用领域
在药物分析领域,HPLC被用于原料药和成品药的质量控制,以确保药物的纯度和成分符合严格的药品制造标准。对于单克隆抗体的生产,HPLC能有效地从复杂的生物体系中分离出具有治疗活性的抗体分子。这种分析涉及常规的成分定性和定量,并包括对抗体药物的糖基化模式和其他修饰形式的深入分析,可直接影响药物的效力和人体的免疫反应。在食品安全领域,食品中的微量添加剂和污染物,如农药残留和食品包装材料中的塑化剂等,会给消费者健康带来潜在风险[3]。HPLC的应用则可准确地检测并量化这些物质的存在,有效对接食品安全标准。
2色谱柱的选择对药物纯化的影响
2.1色谱柱种类
不同类型的色谱柱根据其物理和化学特性差异,可满足不同的分析需求。常用的HPLC色谱柱种类如表2所示。
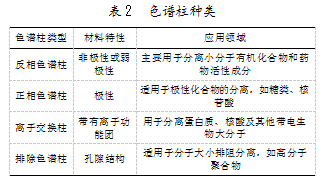
反相色谱柱是HPLC中使用最为广泛的色谱柱类型,通常使用硅胶为基质,表面附着烷基链(如C18或C8),非极性很强,主要用于分离从非极性到中等极性的化合物;正相色谱柱的表面含有极性基团,适用于分离极性较强的样品,在药物发现的早期阶段筛选天然产物和新化合物方面具有较高价值,可有效处理和分离强极性混合物;离子交换色谱柱强调利用样品分子与色谱柱填料上的离子团间的电荷相互作用,常用于蛋白质和其他大分子生物物质的纯化;排除色谱(GPC/SEC)主要依据分子大小进行分离,适用于大分子如聚合物和蛋白质等的分析。
2.2色谱柱材料的影响
2.2.1硅胶基色谱柱
硅胶基色谱柱的优点在于其出色的机械稳定性和化学惰性。硅胶基质由二氧化硅构成,表面通过硅烷化处理引入各种烷基链。这些烷基链赋予了色谱柱不同的疏水性能,使其能有效地分离从非极性到中等极性的化合物。硅胶柱的核心优势在于其高分辨率和优异重现性[4]。另外,硅胶柱对温度和pH的宽容度较高,允许在较广泛的条件下运行。这拓宽了其在药物分析和纯化中的适用性。
2.2.2聚合物基色谱柱
聚合物基色谱柱适用于分离极性较强或具有生物活性的大分子。与硅胶基柱相比,聚合物基色谱柱由多种合成聚合物如聚苯乙烯-二乙烯苯或聚甲基丙烯酸甲酯等材料制成,具有更高的化学稳定性和更宽的pH操作范围(通常为1~14)。这使得聚合物基柱适用于分离易被酸碱条件降解的敏感分子。另外,聚合物基色谱柱通常具有更均匀的孔径分布,可实现更精确的分离效果。
2.2.3混合基材色谱柱
混合基材色谱柱提供了高效液相色谱(HPLC)处理多样化分析需求的强大工具。这些柱子由硅胶和聚合物等不同材料的混合物构成,能够结合各自优点,实现有效分离。混合基材的设计使色谱柱能够在更广泛的化学环境下运行,优化了柱子的机械强度和化学耐受性。例如,混合基材色谱柱在酸性到强碱性环境中均可保持良好的分离性能。
2.3填充载体的物理化学属性
2.3.1粒径大小的影响
较小的粒径可提供更大的表面积,增加样品分子与填充材料接触的机会,从而提高分离效率和峰的分辨率。小粒径填充物尤其适用于复杂样品的分析。其中,目标分析物需要从众多相似化合物中被精确分离开来,这种精细的分离能力使得小粒径填充可显著提高药物成分的检测灵敏度和定量准确性。然而,小粒径也会导致色谱柱背压增高,要求使用能承受更高压力的色谱系统,进而增加设备的操作成本。
2.3.2孔径大小的影响
孔径大小直接影响分离过程中的分子筛选和吸附作用,较大孔径允许大分子的进入和交互作用,适用于大分子如蛋白质或多糖类的分离。该类大孔径的色谱柱提供了足够空间,允许大分子进入孔隙中进行有效的相互作用且不被排除,保证了分离的有效性和分析的准确性。在药物纯化过程中,选择适当孔径的色谱柱对于目标化合物的选择性和回收率至关重要。对于较小药物分子,使用较小孔径的色谱柱有利于增强分子与填充材料表面的相互作用,从而提高分离效率和峰的尖锐度。
3高效液相色谱技术在药物纯化过程中的具体应用
3.1具体应用
β癌症治疗药物期间使用HPLC进行了小批量
的药物纯化。具体使用了半制备型HPLC系统,装填了C18色谱柱。药物的纯化过程中设置了复杂的梯度洗脱程序,从25%乙腈开始,40 min内升至75%乙腈,流速为5 mL/min,同时采用紫外检测器在280 nm处进行检测。通过该过程,成功从反应混合物中分离出高纯度的目标化合物,纯度评估为99.2%,为后续临床试验提供了高质量的候选物质。
3.2少量小分子药物纯化
高效液相色谱(HPLC)技术通常涉及复杂的合成路径,需要采用高度精确的纯化方法来确保最终产品的质量和效能。本案例使用半制备型HPLC系统,配备C18反相色谱柱,能够有效处理从毫克到克级别的样品。同时,进行梯度洗脱,允许通过调整溶剂比例(通常是水和有机溶剂如乙腈或甲醇等),在分析过程中逐渐增强洗脱强度,以优化目标化合物的洗脱时间和峰形。纯化过程中的关键参数如表2所示。
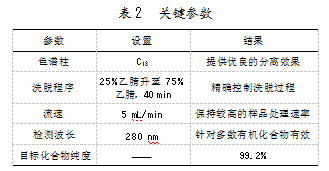
纯度的高评估值表明HPLC能从复杂混合物中有效分离出目标化合物,且确保了高纯度,对于后续药效测试和临床试验具有重要意义。使用HPLC进行少量小分子药物的纯化可显著加速从实验室到临床试验的过程,并降低生产成本。该项技术的应用提供了可靠、高效率的纯化手段,特别是对于高价值、低容错率的药物研发项目。
4结论
本文系统探讨了高效液相色谱(HPLC)技术在药物纯化过程中的关键参数优化,通过深入分析不同类型的色谱柱(如硅胶基、聚合物基和混合基材色谱柱等)及其物理化学属性,强调匹配药物性质与色谱柱特性的重要性,从而实现高效、精确的药物分离和纯化。总之,HPLC技术的深入优化为制药行业提供了更高效、经济和稳定的药物纯化方案,为未来药物研发和质量控制提供了有力的技术支持。
参考文献
[1]童嘉琦,朱谷焕,蓝航镇,等.分散固相萃取-高效液相色谱-串联质谱法测定消毒产品中42种抗微生物药物[J].色谱,2024,42(11):1077-1086.
[2]金晓峰,赵贵,田兵,等.固相萃取-超高效液相色谱-串联质谱法快速测定鸡粪中37种抗菌药物的含量[J].分析科学学报,2024,40(3):315-322.
[3]王欣然,齐建平,吴夏青,等.制备型高效液相色谱在药物分离纯化中的应用研究进展[J].分析试验室,2014,33(12):1476-1480.
[4]杨秉呼,王升启.反义寡核苷酸药物的高效液相色谱大规模纯化技术[J].国外医学(药学分册),1999(6):359-363.










