酶催化在维生素及其衍生物制备中的应用论文
2024-09-24 16:23:02 来源: 作者:liziwei
摘要:酶属于天然催化剂,在不同条件下均具备较强的催化性能。近年来,为了推动生物、工业等行业快速发展,酶的有效性及其多方面应用成为研究的重点之一。目前,VC、VB2、VB12通过发酵法进行生产,而其他维生素主要采用化学合成方法生成,酶催化的应用方式在逐渐增多。不同种类的酶,在不同底物、不同条件下,得到的催化效果是不一样的。
摘要:酶属于天然催化剂,在不同条件下均具备较强的催化性能。近年来,为了推动生物、工业等行业快速发展,酶的有效性及其多方面应用成为研究的重点之一。目前,VC、VB2、VB12通过发酵法进行生产,而其他维生素主要采用化学合成方法生成,酶催化的应用方式在逐渐增多。不同种类的酶,在不同底物、不同条件下,得到的催化效果是不一样的。
关键词:酶;酶催化;维生素;衍生物
大部分酶都是具有催化功能的蛋白质,还有一小部分天然酶是RNA。自然界中存在具有诸多功能的酶,不仅对特定底物表现出一定的选择性,在催化反应中也展现出了卓越的效率。值得注意的是,在非自然环境中,酶的催化过程、底物选择,以及催化环境均呈现出多样化的特点,这为酶在多个领域的应用提供了广阔的可能性。
1酶催化合成维生素或其中间体
1.1 VB3
VB3又被称为烟酸,在我国还未实现长期、大规模生产。尽管运用氨氧化法,以3-甲基吡啶为原料可以合成烟酰胺,但这种方法存在明显缺陷,效率低下且经常产生副产物烟酸。Asano等将微生物J1中发挥关键作用的酶命名为腈水合酶。该种酶主要来源于细菌,拥有多种类型,包括非血红素铁离子依赖型、非类咕啉钴离子依赖型,以及其他金属离子依赖型。
1.2 VB5
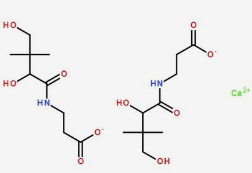
VB5又被称为D-泛酸,在生物体内广泛存在,主要用于合成辅酶A,是一种在细胞代谢中发挥关键作用的物质。VB5主要通过化学法合成,需要用到手性拆分剂,但这些拆分剂不仅成本较高、有毒,且分离较为困难。目前,工业生产中常采用选择性水解D-泛解酸内酯的方法来回收生成的D-泛解酸,并通过酯化反应获得高纯度的D-泛解酸内酯。这一过程的重点在于控制水解程度,以确保其不彻底水解,从而提高回收的D-泛解酸内酯的纯度。通过这种方法,可以实现对资源的有效利用,并提高产品的质量和产量。D-泛解酸内酯水解酶在多种丝状真菌中存在,如赤霉菌属等。在传统筛选过程中,研究者利用溴百里酚蓝等酸碱指示剂识别土壤中具有D-泛解酸内酯水解酶活性的菌株,并采用化学试剂、紫外线照射或常压室温等离子体(ARTP)诱变等方法,进一步筛选出具有更高D-泛解酸内酯水解酶活性的菌株。
β-丙氨酸是VB5的直接前体,有助于促进肌源活性肽与辅酶A的合成。丙烯腈化学合成方法往往伴随着很多废盐的产生,缺点较为明显。相比之下丙烯酸化学合成方法则不会有废盐产生,反应过程更加简洁。发酵法合成β-丙氨酸是通过基因工程手段来改造大肠杆菌。酶催化合成β-丙氨酸的方法主要有三种,其中最直接的方式就是利用富马酸或天冬氨酸作为底物进行合成。然而,不管是将富马酸还是天冬氨酸作为底物,均存在一些问题。同时,上述路线还可能需要解决酶活性较低和副产物积累的问题。对于天冬氨酸路线,其虽然原料成本较高,但可以借助基因工程技术对天冬氨酸-α-脱羧酶进行改造,以提高其催化效率和β-丙氨酸的产量,原因在于其酶活性水平本身比较低。
2017年,吴边等发明了以丙烯酸为底物的酶催化法,并在工业领域得到了逐步应用。丙烯酸酶催化法不仅成本支出较少,且收率更高,简化了原本的反应合成步骤,与化学法相比优势更为显著。
1.3 VC
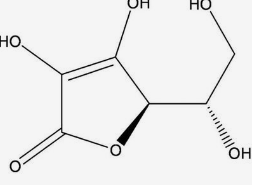
VC是人体必需的维生素,可以治疗坏血病,被广泛应用于各个行业中。
我国科学家不断利用诱变等创新方法来优化菌株,最终成功研发出两步发酵法来生产VC。其具体流程如下。第一步,利用氧化葡萄糖酸杆菌将D-山梨醇催化转化为L-山梨糖。其中,D-山梨醇脱氢酶发挥着核心催化作用,并以吡咯喹啉醌(PQQ)作为辅酶。第二步,混合使用普通生酮基古龙酸菌和巨大芽孢杆菌进行发酵,将L-山梨糖转化为2-酮基-L-古龙酸(2-KLG),以提高2-KLG的产量和纯度。最终2-KLG可通过酯化及内酯化反应合成VC。就工业发展现状来看,采用两步发酵法的主要原因在于,该方法所使用的酶均为PQQ依赖型脱氢酶,不仅可作为催化底物,还能为细胞生长提供一定的能量。采用发酵法有助于提高原料利用率,节约成本。此外,Zeng等已实现了一步发酵合成2-KLG,产量高达72.4 g/L。
1.4 VD3
VD3即胆钙化醇,可治疗甲状腺机能衰退、骨质疏松症等疾病。数据显示,我国的VD3产能约占全球产能的75%。就VD3的本质特点来看,其本身没有生物活性,当相关元素进入生物体内后,会通过一系列的羟化反应生成活性VD3,然后再逐步发挥相应的生理作用。活性VD3可通过化学合成法与酶催化法合成。其中,前者的合成途径比较复杂,且要求较高、条件较多、步骤繁琐,同时还会在一定程度上污染环境,在现实生活中并不能实现大规模生产;后者则具有催化位点特异性,P450羟化酶能特异性催化VD3相应位点羟基化。
2酶催化合成维生素衍生物
2.1 VA衍生物
VA主要包括VA1和VA2两种,VA1即视黄醇,VA2即3-脱氢视黄醇。一般情况下,人们所说的VA指的是VA1,可通过食用富含β-胡萝卜素等的食物来补充VA1。同时,VA及其衍生物可促进免疫球蛋白合成,有助于维护正常的视觉功能,促进生物健康生长,抑制肿瘤生长。VA是脂溶性维生素,直接暴露在空气中会变得不稳定,且紫外线照射也会使其极易失去活性。VA对皮肤具有一定的刺激性,因此其在医药化妆品行业中的应用频率并不高。由于VA醋酸酯的结构不稳定,因此目前工业中常制备的是VA丙酸酯、VA棕榈酸酯等。传统的化学合成法需要用到相关有毒试剂,安全性得不到保障,而酶催化的作用能有效避免这一缺点。例如,高静等采用脂肪酶催化合成VA乳酸酯,收率达52.19%。
2.2 VC衍生物
2.2.1 VC糖苷类
VC葡萄糖苷有多种同分异构体。其中,谁受到的关注最高?表意不明受到的关注度最高,因为其热稳定性和生物活性最好。进入细胞后,其可以被水解成VC并发挥生理活性,不仅可以抵御紫外线,还可以抑制黑色素的生成,因此在化妆品行业得到了广泛应用。当前,通过酶法可将葡萄糖基转移到VC上,形成糖苷键,而这一过程需要催化酶的作用,酶包括环麦芽糊精葡聚糖转移酶(CGtase)等。就CGtase的本质来看,其可以催化淀粉水解成环糊精,也可以利用α-环糊精等作为糖基供体合成。β-环糊精的应用频率最高,原因在于其成本较低,但也存在水溶性较差的缺点,可分为嗜常温和嗜热两种。其中,对来源于嗜热脂肪芽孢杆菌的研究最多,其不仅可以催化糖基转移合成AA-2G,还可以合成熊果苷等。但是,大部分的酶催化活性并不高,同时催化过程中还会产生其他副产物,需要用糖化酶等进一步水解生成。刘龙等通过研究,使多位点组合突变获得高活性突变体,提高了产物的浓度,达到了2.23 g/L,催化活性提高了4倍。
2.2.2 VC酯类
采用脂肪酶合成VC磷酸酯或VC棕榈酸酯是较为常见的VD酯类合成方法。2001年,日本某公司开发出了一种新方法,即用酶法合成VC磷酸酯。具体来说,这一过程以维生素C和磷酸为基础原料,利用铜绿假单胞菌作为全细胞催化剂,随后加入NaOH进行中和反应,最终得到VC磷酸酯钠盐。该方法对反应条件具有较高的要求,这是因为VC易溶于水,但棕榈酸难溶于水,在选择反应溶剂时,就要确保溶剂既能溶解VC,又能溶解棕榈酸。叔戊醇等溶剂便是满足这一要求的选择之一。值得注意的是,不同溶剂的反应转化率可能会存在显著的不同。大量研究证明,叔戊醇在某些化学反应中表现出了较高的转化率。尽管在非水相体系中,脂肪酶能够有效催化酯类的合成,但这并不意味着完全不需要水的参与。事实上,为了达到理想的反应效果,仍需要少量水的存在。考虑到底物溶解性问题,应着重关注溶剂的种类和比例。Karmee等先用化学法合成棕榈酸乙烯酯作为底物,然后将脂肪酶作为催化剂,实现了VC棕榈酸酯的合成。
2.3 VE衍生物
VE是一种脂溶性维生素,天然VE包括生育酚和生育三烯酚等。研究发现,VE有8种异构体,其中又以α-生育酚的含量最为丰富,且具有一定的活性。通常情况下,现实生活中所说的VE就是α-生育酚。工业上,将VE转化成VE衍生物,有利于进一步增强其稳定性,使其应用范围更加广泛。VE衍生物中常见的有VE酯类等,主要通过采用化学法合成。梳理相关研究成果得知,在酶催化过程中,脂肪酶CRL的活性较强,催化收率达到了28.37%。尹春华等[7]利用琥珀酸酐修饰诺维信脂肪酶,发现修饰后的酶相较于原始酶而言,能够更好地进行催化作用,催化收率达到了94.4%。
3结语
酶本质上是一种生物大分子,酶催化技术在各个领域得到了广泛应用。相对于生物发酵来说,酶催化不依赖活细胞,生物安全性更高,耐受范围更广,应用形式也更多。
参考文献
[1]吴边,刘洋,李瑞峰,等.天冬氨酸酶变体及其制备方法与应用:CN 202110768059.5[P].2021-09-21.
[2]ZENG W,WANG P,LIN,et al.Production of2-keto-L-gulonic acid by metabolically engineered Escherichia coli[J].Bioresource Technology,2020,318:124069.
[3]YOSHIKAZU F,HIROKI K,KENJI N,et al.Purification,characterization,and directed evolution study of a vitamin D3 hydroxylase from Pseudonocardia autotrophica[J].Biochemical and Biophysical Research Communications,2009,385(2):170-175.
[4]高静,姜艳军,马丽,等.混合溶剂中酶促合成维生素A乳酸酯[J].分子催化,2006(4):346-350.
[5]LIU L,XU Q Y,HAN R Z,et al.Improving maltodextrin speci ficity for enzymatic synthesis of 2-O-D-glucopyranosyl-L ascorbic acid by site-saturation engineering of subsite-3 in cy clodextrin glycosyltransferase from Paenibacillus macerans[J].Journal of Biotechnology,2013,166(4):198-205.
[6]KARMEE S K.A two step chemo-enzymatic method for the synthesis of fatty acid ascorbyl esters[J].Journal of Oil Palm Research,2012,24:1518-1523.
[7]YIN C H,ZHANG C,GAO M.Enzyme-catalyzed synthesis of vi tamin E succinate using a chemically modified novozym-435[J].Chinese Journal of Chemical Engineering,2011,19(1):135-139.










