平板计数法检测化妆品中需氧细菌总数的不确定度评估论文
2024-09-24 16:50:26 来源: 作者:liziwei
摘要:文章将不确定度原理引入平板计数中,以测量需氧细菌总数检测过程中平皿计数法的检测误差。检测方法参照USP 2023<61>中的“非无菌产品微生物限度检查”,采用微生物计数法定量检测化妆品中的需氧细菌总数,并参照JJF1059.1-2012《测量不确定度评定与表示》中的要求,用需氧细菌总数对数值表示,通过评定需氧细菌总数检测中平皿计数法测量的不确定度,探讨平皿计数的检测误差。结果表明,平皿法检测需氧菌总数的测量误差主要由A类评定的不确定度所致,而B类评定不确定度造成的误差可以忽略不计,因而据此得出
摘要:文章将不确定度原理引入平板计数中,以测量需氧细菌总数检测过程中平皿计数法的检测误差。检测方法参照USP 2023<61>中的“非无菌产品微生物限度检查”,采用微生物计数法定量检测化妆品中的需氧细菌总数,并参照JJF1059.1-2012《测量不确定度评定与表示》中的要求,用需氧细菌总数对数值表示,通过评定需氧细菌总数检测中平皿计数法测量的不确定度,探讨平皿计数的检测误差。结果表明,平皿法检测需氧菌总数的测量误差主要由A类评定的不确定度所致,而B类评定不确定度造成的误差可以忽略不计,因而据此得出可以扩展不确定度。研究所得的通过对需氧细菌总数检测中平皿计数结果的测量进行不确定度评定,可用于评估平皿计数法的检测误差。
关键词:化妆品;平板计数法;需氧细菌总数;不确定度;标准不确定度;扩展不确定度
随着科技的不断发展,我国的国民生活水平也在日益提高,而人们对美的追求永无止境。在此背景下,各种化妆品应运而生,并已成为人们日常生活的重要组成部分。国内化妆品要想出口到国外,就必须通过国际标准检测,如USP、ISO标准等,并获得认可,从而顺利进入国外市场。由此可见,USP药典检测方法的必要性,故而本文对利用药典方法进行化妆品检测的可行性及不确定因素展开评定。
在化妆品生产、流通的过程中,需氧细菌总数是一项至关重要的卫生指标,必须予以严格控制。本文基于美国药典<61>章节中的“非无菌产品微生物限度检查”,采用微生物计数法中的平板计数法对需氧细菌总数进行检测,对测试过程中存在的不确定因素进行分析,并论述化妆品需氧细菌总数计数中不确定度的评定步骤、检测结果及其不确定度在定量检测过程中的应用。研究表明,化妆品卫生指标采用药典标准检测具有一定的可行性,可以为化妆品卫生指标检测提供理论依据。
1实验部分
1.1试验方法
根据USP 2023<61>中的“非无菌产品微生物限度检查”,采用微生物计数法进行检验。
1.2主要试剂和培养基
稀释液Diluent为0.85%NaCl+0.1%蛋白胨;胰酪大豆胨琼脂培养基TSA;
胰酪大豆胨液体培养基TSB;
以上试剂在121℃条件下灭菌处理15 min。
1.3主要仪器
漩涡振荡器;拍击式均质器;二级生物安全柜;恒温水浴摇床;移液枪;电热恒温培养箱;麦氏比浊管;高压灭菌锅。
1.4供检测样品的处理方法
测试前,首先应根据供测试产品的物理化学特性与生物学特征,采用适宜的方法制备符合要求的供检样液。如果用来测试的供检样液的制备过程需进行加温处理,则应保证受热均匀,并将温度控制在45℃以下,总时间控制在1 h之内。检测中,经常使用的样品供检样液处理方法步骤如下。
第一,水溶性产品的制备。通过无菌操作称取10 g或10 mL样品于无菌袋中,加入90 mL pH为7.0的缓冲氯化钠-蛋白胨或磷酸盐缓冲液或TSB或LeB(对于化妆品或可能含有防腐剂的产品),均质1 min制成浓度为10-1的稀释液。如有必要,可调节pH至6~8。再吸取1 mL上述样液(10-1的稀释液)至9 mL经灭菌处理的同质稀释液中,制成10-2的稀释液,依此同样制成10-3,10-4……的稀释液。
第二,不溶于水的非脂溶性样品的制备。通过无菌操作称取10 g或10 mL样品于无菌袋中,加入90 mL pH为7.0的缓冲氯化钠-蛋白胨或磷酸盐缓冲液或TSB或LeB(对于化妆品或可能含有防腐剂的产品),均质1 min制成浓度为10-1的稀释液。如有必要,可调节pH至6~8(可加入1 g/L的吐温80来提升样品的均匀度)。吸取1 mL上述样液(10-1的稀释液)至9 mL经灭菌处理的同质稀释液中,制成10-2的稀释液,依此同样制成10-3,10-4……的稀释液。
第三,脂溶性样品的制备。通过无菌操作称取10 g或10 mL样品,使用经灭菌处理的膜过滤装置进行过滤,制成样本,或无菌称取10 g或10 mL样品于无菌袋中,加入5 g预热不超过40℃的吐温80,混匀,再加入85 mL经过预热的pH为7.0的缓冲氯化钠-蛋白胨或磷酸盐缓冲液或TSB或LeB(对于化妆品或可能含有防腐剂的产品),完全混匀,再利用水浴锅保持不超过40℃的温度使其在最短时间内乳化。吸取1 mL上述样液(10-1的稀释液)至9 mL灭菌的同质稀释液中,制成10-2的稀释液,依此同样制成10-3,10-4……的稀释液。
第四,雾化形式的液体或固体样品的制备。通过无菌操作取10 g或10 mL样品,使用经灭菌处理的膜过滤装置进行过滤,制成样本,或无菌条件下将样品转移到无菌容器中,使用整个内容物或包装中的一定量样品进行取样,并进行测试。
第五,膜剂供试样品的制备。在无菌操作下取出供试样品,用无菌剪刀剪碎,再加入稀释剂(TSB),浸泡30 min,振荡摇匀,制成1∶10的样品供检样液。如果需要,可调节供检样液的pH至6~8。吸取1 mL上述样液(10-1的稀释液)至9 mL灭菌的同质稀释液中,制成10-2的稀释液,依此同样制成10-3,10-4……的稀释液。
1.5实验操作流程
(1)先用经灭菌处理的枪头吸取1∶10稀释的样品待检液体1 mL,将其加入一次性无菌塑料培养皿中,做2个平皿。然后,另外用一支无菌枪头吸取1 mL待检样液加入9 mL灭菌的同质稀释液体玻璃试管中(特别要注意不能使无菌枪头接触稀释液液面),再更换一支无菌枪头,使用漩涡振荡器将稀释样液充分混匀,便制成了1∶100的待检稀释液。采用同样的方法,用灭过菌的枪头吸取1∶10稀释的样品待检液体1 mL,将其加入一次性无菌塑料培养皿中,做2个平皿。如果待检样品污染严重,菌含量特别高,还需要用同样的方法再将其稀释成1∶1 000,1∶10 000,……等梯度的待检样液。另外,每做一次梯度稀释都要更换1支无菌枪头。
(2)待检样液制备完成后,将121℃条件下灭菌15 min后的胰酪大豆胨琼脂培养基(TSA)取出,放置在室温下,待冷却至45~50℃后,加入有待检样液的无菌培养皿内,且每个培养皿内都大约放有15~
20 mL的胰酪大豆胨琼脂培养基(TSA),随后缓慢转动平皿,勿使培养基外溢,将待检样品与胰酪大豆胨琼脂培养基充分混匀,静置等待胰酪大豆胨琼脂培养基凝固,再将培养皿翻转,倒置培养,于30~35℃生化培养箱中培养5 d。同时,需要设立一个空白对照组,即另外准备一个不加待检样品的无菌空平培养皿,同样在其中加入约15~20 mL胰酪大豆胨琼脂培养基(TSA),静置等待胰酪大豆胨琼脂凝固后,再将培养皿翻转过来,倒置培养,于30~35℃生化培养箱中培养5 d。
(3)培养结束后,对培养平皿进行计数。首先用肉眼观察培养平皿,打点记录需氧细菌总数,然后再将其放到点板计数器上,用放大镜检查并计数,避免遗漏导致结果数值偏小。将各培养平皿内的需氧细菌总数记录下来,然后求取其平均值。若有菌落呈片状蔓延生长,则该培养平皿不适宜用于点板计数。若其片状菌落现象没有达到培养平皿的一半,而其中需氧细菌总数生长分布状态很均匀且易于计数,那么就可以将此半个培养平皿菌落打点计数后再乘以2,以表示全培养平皿的需氧细菌总数。
1.6实验结果处理
(1)应选取需氧细菌总数为25~250 CFU且菌落无蔓延生长现象的平板进行计数。对于需氧细菌总数在25 CFU以下的平板,应记录其具体的需氧细菌总数;需氧细菌总数高于250 CFU的平板可记录为多不可记。每一个稀释梯度下都应采用两个计数平板的平均数作为需氧细菌总数。
(2)如果在适宜的计数范围内只有一个稀释梯度平板上的需氧细菌总数符合要求,那么就取其平均值乘以稀释倍数,作为需氧细菌总数。
(3)如果在适宜计数范围内有两个连续稀释度的平板需氧细菌总数符合,那么就按照以下公式计算需氧细菌总数。
N=ΣC/
式中:N为样品中需氧细菌总数;ΣC为各平板需氧细菌总数之和;n1为第一个适宜稀释度梯度的需氧细菌总数;n2为第二个适宜稀释度梯度的需氧细菌总数;d为第一稀释度梯度的稀释因子。
2不确定度来源识别
不确定度来源识别具体步骤如图1所示。
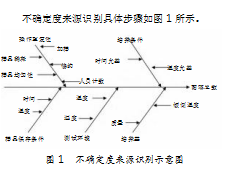
3不确定度评定
(1)本检测中不确定度的主要来源包括以下几方面:测试过程的重复性(如样品添加、样品梯度稀释,结果数值修约、样本本身的均匀性,人员的计数过程等)、平板的培养条件(如温度、湿度、时间等)、检测环境(如测试环境的温度、湿度等),以及测试工具(如生物安全柜、超净工作台、移液枪、电子天平等)。
经过分析,在化妆品需氧细菌总数的检测过程中,不确定度的来源可分为A类不确定度和B类不确定度。A类不确定度由样品本身微生物分布的均匀性及重复性检测过程导致。B类不确定度由检测程中所使用的设备产生。经过分析发现,B类不确定度分量对合成不确定度的影响较小,可以忽略不计。以重复检测造成的不确定度为主,因此,可采用统计学方法合并样品标准差(A类)来评定检测结果的不确定度。数学模型可表达如下。
Y=X
(2)在实验室内,由不同检验人员在同一检测环境下按照同一检测标准对同一批次制成的10个样品开展需氧细菌总数检测。具体参照USP 2022<61>中的“非无菌产品微生物限度检查”方法,采用微生物计数法进行检验。
选择合适的稀释度梯度,且每个稀释度梯度设置2块无菌平皿,在每平皿内加入1 mL待检稀释液。同时,设立空白对照平皿,将1 mL稀释液加入无菌平皿中。统计10组需氧细菌总数的检验数据,并分别取各组数据的常用对数值进行不确定度评定。
(3)本试验对10份乳液样品进行不确定度评定,样品经过TSB肉汤稀释,可以满足方法验证要求,以得到每个样品的需氧细菌总数。本实验样品由两人测量,每人测试一次,即得到两组数据。得到每个样品两次测量所得的需氧细菌总数,再采用合并样本方差进行计算,求出不确定度。
样本方差进行计算,求出不确定度。
①本实验总计测量10个待检样品,且每个样品由两个不同人员各测量一次,求出第j个样品的两次测量结果分别为x1j和x2j;
②对测量结果x1j和x2j取常用对数,得到lg x1j和lg x2j,求得两者的平均值为lg xj;
③每个样品分别求得10组数据,再对每一个试样分别进行残差平方和统计,公式如下。
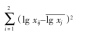
需氧细菌总数测试及统计计算结果如表1所示。
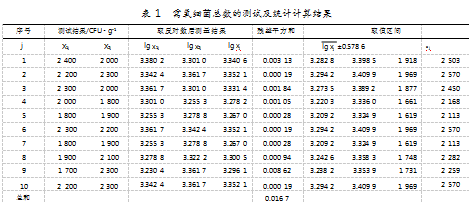
④分别求出两个样品结果的残差平方和,再统计10个测试样本的合并样本标准差,结果为:
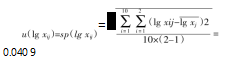
⑤在本次实验中,每个测试样品都经过了两次测试。因此,两次测试平均值的标准不确定度为:
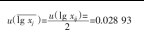
⑥当取包含因子为k=2.0时,可求出扩展不确定度为:U(lg xj)=k·u(lg xj)=2.0×0.028 93=0.057 86;
⑦以区间形式表示为:
lg xj-U(lg xj)≤lg xj≤lg xj+U(lg xj)
⑧最后,利用标准不确定度,计算数每个样品的需氧细菌总数的取值范围。根据每一个测试样品对数平均值的lg xj取值范围,利用反对数公式得到每个测试样品需氧细菌总数含量xj的所在区间。每个测试样品lg x的取值范围和取反对数结果如表1所示。
4结语
本文通过对平板计数法需氧细菌总数计数结果扩展不确定度的分析与计算,建立了化妆品中需氧细菌计数的测定方法。研究结果显示,标准不确定度为0.028 93,扩展不确定度为0.057 86,并根据以上结果出具了不确定度报告。本文通过探讨在测试中如何分析测试结果的误差来源,以及怎样计算化妆品定量检测中的扩展不确定度,为今后工作中扩展不确定度的评定提供了计算参考。
参考文献
[1]国家质量技术监督局.测量不确定度评定与表示:JJF1059-1999[S].北京:中国计量出版社,1999.
[2]郑萍,丁珵,武利平,等.化妆品菌落总数指标测量不确定度的评定[J].中国卫生检验杂志,2015,25(22):3866-3867,3874.
[3]杨兰花,卢力.化妆品微生物检验菌落总数不确定度评定[J].香料香精化妆品,2010(1):31-32,37.
[4]范媛媛,王树祥,朱宇旌.食品菌落总数检验中不确定度的评定[J].中国卫生检验杂志,2007(2):296-297.
[5]孟宪双,马强等.化妆品质量安全检测技术研究进展[J]分析测试学报,2016,35(2):143-155
[6]程凤.化学计量学方法在化妆品产品质量控制数据分析中的应用[D].上海:华东理工大学,2013.
[7]范红.化妆品微生物检测及质量控制分析[J].商品与质量,2019(2):126.










