基于营养琼脂培养基保温后浑浊问题与对策研究论文
2024-09-24 15:06:59 来源: 作者:liziwei
摘要:营养琼脂培养基在50℃条件下保温18 h后,会出现浑浊现象,给无菌判定带来困难,同时也会影响菌落计数等微生物实验的准确性。为查明营养琼脂培养基在保温后出现浑浊现象的原因,以提高涉及该培养基的所有实验的准确性,文章通过复融法、磷酸盐沉淀法和初始菌控制法对其原因进行研究分析。实验结果表明,导致营养琼脂培养基在保温过程中出现浑浊现象的主要原因是培养基中初始菌含量过高,在121℃灭菌15 min的条件下无法全部灭活。针对验收过程中出现的保温浑浊问题,可以采用辐照灭菌的方法,将培养基以15~18 kgy的剂量进行辐
摘要:营养琼脂培养基在50℃条件下保温18 h后,会出现浑浊现象,给无菌判定带来困难,同时也会影响菌落计数等微生物实验的准确性。为查明营养琼脂培养基在保温后出现浑浊现象的原因,以提高涉及该培养基的所有实验的准确性,文章通过复融法、磷酸盐沉淀法和初始菌控制法对其原因进行研究分析。实验结果表明,导致营养琼脂培养基在保温过程中出现浑浊现象的主要原因是培养基中初始菌含量过高,在121℃灭菌15 min的条件下无法全部灭活。针对验收过程中出现的保温浑浊问题,可以采用辐照灭菌的方法,将培养基以15~18 kgy的剂量进行辐照灭菌,降低初始菌含量,并在121℃的条件下灭菌15 min。
关键词:营养琼脂;复融法;磷酸盐沉淀法;初始菌控制法;保温;浑浊
营养琼脂培养基富含蛋白胨和牛肉浸粉等营养物质,能为微生物生长繁殖提供必需的营养物质和固体支撑,被广泛应用于微生物的计数、分离和鉴定环节。然而,在实际使用过程中,实验人员经常会遇到保温灭菌后培养基浑浊的现象,对实验进程和准确性造成不良影响。本文针对这一现象,采用复融法、磷酸盐沉淀法和初始菌控制法进行研究分析,找出其原因,并提出预防措施,以期提高实验准备的效率和准确性。
1材料与仪器
1.1材料
营养琼脂培养基、磷酸二氢钾(AR)、胰酪大豆胨琼脂培养基、沙氏葡萄糖琼脂培养基、1 000 mL蓝盖瓶。
1.2仪器
压力蒸汽灭菌器、超净工作台、生物安全柜、电热恒温培养箱、霉菌培养箱、电子天平、水浴锅。
2实验方法
2.1复融法
称取26.4 g营养琼脂加入100 mL蓝盖试剂瓶中,再加入800 mL去离子水,使其充分溶解,共配制12瓶试剂,121℃条件下灭菌15 min后,取出冷却至80℃,轻轻摇晃,使培养基溶液溶解均匀,然后静置于50℃水浴锅中保温。待溶液温度降至50℃,将其放入50℃电热恒温培养箱中进行保温试验18 h,然后将浑浊的培养基取出,放置在100℃水浴锅中保温30 min,保温结束后观察培养基能否恢复至澄清状。
2.2磷酸盐沉淀法
称取26.4 g营养琼脂和4 g磷酸氢二钾共同置于1 000 mL的蓝盖试剂瓶中,加入800 mL去离子水,使其充分溶解,共配制12瓶试剂,121℃条件下灭菌15 min,灭菌结束后,取出冷却至80℃,轻轻摇晃使培养基溶液溶解均匀,观察培养基是否呈澄清状。
2.3初始污染菌控制法
将250 g同批次营养琼脂培养基干粉装入尼龙袋中密封,送至辐照灭菌中心实施γ射线灭菌。将辐照灭菌和未辐照灭菌的营养琼脂培养基分为A组和B组,分别称取26.4 g营养琼脂加入1 000 mL蓝盖试剂瓶中,加入800 mL去离子水,使其充分溶解,共配制12瓶,121℃条件下灭菌15 min,灭菌结束后取出,在室温环境下冷却至80℃,轻轻摇晃,使培养基溶液溶解均匀,然后静置在50℃水浴锅中。待溶液温度降至50℃,将其放入50℃电热恒温培养箱中进行18 h的保温试验。18 h后将浑浊的培养基取出,轻轻摇晃,观察培养基是否呈澄清状。
同时,对保温18 h的培养基溶液进行无菌操作,分别从每瓶中抽取1 mL,通过点种法将其接种至胰酪大豆胨琼脂平皿上,每瓶平行接种到4块平皿上,2块平皿36±1℃培养,2块平皿50±1℃培养48±2 h;逐日观察平皿中菌落的生长情况。
3实验结果分析
3.1复融法结果分析
3.1.1营养琼脂分子构成
营养琼脂培养基中的凝固剂为琼脂。琼脂的主要成分是琼脂糖,是一种由1,3联结的D-半乳糖和1,4联结的3,6内醚-L-半乳糖交替重复接连而成的长链型高分子多糖。此外,琼脂中还含有不具备凝胶性的硫酸酯素,称为琼脂胶,是工业生产中需要去除的部分。琼脂糖是由D-半乳糖和3,6-脱水-L-半乳糖组成的直链,通过氢键相互作用形成双螺旋结构。每个结构单元都存在四个羟基,其中三个向外的羟基可以通过氢键与相邻的螺旋或溶剂结合,最后一个羟基则在螺旋内部通过氢键与螺旋内的水分子结合。
3.1.2琼脂溶液冷却后的持水性
其双螺旋结构形成三维网状凝胶结构,分散液体镶嵌在网状结构的空隙中,且部分水分-T-能与琼脂中的疏水主链通过氢键结合,形成琼脂聚合物。此外,随着琼脂质量分数的增加,凝胶中的水分流动性逐渐降低,即持水性越来越强。同时,随着琼脂质量分数的增加,琼脂溶液中双螺旋结构也会不断增加,分子间相互缠结形成的网络节点也在随之增加,三维网状凝胶结构的结合会更加紧密,与水相互结合的位点也会随之增加,因此,凝胶中水分流动性降低而溶液黏度增加,澄清度下降故而呈浑浊状态。
3.1.3琼脂复溶法结果分析
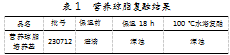
将培养基溶液复融,如果培养基的透明度恢复,便可说明浑浊现象是由琼脂在保温过程中黏度增加造成的。但进行复融之后发现,溶液依然呈浑浊状态(见表1、图1),由此可以判定,引起浑浊的原因并非保温过程中琼脂黏度的增加。

3.2磷酸盐沉淀法结果分析
相关研究表明,微生物培养要求所用的生化琼脂透明度良好。然而,在使用国产琼脂配置微生物培养基时,加入磷酸盐后经常会出现浑浊或沉淀现象,导致培养基透明度降低,会影响对微生物群落的观察及计数。部分学者认为,这是因为国产琼脂中含有Ca2+、Mg2+,这些离子在培养基的配制过程中会与磷酸盐反应生成不溶性沉淀,从而引起培养基浑浊度增加和透明度降低的“磷酸盐沉淀”现象。
尽管营养琼脂中的各成分经过磷酸盐沉淀检测均属合格,但仍无法排除原料中存在微量Ca2+、Mg2+。在多种原料混合后,培养基中Ca2+、Mg2+的整体含量可能会有所增加,在长时间的保温过程中,这些Ca2+、Mg2+会释放出来,并与溶液中的磷酸根离子结合,生成不溶性沉淀,从而造成培养基浑浊。
陈志林等发现在氯碱工业中加入磷酸盐,可以明显去除其中存在的Ca2+、Mg2+。按照琼脂磷酸盐沉淀检测方法,每100 mL培养基中加入0.50 g磷酸氢二钾并用磷酸溶液调节pH至7.0~7.5,121℃条件下灭菌15 min后进行透明度和浊度测定。
从实验结果可知,灭菌后,培养基未出现浑浊现象(见表2、图2),因此,可以排除培养基保温过程中的浑浊现象与Ca2+、Mg2+有关。


3.3初始污染菌控制结果分析
灭菌指在一定时间内通过高温或化学消毒等方法完全杀灭所有微生物(包括病菌、细菌等)的过程。在建立的灭菌剂量实验研究中,生物负载检测数据作为关键值,决定了产品最终灭菌剂量的结果。微生物负载量不同,就应选择不同的灭菌参数。
实验结果表明,营养琼脂干粉经辐照后,微生物负载量显著减少,保温过程中未出现浑浊现象,接种的平板上也未见菌落生长。相比之下,未经辐照灭菌的营养琼脂则在保温过程中出现了浑浊现象,并在50℃培养的平板上长出了菌落(见表3、图3~4)。由此可以判断,培养基在保温过程中出现的浑浊现象,是由于培养基初始含菌量过高,经121℃灭菌15 min后未被完全杀灭,导致保温过程中复苏和增殖所致的。



4营养琼脂培养基保温后浑浊问题的对策与解决方案
分析上述实验结果可知,培养基中初始菌含量较高且存在嗜热菌,按照常规灭菌方法(121℃、15 min)无法彻底灭菌。针对这一问题,可以从以下几方面入手加以解决。
增加初始菌含量检测,根据《食品微生物学检验培养基和试剂的质量要求》[13]在验收确认的基础上,增加对培养基初始菌含量的检测,确认其初始含菌量。从厂家处获取出厂时的初始含菌量;以3MTM压力蒸汽灭菌生物培养指示剂中含嗜热脂肪杆菌芽孢水平≥105 CFU/支为参考,当检测到初始含菌量≥105 CFU/g时需加以重视。根据厂家标注的培养基灭菌要求进行灭菌处理后,进行18 h的保温实验,通过观察透明度和在36℃与50℃条件下培养的菌落总数来评定灭菌效果。在所有验收参数全部合格后,该批培养基方可用于日常检测。
如果在保温实验中发现培养基出现浑浊,且培养基中初始污染菌含量超过121℃、15 min条件下的灭菌能力,则可对该培养基在15~18 kgy的辐照剂量范围内进行辐照灭菌。然后按照培养基要求的灭菌条件实施灭菌处理,并在50℃电热恒温培养箱中进行18 h的保温试验,确保无菌落生长和浑浊现象。同时,参照GB 4789.28-2013《食品微生物学检验培养基和试剂的质量要求》中的规定,对培养基进行pH变化的监测和促生长实验,确保培养基的pH无显著变化,促生长比PR≥0.7,且菌落直径与对照培养基相比无显著差异。
合理调整灭菌程序,科学制定验证方案并严格执行。当培养基初始菌含量过高时,通用灭菌器灭菌可能无法达到所需的等效灭菌时间值(F0)。因此,需要增加初始菌含量检测和18 h保温实验,以降低无效灭菌概率。如果灭菌失效,可还增加辐照程序,以确保实验的准确性。
5结论与建议
综上所述,培养基中不同初始污染菌所表现出来的耐受性各不相同。在灭菌工艺验证的生物学确认阶段,应根据测定的不同微生物初始污染值计算F0值,以确保灭菌的有效性。在灭菌工艺验证工程中,应考虑培养基中营养物质的耐受性差异,采用合适的灭菌工艺,保证营养水平充足。本研究有助于促进培养基生产企业针对培养基生物负载量开展质量标准工作,也能给使用单位提供更多验收方案的选择。
在进行培养基的灭菌验证时,前提是要确保高压灭菌锅性能良好。为避免灭菌锅性能造成的误差,建议在灭菌时使用化学灭菌指示胶带或生物灭菌指示剂,以确保灭菌锅灭菌程序的有效性。
针对营养琼脂培养基,设置标准灭菌条件121℃、15 min,需要对干粉培养基中的生物负载量进行测试和控制。尽管培养基制造厂家会对产品进行质量评估,但《食品微生物学检验培养基和试剂的质量要求》中的验证要求目前仅适用于即用型培养基。因此,实验室在收到培养基后,有必要对初始菌进行检测,并对灭菌后的琼脂进行保温实验,作为验收营养琼脂培养基的指标。
针对微生物负载过程中筛选出的耐热菌,应进行鉴定与保存,并建立菌种数据库。在后期的灭菌效果验证中,可以作为内控验证菌,来验证灭菌效果的可靠性。
参考文献
[1]SCIONTI G,MORAL M,TOLEDANO M,et al.Effect of the hydration on the biomechanical properties in a fibrin-agarose tissue-like model[J].Journal of Biomedical Materials Research Part A,2014,102:2573-2582.
[2]WANG L,SHEN Z,MU H,et al.Impact of alkali pretreatment onyield,physico-chemical and gelling properties of high quality agar from Gracilaria tenuistipitata[J].Food Hydrocolloids,2016,70:356-362.
[3]ARNOTT S,FULMER A,SCOTT W E,et al.The agarosedouble helix and its function in agarose gel structure[J].Journal of Molecular Biology,1974,90(2):269-284.
[4]LABROPOULOS K C,NIESZ D E,DANFORTH S C,et al.Dynamic rheology of agar gels;theory and experiments.Part I.Development of a rheological model[J].Carbohydrate Polymers,2002,50(4):393-406
[5]苏生显,许永安.红藻胶的理化特性及应用研究进展[J].现代农业科技,2013,(10):279-280+282.
[6]王璋,许时婴,汤坚.食品化学[M].北京:中国轻工业出版社,2011.
[7]XIA K,LIU X,ZHAO J,et al.The physicochemical property characterization of agar acetate[J].Carbohydrate Polymers,2014,110:32-37.
[8]KUMAR TRIVEDI M.Comparative physicochemical evaluation of biofield treated phosphate buffer saline and hanks balanced salt medium[J].American Journal of BioScience,2015,3(6):267.
[9]朱运恒,姜泽东,倪辉,等.高透明度琼脂的制备工艺研究[J].食品工业科技,2019,40(21):149-153,158.
[10]刘立行,刘丽君.琼脂中微量元素的测定—非完全消化-火焰原子吸收法[J].辽宁石油化工大学学报,2005,25(1):55-57.
[11]陈志林,卞屾,孙玉和,等.磷酸盐除钙镁盐水精制试运行总结[J].氯碱工业,2016,52(3):8-10,34.
[12]薛玲,林华,王辉.北京市医疗器械产品γ射线辐射灭菌调研[J].首都医药,2007,18:4-5.
[13]中华人民共和国国家卫生和计划生育委员会.食品安全国家标准食品微生物学检验培养基和试剂的质量要求:GB 4789.28-2013[S].北京:中国标准出版社,2013.










