玉屏风口服液黄芪甲苷含量测定前处理方法的优化论文
2025-04-22 11:38:12 来源: 作者:xujingjing
摘要:文章建立加热回流的前处理方法,对玉屏风口服液含量测定的前处理过程进行方法优化。采用高效液相色谱法(HPLC)测定,用蒸发光散射检测器(ELSD)作为检测器,以黄芪甲苷为指标,对加热回流法和有机溶剂萃取法进行了比对,以确定其含量。结果表明,加热回流法为更优的制备方法,黄芪甲苷在进样量为0.438 6~0.877 3μg之间表现出良好的线性和准确度,其相关系数r=1.000,回归方程为Y=1.809 2X+2.314 6,平均回收率为94.95%,RSD值为1.2%(n=13),符合方法建立的要求。建立的加热
摘要:文章建立加热回流的前处理方法,对玉屏风口服液含量测定的前处理过程进行方法优化。采用高效液相色谱法(HPLC)测定,用蒸发光散射检测器(ELSD)作为检测器,以黄芪甲苷为指标,对加热回流法和有机溶剂萃取法进行了比对,以确定其含量。结果表明,加热回流法为更优的制备方法,黄芪甲苷在进样量为0.438 6~0.877 3μg之间表现出良好的线性和准确度,其相关系数r=1.000,回归方程为Y=1.809 2X+2.314 6,平均回收率为94.95%,RSD值为1.2%(n=13),符合方法建立的要求。建立的加热回流前处理方法操作简便、有效成分损失小,数据准确性高、重现性好,可作为玉屏风口服液含量测定的方法,为黄芪甲苷制剂方法优化提供参考。
关键词:黄芪甲苷;玉屏风口服液;前处理方法
0引言
玉屏风为中医扶正固表的经典名方,出自元·朱丹溪的《丹溪心法》,其主要成分由黄芪、白术与防风配成,各有其用处;本方为治疗表虚自汗的常用方,其功能在于增强人体免疫力、巩固外围防御系统以防止流失过多水分及预防感冒等症状的发生,也就是通过提升患者的正气以防御外邪,适用于健康和亚健康人群[1]。黄芪为其关键组成部分,拥有补气升阳、利水消肿、生津养血和固表止汗等功效,为君药,其中黄芪甲苷是中药黄芪的主要成分之一,具备维护心脏健康、调整血糖水平、保持中枢神经系统稳定、抵抗自由基以及抑制癌症等多种强大的生物活性,因此评价玉屏风的一项重要指标为主要药效物质黄芪甲苷的含量[2-4]。玉屏风口服液收录在2020年版《中国药典》中,以黄芪甲苷单一成分作为质量控制指标,但该制剂含量测定供试品制备工艺复杂、耗时较长,需反复多次的萃取、洗涤以及转移操作,容易导致有效成分损失,可操作性和可重复性不佳。近年来,黄芪甲苷的提取方法涌现出不少的改进工艺,例如,采用双水相萃取技术分离纯化黄芪甲苷,该方法具有提取效率高、环境友好等优点;将超声波和微波辅助提取法相结合,通过优化提取条件显著提高黄芪甲苷的提取率。黄芪甲苷的提取方法和工艺主要分为热提法、超临界流体萃取法、发酵法,其纯化方法主要为大孔树脂吸附法、碱化处理法[5-6]。本文综合考虑方法是否得率高、操作简便、成本低等,根据文献调研[7-9]、《中国药典》中黄芪项下的黄芪甲苷含量测定方法以及本实验室前期制定方法的优化整合,创建加热回流法确定其含量,并对13个批次样品的质量一致性进行了评估,旨在为更加精确、便捷且合理控制评价此药品的品质提供指导性的参考信息。
1仪器与试药
1.1仪器
高效液相色谱仪(Agilent 1260 Infinity II,安捷伦科技(中国)有限公司);水浴锅(D2KW-D-2,北京市永光明医疗仪器厂);电子天平(XS205DU,瑞士梅特勒-托利多公司)。
1.2试药
黄芪甲苷对照品(中国食品药品检定研究院,批号110781-202219,纯度96.2%);玉屏风口服液(13个厂家,不同生产批号)均购自长沙市药店,如表1所示;色谱纯乙腈,超纯水,甲醇、浓氨、正丁醇等试剂均为分析纯(国药集团化学试剂有限公司)。

2方法和结果
2.1前处理方法比较、溶液和色谱条件
2.1.1加热回流法制备供试品溶液
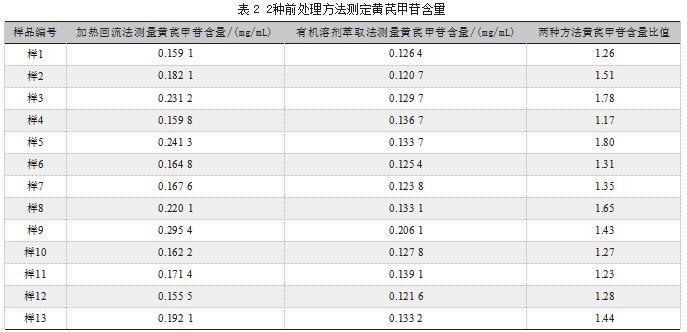
精密移取本品20 mL,置250 mL塞锥形瓶内,精密加入80%甲醇溶液50 mL,含4%浓氨试液,塞密,称重,摇匀,加热回流1 h。冷却(完全擦去锥形瓶外壁水)后称重,用80%甲醇溶液含4%浓氨试液补足减失重量,摇匀,过滤,弃去初滤液,精密移取续滤液20 mL置蒸发皿中,水浴蒸干后冷却,残渣先加少量80%甲醇溶解,然后用80%甲醇分多次少量清洗蒸发皿,并转移至25 mL量瓶中。最后用80%甲醇定容至刻度,摇匀,0.22μm滤膜过滤,弃去初滤液,取续滤液,即得。该法测定13批次玉屏风口服液中黄芪甲苷含量,如表2所示。
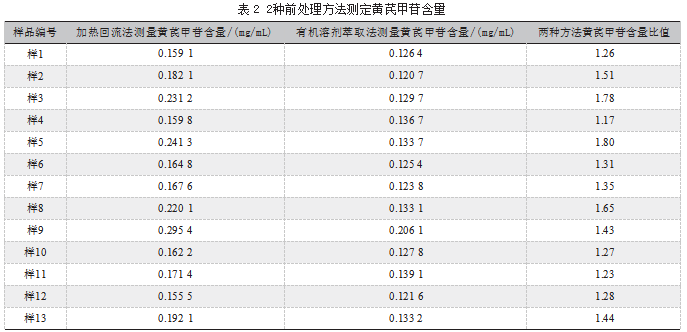
2.1.2有机溶剂萃取法制备供试品溶液
精密量取本品20 mL,置分液漏斗中,以水饱和正丁醇充分振摇提取5次,每次25 mL,每次振摇后应尽量使溶液完全分层。合并正丁醇萃取液后,完全转移正丁醇萃取液置分液漏斗中,用氨试液洗涤3次,每次20 mL,氨试液洗涤过程应尽可能长,保证杂质除去完全。用蒸发皿收集正丁醇萃取液,置水浴蒸干,残渣先加少量甲醇溶解,然后用甲醇多次少量清洗蒸发皿,并转移至20 mL量瓶中。最后用甲醇定容至刻度,摇匀离心,取上清液,0.22μm滤膜过滤,弃去初滤液,取续滤液,即得。该法测定13批次玉屏风口服液中黄芪甲苷含量如表2所示。
2.1.3对照品溶液制备
精密称取黄芪甲苷对照品0.011 40 g(纯度96.2%),置25 mL容量瓶中,加适量甲醇超声溶解,冷却后用甲醇稀释定容至刻度,摇匀,作为对照储备液(浓度约为0.4 mg/mL)。精密移取适量对照储备液置容量瓶中,加甲醇稀释并定容至刻度,摇匀即得(浓度约为0.04 mg/mL)。
2.1.4阴性对照溶液的制备
按2.1.1节前处理方法制备不含黄芪甲苷的阴性对照溶液,0.22μm滤膜过滤,取续滤液,即得。
2.1.5高效液相色谱(HPLC)-蒸发光散射检测器(ELSD)色谱条件
色谱柱为Waters sunfire C18(250 mm×4.6 mm,5μm);柱温为30℃;流动相为乙腈(35)∶水(65);流速为1.0 mL/min;检测器为ELSD(温度110℃);进样体积为10、20μL;进样次数为3次,以3次峰面积的平均值计算黄芪甲苷的含量;高效液相色谱仪为Agilent 1260 Infinity II。
2.2方法学考察
2.2.1专属性试验
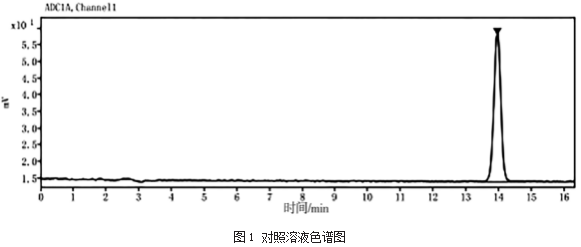
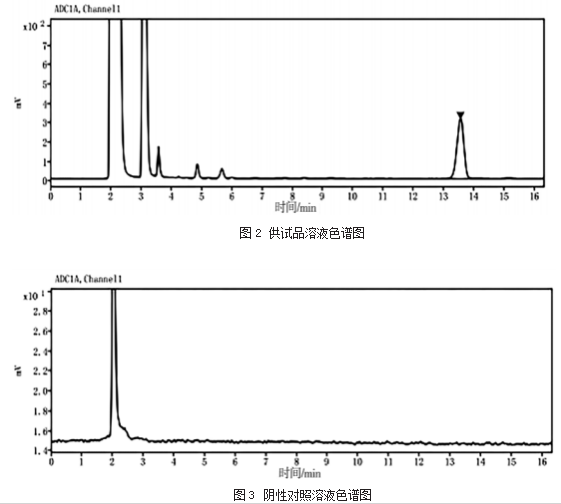
照2.1.5节所述色谱条件,自动进样器进样量为10μL,分别吸取阴性对照溶液、供试品溶液、对照品溶液,采集时间为30 min,得到3张色谱图,如图1~图3所示。供试品色谱图中,在黄芪甲苷对照品色谱图的对应位置上有相同保留时间(相对保留时间为13.505 min)的色谱峰,且在此出峰时间附近未见明显杂质峰,无杂质峰干扰。而阴性对照溶液色谱图在此保留时间不呈现黄芪甲苷的色谱峰,说明阴性对照溶液对此实验无干扰,专属性强。
2.2.2线性关系考察
取2.1.3节制备的对照品溶液,自动进样器进样量分别为10、20μL,注入液相色谱仪,进样次数为3次,测定。以进样量的对数为横坐标、峰面积的对数(3次测定的平均值)为纵坐标,以外标两点法计算其对数方程得到Y=1.809 2X+2.314 6。结果表明,黄芪甲苷在进样量为0.438 6~0.877 3μg范围内具有线性关系。
2.2.3精密度试验
取2.1.3节制备的对照品溶液,进样次数为6次,进样体积为10μL,对峰面积进行考察,面积分别为46.22、46.69、46.53、46.36、46.66、46.89,计算峰面积相对标准偏差(RSD)值为0.52%,表明仪器的精密度良好,符合试验要求。
2.2.4重复性试验
取同一批样品(1号),按2.1.1节的方法制备6份供试品溶液,按2.1.5节色谱条件分别测定其含量,结果为0.159 1、0.159 1、0.160 4、0.160 4、0.158 9、0.159 8 mg/mL,平均值为0.159 6 mg/mL,相对标准偏差(RSD)为0.43%,表明该方法重现性良好。
2.2.5稳定性考察
取2.2.4节供试品溶液(1号)先后于0、1、3、6、12、24 h按2.1.5节色谱条件测定黄芪甲苷的峰面积,分别为74.26、75.36、74.19、75.10、74.46、74.10,平均峰面积为74.57,RSD为0.71%,表明24 h内供试品溶液是稳定的。
2.2.6加标回收试验
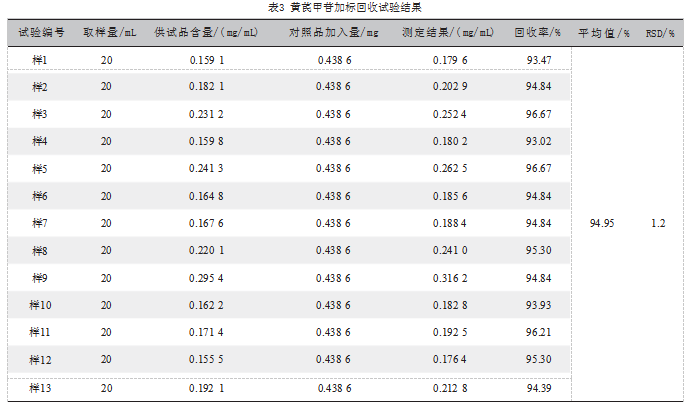
精密吸取13批样品20 mL,用移液器精密吸取一定量的黄芪甲苷对照品溶液(2.1.3节浓度约为0.4 mg/mL的对照品储备液)1 mL分别依次加入13份样品中,再按照2.1.1节加热回流法制备供试品溶液的处理方法进行制备,按2.1.5节色谱条件进行测定,计算得到黄芪甲苷加样回收率达到93.02%~96.67%,平均回收率为94.95%,RSD为1.2%,表明该方法回收率良好,能达到准确试验的要求,结果如表3所示。
2.3结果
采用加热回流法和有机溶剂萃取法,对13个批次的样品进行黄芪甲苷含量测定,结果表明,加热回流法黄芪甲苷含量明显高于有机溶剂萃取法。
3结语
经过对玉屏风口服液前处理方法比对试验,发现采用加热回流法提取黄芪甲苷操作更简单、时间短、提取率高,而有机溶剂萃取法过程繁琐、耗时长、损失量大,且含量处于标准要求的边缘值。另外,还考察了30、45、60、90、120 min不同加热回流时间对试验结果的影响,发现加热回流时间为60 min得到的黄芪甲苷含量最高,延长加热回流时间后黄芪甲苷含量无明显提高,故最终确定加热回流时间为60 min。同时还对少批量的玉屏风颗粒和玉屏风胶囊考察两种前处理的比对,结果同玉屏风口服液一致。综上所述,加热回流法更高效、准确、省时和简便,适用于玉屏风各制剂中有效成分黄芪甲苷的含量测定。
[1]国家药典委员会.中华人民共和国药典(一部2020年版)[S].北京:中国医药科技出版社,2020.
[2]赵小强,赵静,张浩波,等.黄芪甲苷的提取、分离、纯化及其药理作用的研究进展[J].华西药学杂志,2022,37(6):711-716.
[3]关静,黄凡克,周伊璐,等.黄芪甲苷抗心力衰竭患者缺血缺氧性心肌损伤的机制研究进展[J].实用心脑肺血管病杂志,2023,31(9):111-114.
[4]杨睿,樊海军,张伟.黄芪甲苷在多发性硬化症模型动物中的保护作用及机制研究[J].中国药师,2022,25(7):1138-1144.
[5]路立峰,沈伟.玉屏风方制剂质量控制的研究进展[J].中华中医药学刊,2020,38(11):62-66.
[6]陈勇,杨欢.黄芪甲苷在液体制剂中含量测定优化方法的探索[J].中国药物评价,2022,39(2):122-124.
[7]梁曜华,李春,冯伟红,等.连续单因素法优化黄芪中黄芪甲苷的含量测定方法[J].中国中药杂志,2021,46(2):391-397.
[8]刘和平,彭招华,张润容,等.黄芪药材中黄芪甲苷UPLC-ELSD含量测定方法的优化[J].中国实验方剂学杂志,2015,21(5):92-94.
[9]田洋.黄芪甲苷提取与纯化工艺研究进展[J].农业科技与装备,2015(10):42-43,46.










