骨形成相关基因及其遗传性疾病的研究进展论文
2024-05-23 09:25:57 来源: 作者:xuling
摘要:骨骼对人体具有重要意义,可发挥运动、保护和支撑等作用。骨的正常形成是一个复杂的过程,依赖于各种骨相关基因、转录因子和信号通路的参与和调控。因此,深入了解骨发育及其代谢等生理活动的分子机制至关重要。若发生基因突变导致调控异常,则可能发生遗传性骨病。因此,本文对骨形成的分子机制及遗传性骨病和相关基因进行综述,为骨相关疾病的诊断、治疗和预防提供更有效、更精确的策略。
[摘要]骨骼对人体具有重要意义,可发挥运动、保护和支撑等作用。骨的正常形成是一个复杂的过程,依赖于各种骨相关基因、转录因子和信号通路的参与和调控。因此,深入了解骨发育及其代谢等生理活动的分子机制至关重要。若发生基因突变导致调控异常,则可能发生遗传性骨病。因此,本文对骨形成的分子机制及遗传性骨病和相关基因进行综述,为骨相关疾病的诊断、治疗和预防提供更有效、更精确的策略。
[关键词]骨骼,骨形成,遗传性骨病,调控基因
Progress in the Study of Bone Formation-related Genes and Their Inher⁃ited Diseases
CHEN Xinyi1,DENG Yekun2,ZHANG Jingchen2
1.Department of Stomatology,Soochow University,Suzhou,Jiangsu Province,215006 China;2.Department of Orthope⁃dics,the Second Affiliated Hospital of Soochow University,Suzhou,Jiangsu Province,215006 China
[Abstract]Bone is important to the human body,playing the roles of movement,protection and support.Normal bone formation is a complex process that depends on the participation and regulation of various bone-related genes,tran⁃scription factors and signaling pathways.Therefore,it is crucial to gain a deeper understanding of the molecular mechanisms underlying physiological activities such as bone development and its metabolism.Inherited bone diseases may occur if mutations in the genes lead to abnormal regulation.Therefore,this paper provides an overview of the mo⁃lecular mechanisms of bone formation and hereditary bone diseases and related genes,in order to provide a more effec⁃tive and precise strategy for the diagnosis,treatment and prevention of bone-related diseases.
[Key words]Bone;Bone formation;Hereditary bone diseases;Regulatory genes
人体的骨骼有多种功能,在起到支撑人体作用的同时,也保护重要脏器并支持人体的运动。骨骼的发育和形成是由干细胞分化、成骨细胞和软骨细胞增殖等一系列过程逐步形成的,并受到多种基因、转录因子和信号通路的调控。然而,在骨的发育和生长过程中,由于遗传物质的异变,会导致人体骨骼出现一系列病变与异常,即发生遗传性骨病(Genetic Skeletal Disorders,GSD)。由于任何一个因素的变化都可能致使骨骼发育异常或产生骨骼疾病,所以理清调控骨骼形成和生长的分子机制,对于骨病的预防、诊断和治疗具有重要的意义。
1调控骨形成的重要基因或转录因子
骨骼在成骨细胞和破骨细胞的介导下,处于动态的成骨和破骨平衡中。成骨细胞作为骨的功能细胞,合成骨基质并调节其矿化。破骨细胞可以吸收完全矿化的骨,介导骨破坏过程。骨骼损伤后,其重塑和改建对人体骨骼有重要意义。因此,梳理总结影响骨细胞的分化、骨矿化和骨重塑的相关基因和转录因子十分关键。
1.1与成骨细胞分化和形成相关的基因
RUNX2(Runt-Related Transcription Factor 2,RUNX2)为RUNT相关转录因子2,是成骨细胞分化最上游的转录因子,通过特异性结合DNA的Runt结构域调控基因的转录[1],在骨形成过程中对间充质干细胞向软骨细胞和成骨细胞分化起着重要作用。
Osterix基因即成骨相关转录因子,也被称为Sp7。Sp7在骨形成中是必需的,在成骨细胞的成熟、分化中起着一系列调控作用。Sp7作用于RUNX2的下游,调控I型胶原、骨钙蛋白、骨涎蛋白、骨桥素、骨唾液酸蛋白(Bone Sialoprotein,BSP)等表达。Sp7还上调各种成软骨因子来促进软骨细胞的分化。Sp7与成骨不全和骨质疏松也有显著关联,Sp7基因突变的患者常出现骨折易发生、骨骼畸形、牙齿发育延迟等成骨不全症的特征[2]。
BMP2(Bone Morphogenetic Protein 2,BMP2)是骨形态发生蛋白,又称为“成骨素”,是TGF-β超家族BMP亚家族的重要成员,在调控骨骼的发育与形成中起着关键作用,拥有增强间充质干细胞向软骨细胞和成骨细胞分化的能力,促进成骨细胞分化成熟。BMP2还参与骨和软骨的生长发育及其重建过程,加速骨缺损修复。在骨形成早期,BMP2可上调其受体的表达,增强骨髓基质细胞的成骨分化,促进骨基质的矿化[3]。
胰岛素样生长因子1(Insulin-like Growth Fac⁃tors-1,IGF1)是促进骨的发育、保持骨正常结构的重要的生长因子,可保持骨的正常合成代谢,增强骨密度,促进成骨细胞的增殖、分化以及基质形成,同时增强骨髓基质细胞内碱性磷酸酶的活性,上调骨钙素分泌和骨胶原合成[4]。IGF1还有助于软骨生长,促进软骨细胞增殖,合成软骨基质。
BMAL1基因是调控人体昼夜节律的生物钟基因的重要成员,对胚胎时期和出生后发育有至关重要的作用。BMAL1也参与调节软骨细胞、成骨细胞和破骨细胞分化。BMAL1调控骨的形成机制与多种基因和信号通路有关,例如通过调控RUNX2以间接地调节骨细胞分化[5]。
SOX9[SRY(性别决定区Y)9]在性别调控方面起关键作用,同时也在软骨发育和软骨内成骨上起重要的调控作用[6]。SOX9可以激活Col2α1、SOX5或SOX6的表达,这对软骨的分化起到一定作用。SOX9可通过对RUNX2进行负调控以抑制软骨细胞的成骨进程。
激活转录因子4(Activating Transcription Factor 4,ATF4)在成骨细胞表达、分化和功能中具有不可或缺的价值。ATF4缺乏可延缓发育期间的骨形成。ATF4突变还可导致Coffin-Lowry综合征和I型神经纤维瘤病的骨量减少[7]。ATF4缺失的成骨细胞中,BSP和骨钙素表达也存在明显降低。
1.2调控骨矿化相关的基因
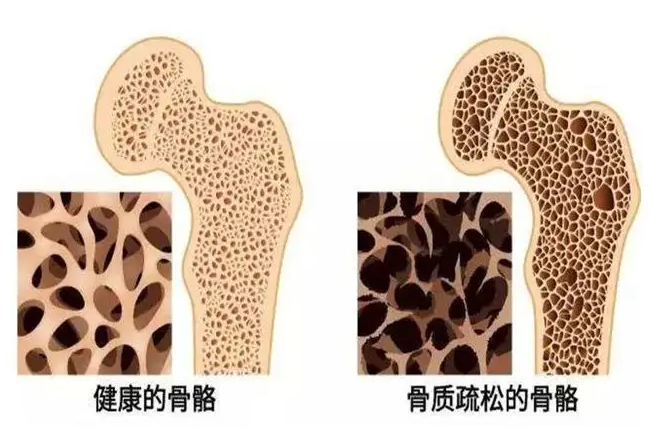
BSP是细胞外基质中的一种阴离子磷蛋白,在矿化组织中高度表达,成骨细胞、破骨细胞以及其他骨相关细胞中都可分泌BSP。因此,BSP基因表达的调控不仅影响各种骨相关细胞的分化,也与骨基质的矿化密切相关。当成骨细胞中BSP缺失,成骨细胞功能减退,骨密度降低,骨矿化减少,骨修复出现延迟,还可导致骨质疏松。此外,血清BSP浓度可反映破骨细胞活性和骨吸收过程。如果血清BSP水平明显升高,需要警惕一些骨代谢性疾病的发生,如多发性骨髓瘤、无症状或良性的甲状旁腺机能亢进症、Paget病等[8]。
LIM矿化蛋白-1(LIM Mineralization Protein-1,LMP-1)一般在骨骼中表达,能够促进骨骼的矿化,在成骨细胞分化中也起着正调节作用,还有助于成骨细胞骨钙素的分泌,形成骨结节[9]。
RNA腺苷脱氨酶1(Adenosine Deaminase Acting on RNA,ADAR1)的功能为维持骨形成和骨吸收的平衡以控制骨量的适当与正常。ADAR1功能受损主要抑制成骨细胞的分化,但不影响破骨细胞的形成,所以其导致的骨量减少原因主要成骨细胞的功能损害。
尼尔样-1型分子(Nel-Like Molecule-1,NELL1)是一种分泌蛋白,其在骨骼发育中的作用主要有诱导骨和软骨再生、促进骨细胞分化和骨形成。NELL1基因的缺失和过表达均会引起骨骼发育和形成的异常。NELL1也参与牙齿形成和矿化,包括促进成釉细胞和成牙本质细胞分化、细胞外基质和磨牙牙冠釉质矿化以及牙根形成[10]。
1.3调控骨损伤修复的基因
骨折指由于机械力和骨骼疾病等因素所致的骨的连续性和完整性中断,在破坏骨骼正常结构的同时,也可使骨内的血管等组织发生损伤。在骨骼损伤后愈合过程中,血管破坏后可创造局部缺氧环境,此时,缺氧诱导因子1(Hypoxia Inducible Factor 1,HIF1)可以被激活。HIF1调节细胞对缺氧发生的反应,具有促进骨骼愈合、血管生成的功能。HIF1主要在骨损伤后的血管形成中发挥作用,促进骨损伤后愈合。
降钙素相关肽基因(Calcitonin Gene Related Peptide,CGRP)主要分布于中枢神经和外周神经。
在骨组织损伤后愈合过程中,骨膜和骨组织中的神经纤维CGRP表达增加,调节骨的代谢[11]。骨折修复时,随着血液中CGRP浓度增加,表达CGRP的神经纤维数量也增加,逐渐出现新生纤维和分支,骨折2周后的骨痂从纤维性和软骨性向骨性转变。总之,CGRP基因促进细胞的成骨分化,抑制骨的吸收,对于骨折后修复具有积极意义。
C型利钠肽(C-type Natriuretic Peptide,CNP)是来自尿钠肽家族的多肽类物质,主要由血管内皮细胞分泌产生,可作用于血管使血管扩张。它不仅在大脑、心脏和肾脏等组织中均有表达并发挥功能,还能促进软骨内成骨和骨折修复。
2常见骨形成相关的遗传性疾病
2.1软骨发育异常
软骨发育不全(Achondroplasia,ACH)是一种常染色体显性遗传病,也是最常见的遗传性骨病之一。患者的临床症状为骨发育不良引起不匀称的身材矮小,四肢畸形,与躯干比例失衡。头面部也呈异常改变,如出现前额突出、面中部发育不良、鼻塌和鼻前倾等畸形变化。该病患者的肌肉和关节也有不同程度的异常改变,如出现四肢长骨缩短、肘关节活动受限、髋关节异常活动、膝内翻等,婴儿期表现为运动发育迟缓、肌张力不足。除了骨骼相关的症状外,患者还会出现其他并发症,例如错颌畸形、肥胖、心血管问题、低氧血症、听力受损和寿命减少等[12]。
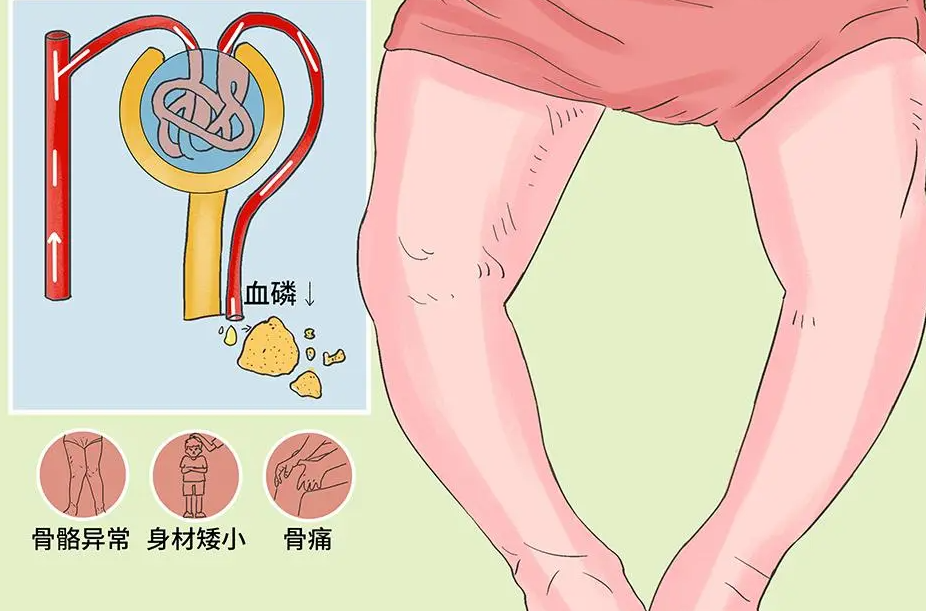
研究发现,ACH的主要致病基因为成纤维细胞生长因子受体3(Fibroblast Growth Factor Receptor 3,FGFR3)[13]。FGFR3编码成纤维生长因子受体3,当基因发生各种错义突变时,编码蛋白功能缺失,已经报道的致病性突变包括c.1138G>A,导致p.Gly380Arg;c.1138G>C,导致p.Gly380Arg,均为第380个氨基酸的错义突变,其中绝大多数患者表现为p.Gly380Arg突变[13]。同时,软骨发育低下与软骨发育不全相似,也与FGFR3基因突变相关,突变类型为c.1620C>A或c.1620C>G,导致第540个氨基酸错义突变(p.Asn540Lys)。其临床症状的严重程度比软骨发育不全轻,如颅面骨异常更加少见,四肢、手指畸形的程度也相对较轻[14]。
2.2成骨不全
成骨不全症(Osteogenesis Imperfecta,OI)为一种结缔组织病,对骨骼的影响主要表现为出现骨密度低、骨骼畸形、骨骼脆性增加和易骨折等现象,因此也称为脆骨病。OI最初被分为4种类型,目前则被分为15种,其临床表现复杂,异质性显著,其中Ⅱ型最严重,甚至可致死;Ⅰ型最轻,在身体形态上无明显异样[15]。
大多OI为常染色体显性遗传,也有部分为常染色体隐性遗传或X染色体连锁的遗传。有报道称IFITM5基因的5’非翻译区c.-14C>T杂合突变也可导致常染色体显性OI,本基因可影响骨的矿化。此外,常染色体隐性遗传型OI较罕见,并与Ⅰ型胶原蛋白合成和翻译后表达的基因相关。胶原蛋白的伴侣分子基因HSP47、FKBP65和BiP突变,以及与成骨细胞特异性转录因子SP7和与阳离子通道相关的TMEM38B[15]突变也可以引发常染色体隐性型OI。X染色体连锁的OI报道较少,PLS-3(Plastin 3)基因突变为此种类型[16]。
2.3其他骨骼发育不良
除了以上提到的遗传性骨病,还有很多其他典型的遗传性骨病,如假性软骨发育不全(Peseudoa⁃chondroplasia,PSACH)。PSACH是一种常染色体显性遗传病,患者有身材矮小、骨骼发育异常等特点。据报道,其致病基因为软骨寡聚蛋白基因(Cartilage Oligomeric Protein,COMP)[17]。
点状软骨发育不良(Chondrodysplasia Punctata,CDP)也称为先天性点状软骨发育不良、先天性钙化性灌入发育不良等。常出现鼻骨发育不良、点状钙化等症状,有时还存在身高较矮,病理特征为软骨的钙盐异常沉积。该疾病有多种类型,对应的致病基因也不同。X染色体隐性遗传的CDPX1型由基硫酸酯酶E(Aryl-Sulfatase E,ARSE)基因突变或该基因所在的X染色体短臂缺失或重排造成,主要为错义突变。X染色体显性遗传的CDPX2型Emo⁃pamil结合蛋白基因突变所致[18]。
3展望
骨骼的正常发育和维持对人体健康和正常活动都至关重要,对骨形成调控机制的研究有助于加深对骨形成和骨相关疾病病因的理解,并为骨组织疾病的诊断、治疗和预防提供更加有效的方法。此外,结合基因编辑和高通量筛选等技术手段,有利于研究关键调控基因和分子,并且在多种技术与方法的帮助下,通过药物开发、基因编辑治疗、干细胞治疗等方法实现更多骨相关疾病的治疗。目前,针对骨疾病的治疗主要包括手术、药物和生物治疗等。许多遗传性骨病通过外科手术的方式进行治疗,从而改善患者病情、提高生活质量。手术治疗的手段包括矫正畸形、固定、植入和延长骨骼等,辅以适当的康复训练,可以有效缓解患者的痛苦。同时,药物治疗也对部分骨病患者有效,如双膦酸盐有影响破骨细胞功能的作用,可以抑制骨吸收,因此对OI患者安全有效。基因治疗的目的是从根源上治疗遗传性骨病,消除缺陷基因及其表达产物对机体的不良影响,但基因治疗还有许多安全问题需要考虑和解决。这些治疗方法应结合患者的具体情况和疾病特点来选择,从而进行个体化治疗,力求达到最佳的治疗效果。骨组织生物学和骨疾病治疗的实际应用也十分重要,包括使用新的治疗方法和技术,针对不同患者的不同病情实现个体化治疗。
[参考文献]
[1]Komori T.Roles of Runx2 in Skeletal Development[J].Adv Exp Med Biol,2017,962:83-93.
[2]Ludwig K,Ward LM,Khan N,et al.Dominant osteogen⁃esis imperfecta with low bone turnover caused by a het⁃erozygous SP7 variant[J].Bone,2022,160:116400.
[3]冯少龙,陈泽驹,刘桂宏,等.骨形态发生蛋白在骨科领域的研究进展[J].中国医药生物技术,2023,18(3):241-246.
[4]Wang J,Zhu Q,Cao D,et al.Bone marrow-derived IGF-1 orchestrates maintenance and regeneration of the adult skeleton[J].Proc Natl Acad Sci USA,2023,120(1):e2203779120.
[5]余明芳,刘旭光,吴晓.生物钟基因Bmal1与骨代谢相关性的研究进展[J].实用医学杂志,2020,36(20):2881-2884.
[6]杨爽,闫景龙.软骨细胞分化过程中SOX9的作用[J].中国组织工程研究,2022,26(14):2279-2284.
[7]Feng Y,Han Z,Jiang W,et al.Promotion of osteogenesis in BMSC under hypoxia by ATF4 via the PERK-eIF2αsignaling pathway[J].In Vitro Cell Dev Biol Anim,2022,58(10):886-897.
[8]曾俊铭,贺小宁.骨涎蛋白在破骨细胞分化和骨吸收中的研究进展[J].海南医学院学报,2023,29(18):1425-1429.
[9]Mu R,Chen B,Bi B,et al.LIM Mineralization Protein-1 Enhances the Committed Differentiation of Dental Pulp Stem Cells through the ERK1/2 and p38 MAPK Path⁃ways and BMP Signaling[J].Int J Med Sci,2022,19(8):1307-1319.
[10]Liu Y,Ju M,Wang Z,et al.The synergistic effect of NELL1 and adipose-derived stem cells on promoting bone formation in osteogenesis imperfecta treatment[J].Biomed Pharmacother,2020,128:110235.
[11]程亮,朱良宇,何涛.重型创伤性脑损伤合并骨折患者血清CGRP的水平及与预后的关系[J/CD].中华老年骨科与康复电子杂志,2020,6(6):327-333.
[12]Pauli RM.Achondroplasia:a comprehensive clinical re⁃view[J].Orphanet J Rare Dis,2019,14(1):1.
[13]代伟倩,顾学范.中国210例软骨发育不全患儿临床遗传特征分析及生长发育曲线探索[J].中华儿科杂志,2020,58(6):7.
[14]赵星星,曾婷,郭毅,等.成纤维细胞生长因子受体3基因突变致软骨发育低下5例的临床特点及基因分析[J].山西医药杂志,2020,49(23):3246-3247.
[15]Botor M,Fus-Kujawa A,Uroczynska M,et al.Osteogen⁃esis Imperfecta:Current and Prospective Therapies[J].Biomolecules,2021,11(10):1493.
[16]Hu J,Li LJ,Zheng WB,et al.A novel mutation in PLS3 causes extremely rare X-linked osteogenesis im⁃perfecta[J].Mol Genet Genomic Med,2020,8(12):e1525.
[17]刘蕊蕊,马士凤,刘笑孝,等.1例COMP基因突变所致假性软骨发育不全病例报告[J].天津医科大学学报,2022,28(5):555-559.
[18]成胜权.儿童常见遗传性骨病的临床及分子遗传学研究[J].中国儿童保健杂志,2022,30(9):933-940.










