3D打印技术在四肢长骨骨肿瘤切除后大节段骨缺损的重建优势论文
2024-03-31 18:09:01 来源: 作者:heting
摘要:原发性骨肿瘤临床较为罕见,其中手术切除为其主要治疗手段,但四肢长骨骨肿瘤切除后骨缺损重建是患者保肢手术治疗过程中所面临的难题。传统自体骨与同种异体骨移植、骨诱导膜技术等存在不能及早负重、效果不理想等缺点。近年来,随着计算机技术和影像学技术的迅速发展,3D打印技术已逐步应用骨科手术中,也可为四肢长骨骨肿瘤切除后骨缺损重建提供新的治疗思路。本文通过分析解读相关的临床报道与临床经验,系统地定义长骨骨缺损的不同程度,阐述3D打印技术的微观设计与临床应用,体现其较所有重建方法在长骨骨肿瘤切除后大节段或极限骨缺损重建
【摘要】原发性骨肿瘤临床较为罕见,其中手术切除为其主要治疗手段,但四肢长骨骨肿瘤切除后骨缺损重建是患者保肢手术治疗过程中所面临的难题。传统自体骨与同种异体骨移植、骨诱导膜技术等存在不能及早负重、效果不理想等缺点。近年来,随着计算机技术和影像学技术的迅速发展,3D打印技术已逐步应用骨科手术中,也可为四肢长骨骨肿瘤切除后骨缺损重建提供新的治疗思路。本文通过分析解读相关的临床报道与临床经验,系统地定义长骨骨缺损的不同程度,阐述3D打印技术的微观设计与临床应用,体现其较所有重建方法在长骨骨肿瘤切除后大节段或极限骨缺损重建中的优势,并通过目前假体材料的发现与尝试的相关临床研究,结合3D打印技术,提出复合材料用于骨肿瘤切除后大段骨缺损的重建治疗的可行性。
【关键词】骨肿瘤,大段骨缺损,3D打印,缺损重建
骨原发性恶性肿瘤指的是发生于骨骼或其附属组织的肿瘤,常发生于四肢、盆骨、脊柱等部位,因其具有较高的侵袭性,常累及骨与周围软组织,且亚型复杂繁多,故治疗过程复杂漫长,且其在临床较为罕见。20世纪中下叶,针对病发于四肢长骨的原发性恶性肿瘤,多用截肢作为外科治疗方法[1]。随着新辅助化疗、放疗技术、精准诊断技术的发展与临床普及,逐渐应用于骨原发性恶性肿瘤的诊断和治疗中,为保肢手术的开展奠定了基础,目前瘤段切除与肢体重建的保肢手术取代了传统的截肢术。保肢手术指肢体长骨恶性骨肿瘤广泛切除后,经过重建技术恢复骨与关节功能的外科操作。术前新辅助化疗能够不同程度地灭活瘤变骨,控制原发灶,在消灭骨室中存在的跳跃灶的同时,也可尽早杀灭远处微小转移灶,缩小肿瘤及周围炎性水肿反应区,利于后续的保肢手术,进而保证了患者的功能活动与生活质量[2]。瘤段切除是骨肿瘤的标准治疗方法之一,重建肿瘤切除后的骨缺损尤为重要,其重建效果决定着肢体功能,然而肿瘤切除后骨缺损的重建面临着诸多挑战。骨缺损指因创伤、感染、生长异常及肿瘤等因素导致骨组织的缺失,常用重建方法有自体骨与同种异体骨移植,瘤体灭活再植,骨搬运,骨诱导膜技术以及髓内钉联合骨移植技术等,这些重建方法具有良好的骨诱导作用,可以基本满足生物重建,但这些重建方法或多或少都有其不足,如手术复杂,早期强度不能保证,大段异体骨移植存在感染、骨延迟愈合风险,瘤骨灭活再植的适应证有限,灭活的可靠性尚无标准,供体多次手术及移植材料有限等问题[3-4]。由于骨肿瘤具有异质性,不同患者骨缺损形态不一,个体差异较大,不同程度的骨缺损的重建方法、难度及预后存在较大区别。目前尚无文献明确提出不同骨缺损的具体概念及量化标准,对于某些骨原发性恶性肿瘤引起的大段或极限骨缺损,不论是自体骨移植或其他常规方法,都难以满足骨重建的需求。
随着3D打印工程的发展及其基础研究的不断深入,运用3D打印技术制备的复合材料具有可靠的生物相容性,可以实现临床个体化治疗原则,并迅速应用在脊柱、肿瘤、创伤手术中。3D打印技术是一类通过数字化控制逐层构建预定性状零件的制造方法的总称,其可能会为骨整合提供更好的解决方案,制造一个多孔的金属表面,允许骨骼生长,3D打印技术似乎是替代同种异体移植物重建的一种很有前途的方法,不仅有助于患者早期进行功能锻炼,还能减少与同种异体移植相关的并发症。基于此,本研究通过对3D打印技术应用于大段骨缺损的可行性进行综述,为临床骨重建方案的选择提供参考。
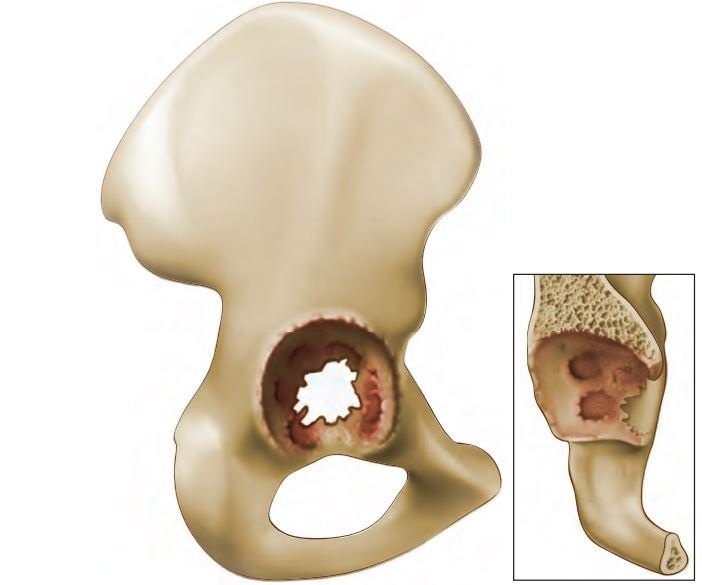
1长骨骨缺损的定义
骨代谢活动是一个骨吸收与骨重建的动态平衡,在这个过程中破骨细胞去除矿化的骨骼,而成骨细胞则会形成新的骨骼。因感染、创伤及部分骨良性肿瘤导致的骨缺损,往往因其缺损程度不大,可有一定的自愈性,采用自体骨及同种异体骨去弥补,即可很好地完成骨缺损的重建[5]。
但大部分骨原发性恶性肿瘤,因为肿瘤的切缘阴性“R0”切除原则,常常会引起大段的骨缺损。有临床研究提出,将缺损程度超过长骨干直径的1.5倍骨缺损定义为临界骨缺损[6]。一旦超过这个范围,则缺损往往不能自发愈合,常常需要移植物来诱导骨长入,重建局部的结构支撑及功能重建。又有动物实验于家兔尺骨干建立不同节段骨缺损,提示1.6 cm可作为其临界骨缺损,也可视作其接近长骨直径的1.5倍是处于临界的骨缺损[7]。针对于临界骨缺损,就需要常规自体骨或同种异体骨移植来进行重建。通常将骨缺损长度>4 cm的骨缺损称为大段骨缺损,有临床报道指出,针对4 cm以上的骨缺损,采用单纯的松质骨游离移植难以满足重建的需求[8-9]。而自体骨移植的骨量无法满足大于10 cm的骨缺损。因此,临床认为,针对于缺损长度介于4~10 cm的四肢长骨骨缺损,采用带血管蒂腓骨移植、诱导膜技术、骨搬运等方法基本可以满足重建需求[10]。大于10 cm的缺损则视作大节段骨缺损,对于大节段骨缺损,或许可以考虑采用自体带血管腓骨移植,骨搬运,骨诱导膜技术等方法,来尝试进行缺损重建,但仍需考虑感染、骨折等相关并发症[11-12]。有临床研究提出,将缺损长度>60%长骨的缺损,视为超临界骨缺损,或可将其称为极限骨缺损[13]。当瘤变临近或侵及骨骺,则势必需要考虑是否保留骨骺。若瘤变距骨骺大于1 cm,则可以在足量化疗或大剂量化疗前提下,尝试保留骨骺[14]。但针对于仅保留关节囊周围骨或仅保留生长板,骨骺或一侧骨端的情况,其缺损的重建与残端的固定稳定必然会变得困难。若瘤变侵及骨骺则不能保留骨骺或骨面,可行3D打印半关节假体以重建,但不能保证关节退变的进展。而某些骨肿瘤患者,其瘤变长骨会存在多处跳跃灶,则势必不能保留整个长骨。就以上几种仅保留些许骨质和不能保留一侧病变长骨的情况,其缺损长度必然超过了90%长骨,是需要在极限骨缺损的范围中另行考虑,可以将其定义为超极限骨缺损。对于极限与超极限骨缺损的重建,不论是自体骨搬运或自体腓骨移植,都难以满足缺损重建与残端的固定,而运用3D打印移植物或可满足重建需求[15]。
2 3D打印在大节段骨缺损重建的探索
骨原发性恶性肿瘤的治疗周期漫长,术中大节段骨缺损与某些极限骨缺损重建是亟需解决的难题。常规的骨缺损重建方法,或多或少都有其不足,3D打印技术则可及时准确地定制符合原始解剖的假体,并通过设计术区的模型与导板,减少术中的误差。其不同于传统假体,可以很好地在微观层次上控制适宜孔径与孔隙率,为残端骨细胞长入提供合适的环境,满足缺损重建的生物稳定,体现了其个性化的长处。
2.1 3D打印在重建骨缺损的微观设计
骨原发恶性肿瘤,尤其是膝关节周围的骨肿瘤,完整的切除及术后缺损的重建,需要用具有一定结构支持与足够的机械应力强度的骨诱导移植物来弥补。随着影像学及相关生物制作技术的不断改进,3D打印技术在临床中逐渐普及。根据术前病变CT,可完美地在三维结构上呈现瘤体毗邻的解剖关系,从而快速准确定制符合术式需求的模型与假体。根据wolff定律可知,骨的生长与骨动态平衡的维持需要一定的应力刺激,3D打印技术可在微观结构截骨接触面上控制适宜的孔径与孔隙率,控制适宜的应力强度,有效地刺激骨长入,也有利于细胞的渗透及物质交换,为骨长入提供条件。有实验证明,500~600μm的孔径及60%~70%的孔隙率的设计,符合人体松质骨的孔径与孔隙率,基本可以满足骨细胞良好的长入及在早期形成稳定的接触面[16-17]。骨原发性恶性肿瘤的骨重建往往是通过膜内成骨的途径来实现,不同于软骨内成骨,膜内成骨途径的骨重建往往对血管有很大的依赖。针对于瘤体切除后截骨面的残留骨细胞,若能为其提供血管的支持,确保氧气的获得,则更有利于其骨长入的生长。而3D打印技术去控制适宜孔径的同时,也可在微观结构上模拟微孔结构并可满足彼此相通的多孔,既有利于微血管的新生,也可避免接触骨面产生积液,为接触骨面的长入实现生物重建[18-19]。相较于传统的假体,3D打印技术可通过不同接触面的设计及形状的个性化设计,来控制其质量,在接触骨面和不必要的减重区采用多孔设计,促进骨长入,在软组织接触面采用非孔设计,保持一定的实心结构,为移植物提供一定的强度。个性化的定制设计,可以有选择性地定制假体形态,可以在满足力学的要求下,设计带弧形的管道,有利于缝线的进出,为局部结构的牢固提供帮助,特别是膝关节等较复杂的解剖结构,单纯的假体贴合和螺钉的固定,在早期未完美骨融合时还无法保证完全的稳定。而个性设计的管道设计可以将周围软组织紧密覆盖于假体,在保证假体软组织覆盖充分的同时,又为接触骨面的贴合提供又一助力。3D打印技术在微观结构上可以更大程度地满足接触骨面的长入,对于四肢瘤体切除的大段甚至是极限骨缺损的重建具有较大的可行性。
2.2 3D打印假体组成材料的发现与尝试
目前临床生物重建大多采用钛合金材料,因其具备良好生物诱导性,在骨肿瘤缺损的重建中也是首要选择。钛合金虽然有较高的力学强度与抗疲劳特性,但其耐腐蚀性较差,随着移植时间延长,不可避免地释放金属离子对周围组织产生毒性,这可能也会对重建的远期生物稳定产生一定的离心力。但近些年,随着科技的发展,越来越多的金属与合金被发掘并用于生物重建,无论是钽或钽合金都可以结合或替换钛合金成为一种新的假体设计尝试。临床骨重建的假体移植物,其组成物应与受体骨组织弹性模量相近,才能保持良好的应力分布,从而保证骨的长入。钽作为稀有金属,密度几乎是钛的4倍,提示其较钛可以提供更多的质量需求,且其弹性模量与正常骨组织接近,这表明如果通过设计适宜的孔径结构,定制钽合金假体,其或许能够保证良好的骨长入,并提供良好的力学稳定与强度。而且同为惰性金属,钽较钛具备更好的耐腐蚀性,可以避免长期的金属解离损失。有研究表明,钽合金或许能够替代钛合金行骨缺损的重建[20]。有临床研究报道,多孔钽合并多孔钛复合假体运用于骨缺损重建中,取得了良好的骨长入[21]。在骨缺损重建的过程中,不可避免地在移植物与残端骨面产生间隙。有动物研究表明,可以通过在钛合金表面植入带孔径的钽,能够很好地促进在移植物与截骨面缺损处成骨,保证假体移植后早期骨整合[22]。
3 3D打印在临床骨肿瘤切除后大段骨缺损重建的个性化体现
自体骨移植常因其具备良好的骨诱导性,而被视作缺损重建的“金标准”,在骨肿瘤大多数良性病变切除治疗中,多采用自体骨移植或同种异体骨去弥补骨缺损。但其因供体材料有限,无法满足大节段骨缺损的力学要求。在化疗技术的普及后,骨恶性肿瘤多以保肢为首选治疗方法。针对瘤体切除后的骨缺损重建,常用肿瘤性假体,可以满足病变的切除。但随着化疗技术的不断发展,不仅有保肢和避免复发的基本要求,还要保证患者术后的功能重建。3D打印技术,因其能及时准确地根据术区解剖定制个性化假体,而逐渐在骨肿瘤治疗中普及。通过微观环境的控制,给予骨长入适宜的应力刺激,更好地满足缺损重建的生物稳定需求。
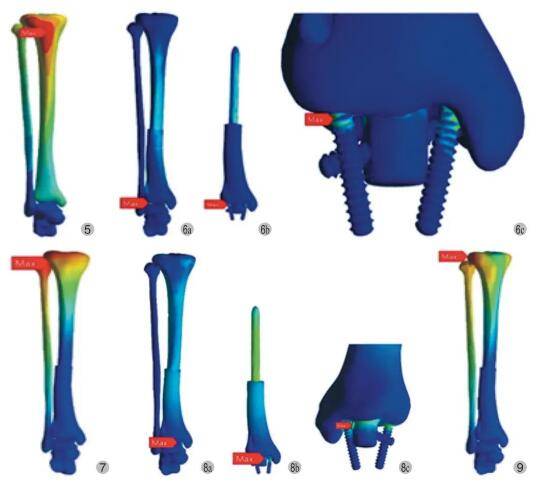
3.1 3D打印在儿童骨恶性肿瘤保肢重建的优势
骨原发恶性肿瘤好发于青少年,尽管外科治疗提倡保肢。但仍需综合考虑患者的年龄,骨生长成熟情况,家庭经济负担以及肿瘤病变位置,病变性质等因素,以保证优于截肢所带来的预期效果。针对于骨恶性肿瘤患者的保留骨骺与否,首先需要保证避免复发与远期双下肢不等长。因此可以就外科保留骨骺手术,提出相应适应证:①肿瘤病发于骨干或干骺端,且瘤变骨骺板尚未闭合;②根据影像学及术中病理提示,瘤变未侵犯至骨骺;③肿瘤病变性质对化疗敏感,新辅助化疗使用规范,且术前保证最大有效剂量。有临床报道提出,当瘤变骨Mirels评分(四肢长骨病理性骨折评分)=8分时建议采用生物重建,而对于Mirels评分>8分,特别是穿过骺板,侵犯骨骺的患者,建议采取机械重建。对于瘤变距骺板>2 cm,且Mierls评分<8分的病变,可以采用骨骺牵张,骨骺灭活再植,骨搬运等生物重建方法,但骨搬运重建需要求病变长度<15 cm。而对于病变接触或侵犯骨骺其并发病理性骨折的病变,若再采用生物重建,则其局部复发风险会提高[23-24]。有临床报道指出,若对骺板保留至少5 mm,即可基本满足再生长的需求,且患者短缩与肢体功能基本可接受[25]。3D打印可以精准地模拟病变解剖,在术中截骨面的病检排除瘤侵的前提下,可以针对瘤变距骺板>1 cm或距关节面>1 cm的病变,精准切除瘤变,保证骨骺或关节面的保留完整,还可还原瘤体切除后的缺损程度,快速定制出带有多孔结构的钛合金假体,在长径设计上还原术前解剖,贴合残留骨端,在横径设计方面适当行缩小设计,以保证残端植入处的适形匹配。而对于侵犯骨骺和关节面的瘤变或并发病理性骨折的患者,可以完整切除一侧骨质,行半关节假体置换,能够保证另一侧的骨面及骨骺的完整性,以尽最大努力保留非病变长骨的再长潜力,以尽量避免远期双下肢不等长的情况。不同于传统的肿瘤型假体,3D打印假体不需在另一侧放置植入物,可以最大程度地保留另一健侧骨面与骨骺的完整性。同时可以保留关节囊周围骨及周围软组织和韧带,推迟膝关节退变的时间,满足假体的软组织覆盖,尽晚行人工关节置换,尽可能地实现生物重建,为青少年患者提供患肢再生长潜力与重建后的生物稳定。且传统肿瘤型假体在设计时固定型号,有时不能满足年龄过小的患者,重新定制则又耗费较长时间,而3D打印假体可以根据术前影像快速设计出相应解剖需求的假体。
针对好发膝关节周围的骨原发恶性肿瘤,特别是青少年患者,设计假体时应该更注重生物性的重建,以达到关节置换或截肢所没有的预期功能效果。通过3D打印技术满足个性化的结构需求,结合髓腔的骨水泥植入,或在残骨端行螺钉或侧板固定,基本可以达到稳定的效果,术后可按力线方向早期负重[26]。相较于传统假体,3D打印技术可以通过在假体表面设计适宜的孔径结构,在内部设计多孔相连的结构,促进残留骨细胞向假体中心段长入,让骨细胞与具有生物性的多孔钛合金假体形成“骨-植入物”复合体,在保肢功能重建的治疗中,尽可能实现生物重建,使其尽早形成生物稳定,尽可能地避免短期的机械松动。
3.2 3D打印技术在极限骨缺损重建的可行性
骨原发恶性肿瘤导致的极限骨缺损,常常累及骨骺,关节面或整个长骨。常规的骨缺损重建有许多可供选择的重建方式,但对于极限骨缺损,临床上尚未有定论。对于极限骨缺损重建,临床中有生物重建,机械重建及复合重建。极限骨缺损的生物重建上,临床采用自体带血管腓骨移植、骨诱导膜技术等方法来尝试生物重建。尽管其基本无排斥反应,抗感染能力强的优点,但有手术创面过大,手术过程繁杂,且适形匹配容错小,移植长度受限等不足。生物重建的早期稳定,依赖于外固定架,骨整合所需时间又过长,故易并发钉道反应,形成延迟愈合,对患者的日常活动形成困扰[27]。3D打印技术,其适应范围较生物重建广泛,可以针对不同部位肿瘤进行重建,且可根据极限骨缺损后的形状,行个性设计,以达适形匹配。临床上通过在残端假体部分,设计3D打印非骨水泥柄并给予螺钉或侧板固定,在髓外采取常规假体设计来满足稳定。通过在骨接触面设计3D打印多孔设计,模拟骨小梁结构,内部多孔相连通道,提供微血管的生长,为骨长入提供微观环境,可以说是通过个性设计,来模拟贴近生物性的重建。有临床报道指出,在最短残留骨端4 cm的重建中,通过3D打印设计非骨水泥生物性假体柄,并设计弯曲椭圆形状,辅以螺钉,进而满足接触面骨长入,提供负重力学稳定及一定抗旋能力,术后早期功能恢复良好[28]。采用3D打印设计极限骨缺损的假体,能够适用于不同位置,不同节段的骨缺损重建,其通过微观控制,设计模拟贴近人体结构的骨小梁结构,来满足骨长入,可以说是机械重建中的生物性设计,既满足结构的强度稳定,又为远期的骨整合提供支持。上述表明,3D打印技术,可以满足长骨大节段或极限或超极限缺损的重建,具有可观的前景与可行性。
4 3D打印假体改进的尝试
目前临床常规使用3D打印假体,取得不错的成效,但有些患者仍会出现远期无菌性松动、假体断裂等并发症。这表明3D打印假体较常规骨重建虽然有其明显的优势,但也存在不足之处。针对骨肿瘤患者,临床上常常通过在髓腔植入骨水泥保持即时的稳定性,或在残端骨质植入假体处辅以螺钉或钢板以增加短力臂的稳定。但对于大节段和极限骨缺损的重建,单纯应用3D打印假体结合髓内骨水泥的固定,常常会导致残端的力臂过短。尽管3D打印微观的多孔相连结构,可以利于残端骨细胞向移植物中心长入,但在大节段骨缺损的重建中,很难完全保证截骨面的骨细胞能通过孔径结构长入到另一端或中心处,从而无法保证残端短力臂长期的生物稳定。因此针对大节段缺损的重建,或许可以舍弃移植物部分中段的3D打印孔径结构,在髓腔植入假体部分采用孔径结构,在髓腔外的大部分处采用常规实心结构。舍弃髓腔植入骨水泥的方式,通过对残端行髓内钉或侧板固定,既能实现早期的稳定;也能保证残端髓腔内的长入,获得生物稳定,提供远期的疲劳稳定[29-30]。在3D打印材料方面,也可以尝试在髓腔带孔径假体部分应用钛合金-多孔钽复合体结构,为骨长入提供有力条件[31-32]。有临床报道,采用非骨水泥固定性股骨柄,可以获得良好的早期与远期生物稳定[33]。这提示或许在残端髓腔部分采用的3D打印复合材料生物柄固定,是有一定可行性的。
新辅助化疗为骨原发恶性肿瘤保肢提供支持,3D打印技术设计内部多孔结构,可以为微观环境提供条件[34]。随着科技的发展,可以对金属材料及微观结构的改善,以更完善地进行生物重建。利用3D打印内部多孔相连结构,将载有化疗药物顺铂的水凝胶填充其中,实现局部抑瘤作用同时,又能避免化疗药物释放入体内循环的损害[35-36]。3D打印多孔结构在满足骨长入的同时,或许也可以尝试搭载些许骨诱导或抑瘤材料等,以进一步完善缺损的重建。
3D打印行骨重建的优势十分明显,针对常规的缺损,既保证了骨肿瘤的个体化假体设计,满足短期稳定性和长期生物力学稳定性的要求,但针对极限缺损或全长骨的重建,其仍存在不足之处,有待改进。或许临床可以尝试3D打印组配式假体,集众家所长,避免发生相关的并发症,相信是有很大发展前景,也值得去尝试探索。
5小结与展望
自体骨移植因其具备良好的骨诱导性且无排斥,在临床中普遍被认为是骨缺损弥补的“金标准”,但其数量有限,无法满足大节段骨缺损。3D打印技术的即时准确且具备个性化设计,使得其具备弥补大节段骨缺损的可行性,不同于传统假体单纯的力学稳定,3D打印可即时精准地设计出具备与人体相近的生物性钛合金假体,通过微观控制适宜的孔径及孔隙率,极大程度地避免应力屏蔽,良好的刺激残骨端的长入;通过多孔相连的结构,尽可能实现生物稳定。通过临床案例及相关动物研究提示,可以认为,3D打印技术在四肢长骨骨肿瘤骨缺损中的可行性,可以替代自体或异体骨移植成为大段骨缺损重建的选择。尽管3D打印设计的假体有其种种优势,但很多临床案例报道中,仍可看到其具有远期无菌松动的风险。针对于部分骨恶性肿瘤,在保肢原则前提下,保证瘤体的切除完整,这不可避免地导致术区的大节段骨缺损,特别是某些极限骨缺损,原本自然解剖结构只能残留些许骨质,植入假体后,是否能保证力学的稳定,满足远期的疲劳稳定,仍不能肯定。为保证缺损重建后的即时稳定及疲劳稳定,可以在残端髓腔部分运用复合材料非骨髓泥柄,结合残端螺钉或侧板固定,在髓腔外假体部分采用实心设计。既保留孔径结构的长入优势,也大大提高了重建后的强度,尽可能地弥补单纯3D打印假体的即时稳定不足与远期松动的不足,使得缺损的重建同时具备早期与远期的稳定。也可以在材料选择上尝试新的骨诱导材料,或通过搭载些许抑瘤物质,以完善骨缺损的重建。总之,通过许多临床案例的报道与讨论,认为可以通过3D打印技术,或对其进行些许地改进与补缺,进一步满足长骨大节段骨缺损,特别是针对部分极限骨缺损的重建,但仍需要远期随访与大样本的支持。
参考文献
[1]朱忠胜,张春林.骨肉瘤保肢与截肢[J].国际骨科学杂志,2012,33(2):124-125.
[2]黄崇新,吕波,邓俊才.新辅助化疗联合关节置换术治疗四肢恶性骨肿瘤的效果及其对血清肿瘤标记物水平、免疫功能的影响[J].中国骨与关节损伤杂志,2018,33(1):39-42.
[3]ZEKRY K M,YAMAMOTO N,HAYASHI K,et al.Reconstruction of intercalarybone defect after resection of malignant bone tumor[J].J Orthop Surg,2019,27(1):1-9.
[4]邹波,高秋明,黄强,等.大段骨缺损外科治疗方法的应用研究进展[J].山东医药,2021,61(36):91-95.
[5]郑沛中,张玮琼,张茂林.自体骨联合同种异体骨对胫腓骨良性骨肿瘤患者骨缺失的修复效果[J].哈尔滨医药,2020,40(4):339-340.
[6]黄希.长骨骨缺损的组织工程治疗现状[J].临床与病理杂志,2021,41(2):456-461.
[7]周东明,敖晔,张海东,等.兔尺骨中段临界节段性骨缺损模型的建立[J].中国基层医药,2019,26(13):1545-1548.
[8]刘冰川,李星材,邱卫鹏,等.应用3D打印多孔钛合金假体重建下肢长骨骨缺损的临床疗效[J].中华骨科杂志,2022,42(10):626-634.
[9]梁庆优,邓春林.长骨大段骨缺损修复材料的力学性能及制备策略[J].材料导报,2021,35(13):13100-13108,13118.
[10]吴昊,王陶然,高嘉锴,等.四肢长干骨骨缺损的系统化新分型研究[J].中华创伤骨科杂志,2019,21(12):1024-1028.
[11]LORO A,LORO F,FRANCESCHI F,et al.Bone transport in the management of post-osteomyelitis femoral defects in children:A case series with a minimum of 10-year follow-up in Uganda[J].J ChildOrthop,2022,16(4):313-321.
[12]KUBES K,FRIEDMAN A,PYLE C,et al.Management of twenty centimeter segmental bone defect of femoral shaft secondary to infected non-union of fracture using masquelet technique:A casereport[J].Int J Surg Case Rep,2021,84(3):106107.
[13]ZHAO D,TANG F,MIN L,et al.Intercalary reconstruction of the"ultra-critical sized bone defect"by 3D-printed porous prosthesis afterresection of tibial malignant Tumor[J].Cancer Manag Res,2020,12(1):2503-2512.
[14]牛晓颖,高世磊,屈国新,等.3D打印定制保留骨骺及关节面假体在青少年股骨原发恶性骨肿瘤大段骨缺损重建中的应用[J].中国修复重建外科杂志,2022,36(11):1374-1380.
[15]AXKMANN T,KLINGEBIEL S,GOSHEGER G,et al.Reconstruction of total bone defects following resection of malignant tumors of the upper extremity with 3D printed prostheses:Presentation of two patients with a follow-up of three years[J].CaseRepOrthop,2020,10(16):1-4.
[16]张伟蒙,汪杰,胡晶.3D打印骨组织支架孔隙结构对支架性能影响的研究进展[J].中国塑料,2022,36(12):155-166.
[17]王庆,翁益平,刘宏伟,等.3D打印不同孔径钛合金支架修复兔股骨缺损:600μm孔径更有利于骨整合[J].中国组织工程研究,2021,25(28):4441-4446.
[18]NULTY J,FREEMAN F E,BROWE D C,et al.3D bioprinting of prevascularised implants for the repair of critically-sized bonedefects[J].Acta Biomater,2021,17(3):154-169.
[19]YE X,HE J X,WANG S L,et al.A hierarchical vascularized engineered bone inspired by intramembranous ossification formandibular regeneration[J].Int J Oral Sci,2022,14(1):31.
[20]LUO C Q,WANG C,WU X D,et al.Influence of porous tantalum scaffold pore size on osteogenesis and osteointegration:A comprehensive study based on 3D-printing technology[J].Mater SciEng C Mater BiolAppl,2021,14(7):112382.
[21]徐永清,范新宇,王腾,等.皮瓣加3D打印微孔钛(钽)假体治疗下肢软组织缺损伴大段骨缺损[J].中华显微外科杂志,2022,45(1):21-27.










