我国药品审评审批制度改革对创新药技术转移的影响论文
2026-04-10 17:49:58 来源: 作者:xuling
摘要:创新药研发具有成本高、周期长、技术密集的特点。药品审评审批是创新药能否上市的重要环节。完善药品审评审批制度不仅能提高创新药研发速度,还能加速创新药技术转移。
摘要:创新药研发具有成本高、周期长、技术密集的特点。药品审评审批是创新药能否上市的重要环节。完善药品审评审批制度不仅能提高创新药研发速度,还能加速创新药技术转移。文章就我国药品审评审批制度改革对创新药技术转移的影响展开论述,以期为我国药品审评审批制度改革提供有效参考。
关键词:药品审评审批制度;创新药;技术转移
近年来,随着我国医疗产业快速发展,药品审评审批制度不断完善,促进了药品高质量发展[1]。药品审评审批制度改革不但可以加速医药创新,还可以推动技术转移,改变医药行业生态环境,促使医药行业从“仿制为主”向“创新驱动”转变[2]。
1目前我国药品审评审批制度改革现状分析
1.1创新药注册申请申报量持续增长
创新药注册申请申报数据可以反映创新药研发情况,为药品审评审批制度改革提供有效参考[3]。国家药品监督管理局的统计报告指出,2023年以注册申请类别统计,受理新药临床试验申请(investigational new drug application,IND)2 997件,同比增加33.56%;验证性临床试验申请170件,同比增加32.81%;新药上市许可申请(new drug application,NDA)470件,同比增加40.72%;2024年受理新药临床试验申请IND 3 073件,验证性临床试验申请247件,NDA 549件。总体来看,我国药品注册数量逐年升高,反映了我国药品审评审批制度改革对药品研发的积极推动作用。制度完善促进了医药企业的药品研发活动;创新药注册申请申报数量增长也表明医药行业对于药品创新抱有较高热情[4]。
1.2创新药注册审评批准数量逐年增长但趋势平缓
创新药的整体质量状况是创新药能否上市的重要依据[5]。国家药品监督管理局的统计报告指出,2023年我国批准化学药品IND 1 448件,同比增加15.92%,包括创新化学药品IND 1 147件(513个品种),同比增加13.12%,改良型化学药品IND 301件(171个品种),同比增加27.54%;2024年批准化学药品IND 1 652件,同比增长13.26%,以注册分类统计,包括创新化学药品IND 1 247件(538个品种),同比增长8.12%,改良型化学药品IND 405件(219个品种),整体呈现逐年增长趋势,但上升趋势相对平缓。创新药质量把关依旧是药品审评审批的关键。因此,如何引导医药企业提高药品研发质量、确保药品的有效性与安全性,是药品审评审批制度改革需要考虑的重要问题[6]。
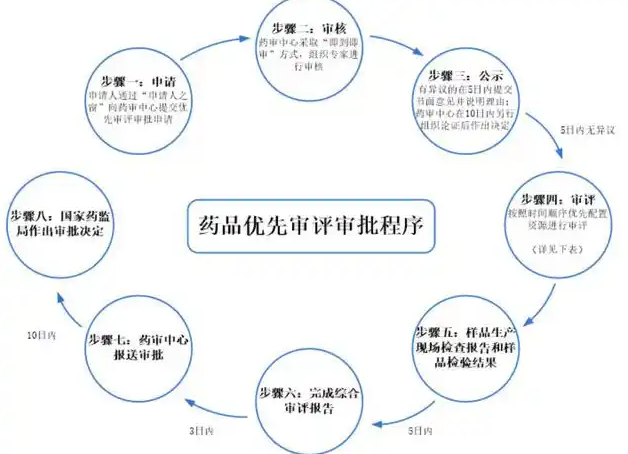
2我国药品审评审批制度改革对创新药技术转移的影响
2.1审评效率提升加速技术转移
药品审评审批制度改革能够简化药品审评程序,引入优先审评机制使创新药技术转移速度大幅提升[7]。自2020年《药品注册管理办法》实施以来,我国共有496件药品注册申请被纳入优先审评程序,包括抗肿瘤药物、皮肤及五官科药物、内分泌系统药物等。其中,抗肿瘤药物数量最多,占比42.54%。抗肿瘤药物审评耗时显著缩短,吸引了跨国药企将研发战线向中国转移,能够为我国医药行业发展带来新活力,同时加速国外技术向国内的转移[8]。
2.2政策变化降低技术转移门槛
传统模式下,企业变更生产场地必须提交全套注册材料,审批周期长且容易造成资源浪费。药品审评审批制度改革后,新政策运行企业在技术转让过程中,通过补充申请来变更生产场地,且无需提交已经获批的注册资料,仅需提交变更后的关键数据,如场地验证报告、质量对比报告等[9]。例如,某医药企业将生产基地从深圳转移到上海时,补充申请审批时间仅3个月,流程耗时缩短60%以上,降低了技术转移造成的行政负担,没有因为反复提交材料影响医药研发进度[10]。同时,药品审评审批制度改革还开展了分段生产试点、跨境委托生产等探索活动,为医药技术转移提供了更加灵活的路径。该举措不但可以减轻企业的产能压力,还能促进区域产业链协调发展,促使技术转移从“单点转移”向“链条化转移”发展[11]。在全球化趋势不断加深的时代背景下,我国政策放宽了跨境委托生产限制,允许医药企业将生产环节转移到海外,以形成“全球研发-海外生产-国内销售”闭环,提高我国医药技术的国际竞争力,也为本土企业参与国际分工提供新途径[12]。
3我国药品审评审批制度改革的优化路径
3.1简化药品审评审批流程
药品审评审批制度改革关系着创新药研发与技术转移,但从整体情况来看,我国药品审评审批流程仍存在较多问题,需要简化流程,构建更加高效、规范的药品审评审批体系[13]。简化药品审评审批流程需要减少其中重复、冗余的环节,以节省资源、降低成本。首先,简化药品注册申请材料,尤其是不必要的行政材料,只需明确申报中的关键材料和数据,确保材料贴近实际研发。例如,可以减少临床试验申请的行政材料,降低医药企业负担,加快创新药的研发进度[14]。其次,开展集中审评审批,减少不必要的环节,提高审批效率。同时,各地区还可以设立一体化的信息化服务平台,提供全方位的咨询指导,避免企业在不同部门间来回奔走[15];构建药品审评审批公开平台,定期发布药品审评审批结果,督促医药企业根据结果及时调整。最后,引入大数据技术,对药品审评审批流程进行监督与控制,及时发现潜在问题[16]。

3.2加强药品审评审批团队建设
药品审评审批工作是一项复杂且专业化的工作,依赖高水平工作人员的支持。因此,需要构建高质量的审评审批团队,以提高工作质量、缩短审批周期、加速创新药研发和技术转移[17]。首先,可以优化人才引进制度,引入具有医药研发经验的人才,提高工作效率。同时,定期组织专业培训,培训内容覆盖政策法规、临床试验等,提高人员专业素养[18]。其次,组织工作人员积极参与国际会议,与其他地区的监管机构进行合作交流,实现信息共享。最后,需要构建多学科协作的审评团队,邀请药学、统计学、临床医学等学科专家,提高审评审批的准确性。
3.3创新药品审评审批模式
创新药品审评审批模式不仅可以提高药品研发速度,更有助于技术转移,促进医药行业的可持续发展[19]。首先,要立足我国实情,提高药品审评审批流程的信息化水平,引入人工智能、大数据技术,开发自动化药品审评审批平台,借助AI服务协助工作人员整理各种资料,实现对药品审评审批的初步筛选。其次,构建云服务平台以集中存放各种资料,方便企业查找与学习,同时设置论坛,方便企业在线提问和讨论。最后,构建跨区域合作平台,对不同地区、不同企业的药品审评审批信息进行数据共享和分析,提供有效的决策建议。
4结语
药品审评审批制度改革是调整我国医药供给侧结构的重要措施,主要通过优化监管流程,提高审评效率,加快创新药从研发到上市的速度。完善药品审评审批制度有助于提高医药研发质量,促进医药行业稳步发展。在相关政策支持下,该项实践赢得了国内企业的大力支持,同时吸引了国外资本参与,形成了多元化协同创新机制,可优化行业发展环境,推动国外技术转移到国内。因此,需要重视药品审评审批制度改革,加速创新药研发与技术转移,推动医药行业可持续发展。
参考文献
[1]孔繁圃.持续深化药品审评审批制度改革以优异成绩迎接党的二十大胜利召开[J].中国新药杂志,2022,31(18):1761-1766.
[2]孔繁圃.深化审评审批制度改革推动药品高质量发展[J].中国食品药品监管,2022(2):14-23.
[3]周思源,杨志敏,宋媛媛,等.我国创新药审评审批的改革与发展—以抗肿瘤药物为例[J].中国食品药品监管,2024(6):4-15.
[4]杨浩宇,田侃,游雪,等.我国优先审评审批上市儿童用药的特征分析[J].中国药房,2025,36(5):519-523.
[5]GUPTA A,PATHAK S.Assessment of analytical techniques for precise quantification of four antiviral drugs in pharmaceutical research and development:a comprehensive review[J].Current Pharmaceutical Analysis,2024,20(6):409-424.
[6]李响,王鑫,孟昭君,等.我国中药品种保护申报审批情况简析[J].天津药学,2025,37(8):995-1000.
[7]中新.国家药品监督管理局改革审评审批支持中药新药上市[J].中医药管理杂志,2024,32(18):43.
[8]吴亦凡,张伟,于巍,等.PDUFA法案对药品监管机构审评能力提升的借鉴[J].中国新药杂志,2022,31(24):2404-2412.
[9]ROHITAS D,RAJESH S,SAKSHI M.Pharmaceutical in situ gel for glaucoma:Recent trends and development with an update on research and patents[J].Critical Reviews in Therapeutic Drug Carrier Systems,2024,41(3):1-44.
[10]李鑫悦,何静雯,吴艺,等.产业视角下中国创新药上市审评审批效率影响因素研究[J].中国药学杂志,2025,60(2):201-206.
[11]郎浩辰,郭述金,温庆辉,等.我国儿童用药审评审批政策创新成效及改革方向[J].中国药物评价,2023,40(2):122-125.
[12]党子悦,郭冬梅.我国药品加快上市注册程序的注册情况分析[J].中国药事,2023,37(7):735-742.
[13]俞颖慧,杨树俊,周斌.我国罕见病药物优先审评审批情况简析[J].中国医药工业杂志,2023,54(2):277-282.
[14]孙权,於莲莲,张宇,等.全球新型抗感染药物加速审评审批机制研究[J].沈阳药科大学学报,2023,40(2):219-232.
[15]吴文文,季兴,倪明明,等.欧盟罕见病用药审评审批分析及其对我国的启示[J].中国医院用药评价与分析,2024,24(11):1402-1408.
[16]吴丽真,董雪婷,李天翥.2021-2024年我国中药注册申请审批情况分析[J].中国药事,2024,38(10):1115-1122.
[17]郭润芳,连桂玉.我国儿童药品加快上市注册程序的实施情况分析[J].中国医药工业杂志,2024,55(9):1295-1299.
[18]推进创新药同步研发、注册与审评,构建中国医药创新生态系统——注册监管科学性及监管能力建设[J].中国食品药品监管,2022(8):14-29.
[19]唐凌,艾星,赵田,等.对“以患者为中心”的罕见疾病药物研发的审评考虑[J].罕见病研究,2024,3(2):168-174.










