青蒿琥酯增强子宫内膜癌细胞对孕激素敏感性论文
2026-04-10 16:55:34 来源: 作者:xuling
摘要:文章旨在评估青蒿琥酯能否增强子宫内膜癌细胞对孕激素的敏感性,并检测其对细胞周期的影响。取对数生长期的子宫内膜癌Ishikawa细胞和AN3CA细胞随机分为4组:对照组、青蒿琥酯组、孕激素组、青蒿琥酯和孕激素联用组。
摘要:文章旨在评估青蒿琥酯能否增强子宫内膜癌细胞对孕激素的敏感性,并检测其对细胞周期的影响。取对数生长期的子宫内膜癌Ishikawa细胞和AN3CA细胞随机分为4组:对照组、青蒿琥酯组、孕激素组、青蒿琥酯和孕激素联用组。加药处理24 h后,用CCK-8检测细胞存活率,用Annexin V-FITC/PI双染法检测细胞凋亡,用划痕实验及Transwell侵袭实验检测细胞迁移侵袭能力,用Western blotting检测细胞周期相关蛋白的表达。与对照组、青蒿琥酯组、孕激素组相比,青蒿琥酯和孕激素联用组细胞存活率最低,细胞凋亡率最高,增殖抑制效果最好,杀伤效果最优。划痕实验及Transwell侵袭实验表明,青蒿琥酯和孕激素联用能明显减弱子宫内膜癌细胞的侵袭迁移能力。Western blotting结果表明,青蒿琥酯和孕激素联用组的细胞周期蛋白Cyclin D1、CDK2表达水平显著降低。研究证实,青蒿琥酯能逆转子宫内膜癌的孕激素耐药,并对细胞周期产生影响。
关键词:青蒿琥酯;子宫内膜癌;孕激素耐药;细胞增殖;细胞周期
子宫内膜癌是常见的女性生殖系统恶性肿瘤之一[1]。孕激素是早期子宫内膜癌治疗的常用药物,通过与孕激素受体结合[2],抑制子宫内膜细胞增殖,并诱导其凋亡。然而,部分患者在治疗过程中会发展出耐药性,主要表现为肿瘤细胞对孕激素敏感性下降或丧失[3]。目前关于孕激素耐药的机制,可能涉及孕激素受体下调或突变、某些信号通路重编程,以及代谢改变[4]。
青蒿琥酯(Artesunate)是从传统中药青蒿中提取出的一种抗疟疾药物。自被用于抗疟疾治疗以来,青蒿琥酯的药理活性便引起了广泛关注[5]。近年来,多项研究揭示了青蒿琥酯的抗癌潜力。青蒿琥酯能通过多种机制发挥抗肿瘤作用,包括抑制肿瘤细胞增殖、促进细胞凋亡、干扰细胞周期、调控自噬和抑制肿瘤新生血管形成等[6]。此外,青蒿琥酯在某些肿瘤模型中表现出了对耐药细胞的抑制作用,具有逆转药物耐药性的潜力[7]。
本研究集中评估青蒿琥酯能否增强子宫内膜癌细胞对孕激素的敏感性,并检测其对细胞周期的影响,以期揭示青蒿琥酯增强孕激素疗效的潜在机制,探索其在子宫内膜癌治疗中的应用可能。
1材料与方法
1.1材料与试剂
Ishikawa细胞和AN3CA细胞,由上海市第一人民医院提供保存;DMEM培养基、胎牛血清、青霉素和链霉素,均购自上海欲立生物科技有限公司;青蒿琥酯,购自上海阿拉丁生化科技股份有限公司;AnnexinV-FITC/PI试剂盒,购自碧云天生物技术有限公司(中国);Cyclin D1、CDK2和α-Tublin单克隆抗体,购自Cell Signaling Technology(CST)。
1.2细胞培养与处理
将Ishikawa和AN3CA细胞接种在含10%胎牛血清的DMEM培养基(含1%青霉素、链霉素)上,培养温度设定为37℃,培养环境为5%CO2[8]。
将细胞分为4组:对照组(无药物处理)、ART组(加青蒿琥酯)、P4组(加孕激素)、ART与P4联用组(加青蒿琥酯和孕激素)。青蒿琥酯浓度为50μM,孕激素浓度为20μM。
1.3细胞增殖和存活率检测
为评估青蒿琥酯和孕激素对细胞增殖的影响,采用CCK-8细胞增殖检测试剂盒进行分析。将细胞以每孔1×105个细胞的密度接种于96孔板,待细胞贴壁后分别给药处理。培养24 h后,每孔避光加入10μL CCK-8溶液,继续孵育2 h。使用酶标仪在450 nm波长处测量吸光度,计算细胞存活率。培养48 h后,测定方法同上。
1.4细胞凋亡检测
细胞凋亡检测采用Annexin V-FITC/PI双染法。药物处理24 h后,收集细胞并用PBS洗涤,将细胞重悬于缓冲液,加入适量Annexin V-FITC和PI染色。染色完成后,用PBS洗掉多余染料,通过流式细胞仪检测凋亡细胞比例。
1.5划痕试验
将Ishikawa和AN3CA细胞分别均匀接种于无菌6孔培养板中,培养至形成一个紧密的单层细胞。使用无菌划痕工具在细胞单层上划出一条直线,形成“伤口”;用无血清DMEM清洗细胞,去除划痕中的细胞碎片和未黏附细胞。将清洗后的细胞分别加药处理,在处理后的不同时间点(0、24 h)使用显微镜观察并记录划痕区域的愈合情况。
1.6 Transwell小室侵袭实验
冰上将Matrigel胶用无血清DMEM进行1:8稀释,混匀后加入小室,将小室放入CO2培养箱中孵育2 h。吸掉孵育完成后小室中多余的液体,每孔加入100μL无血清DMEM,在培养箱中放置水化30 min。将Ishikawa和AN3CA细胞铺在上室中,每小室约3万个细胞,并加入不同药物;在下室中加入500μL含10%FBS的DMEM。培养48 h后,PBS清洗小室,用棉签轻柔擦去上室细胞和Matrigel,于4%多聚甲醛固定15 min,将小室适当风干,用结晶紫染色15 min,PBS清洗3遍,于37℃干燥。将小室置于显微镜下,随机选取3个视野,拍照并计数,评估细胞侵袭能力。
1.7 Western blot分析
Western blot实验用于检测CyclinD1、CDK2等相关蛋白的表达。细胞经药物处理,使用强RIPA裂解液提取总蛋白,并用BCA法定量。取等量蛋白样品进行SDS-PAGE电泳,随后转膜到PVDF膜。膜先与CyclinD1和CDK2抗体(1:1 000稀释)孵育过夜,再与二抗(1:10 000稀释)孵育1 h。使用ECL发光试剂进行化学发光检测,分析各蛋白表达水平。
1.8数据分析
使用Image J软件分析Western blot实验所得的图片灰度。实验数据通过GraphPad Prism 9.0进行统计分析。组间差异采用单因素方差分析(ANOVA)进行比较,结果以均数±标准差表示。P<0.05表示差异具有统计学意义。
2结果
2.1青蒿琥酯与孕激素联用对细胞增殖的影响
为探究青蒿琥酯能否增强子宫内膜癌细胞对孕激素的敏感性,用CCK-8法检测Ishikawa和AN3CA的细胞活力。2种细胞的实验结果如图1所示。相较于对照组,青蒿琥酯组和孕激素组的细胞活力均有所下降。当青蒿琥酯和孕激素联用时,细胞活力进一步降低,揭示两者可能能够协同抑制细胞增殖。
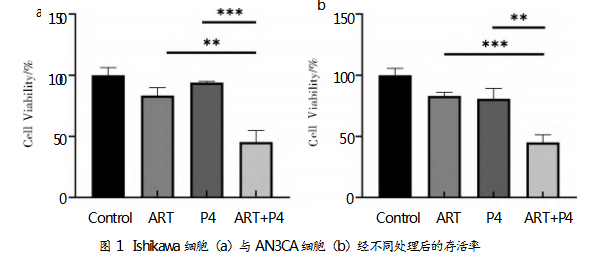
2.2青蒿琥酯与孕激素联用对癌细胞凋亡的影响
通过流式细胞仪评估青蒿琥酯与孕激素诱导的细胞凋亡情况。细胞凋亡时,细胞膜内表面的磷脂酰丝氨酸会翻转到细胞膜外侧,与Annexin V-FITC特异性结合,被流式细胞仪检测到。PI探针则用于标记凋亡晚期无正常细胞膜的细胞。使用AnnexinV-FITC/PI试剂盒检测不同处理组的Ishikawa细胞凋亡水平,结果如图2所示。相较于对照组,青蒿琥酯组、孕激素组的细胞凋亡率可以忽略不计,而青蒿琥酯与孕激素联用组的细胞凋亡率显著提升。数据证实,青蒿琥酯与孕激素联用明显促进了子宫内膜癌细胞凋亡。
2.3青蒿琥酯和孕激素联用对子宫内膜癌细胞迁移和侵袭能力的影响
为探究青蒿琥酯和孕激素联用是否会影响子宫内膜癌细胞迁移及侵袭,开展了划痕实验和Transwell小室侵袭实验。Ishikawa细胞和AN3CA细胞在不同处理条件下的划痕愈合情况如图3所示。在0 h(OH)时,所有组别的划痕宽度基本一致。24 h后,对照组细胞迁移明显,划痕几乎愈合;ART组和P4组划痕愈合程度较低,说明青蒿琥酯和孕激素均能抑制细胞迁移;ART+P4组的划痕愈合程度最低,表明青蒿琥酯和孕激素联用对细胞迁移的抑制作用更显著。
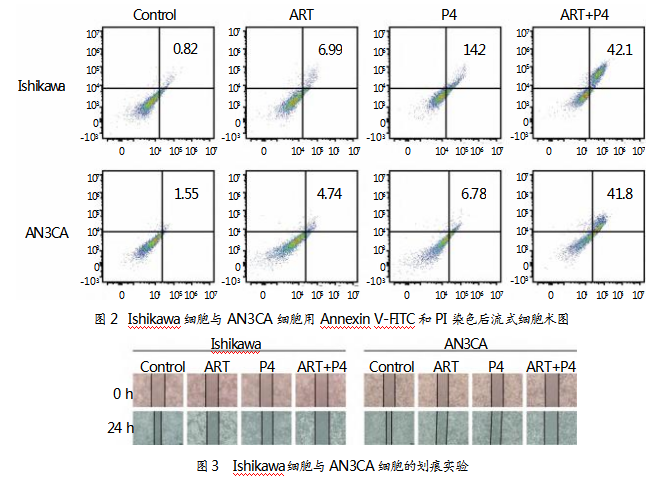
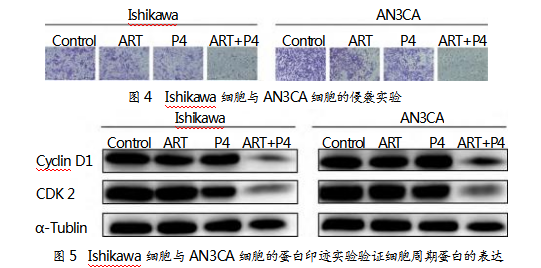
Ishikawa细胞和AN3CA细胞在不同处理条件下的侵袭能力如图4所示。结果显示,对照组细胞侵袭能力较强;ART组和P4组细胞侵袭能力显著降低,说明青蒿琥酯和孕激素均能抑制细胞侵袭;ART+P4组细胞侵袭能力最低,进一步证实了青蒿琥酯和孕激素联用对细胞侵袭的协同抑制作用。
综上,青蒿琥酯和孕激素联用能有效抑制子宫内膜癌细胞迁移和侵袭,证实青蒿琥酯能增强子宫内膜癌细胞对孕激素的敏感性。
2.4青蒿琥酯与孕激素联用对细胞周期蛋白的影响
为验证青蒿琥酯与孕激素联用对细胞周期的影响,开展蛋白印迹实验。以α-Tubulin为内参蛋白,检测Ishikawa细胞和AN3CA细胞中细胞周期相关蛋白Cyclin D1和CDK 2的表达情况,如图5所示。相较对照组,ART组和P4组Cyclin D1和CDK 2蛋白的表达水平无显著变化;ART+P4组中,Cyclin D1和CDK 2的表达水平大幅度降低,表明青蒿琥酯和孕激素联用对细胞周期蛋白抑制作用显著。结果证实,青蒿琥酯与孕激素联用能够显著抑制子宫内膜癌细胞中细胞周期蛋白的表达,可能阻止细胞周期进展,抑制细胞增殖。这一发现进一步支持了青蒿琥酯和孕激素联用在子宫内膜癌治疗中的潜在应用价值,为后续研究和临床应用提供了重要的实验依据。
3讨论
青蒿琥酯作为一种抗疟疾药物,具有一定的抗癌作用,能够抑制多种肿瘤细胞增殖[9]。在肿瘤治疗中,青蒿琥酯能够通过激活胞内凋亡信号通路(如线粒体途径和死亡受体途径),增加细胞内活性氧(ROS)水平,诱导细胞凋亡[10]。肿瘤生长依赖新生血管生成,而青蒿琥酯在抑制新生血管生成方面也发挥着一定的作用[11]。此外,青蒿琥酯还能诱导自噬,增强NK92细胞对癌细胞的杀伤作用。ATG5作为自噬过程中的关键蛋白参与自噬体的形成,而青蒿琥酯能通过调节ATG5的表达影响细胞自噬,发挥抗肿瘤作用[12]。另有研究表明,青蒿琥酯可通过调节AMPK信号通路发挥抗肿瘤作用[13]。青蒿琥酯对人子宫内膜癌细胞具有抑制作用[14-15],且在其他肿瘤模型中与药物联用可增强肿瘤对药物的敏感性[16-19]。然而,青蒿琥酯能否逆转子宫内膜癌的耐药性尚未有明确报道。
本研究通过体外实验探讨了青蒿琥酯与孕激素联用对子宫内膜癌细胞的影响,分析了青蒿琥酯能否通过增强子宫内膜癌对孕激素的敏感性逆转子宫内膜癌的耐药性。结果表明,该联合用药策略能有效抑制子宫内膜癌细胞增殖并促进细胞凋亡。这可能与青蒿琥酯结构上的过氧化桥有关——能在细胞中产生ROS促进细胞凋亡。此外,2种药物联用还能减弱细胞的迁移和侵袭能力,防止肿瘤进一步扩大增长或向别处转移,同时显著降低细胞周期蛋白Cyclin D1和CDK2的表达水平,阻断细胞周期,抑制癌细胞发展。
实验结果证实,青蒿琥酯可显著增强子宫内膜癌细胞对孕激素的敏感性,并对其细胞周期产生影响。这一发现,为青蒿琥酯与孕激素联合应用于子宫内膜癌治疗提供了有力的实验依据,展现出了广阔的研究前景。然而,其背后的深层机制仍需进一步探索,以完善联合治疗策略,为子宫内膜癌耐药患者提供新的治疗方案。
参考文献
[1]CROSBIE E J,KITSON S J,MCALPINE J N,et al.Endometrial cancer[J].Lancet,2022,399(10333):1412-1428.
[2]W K T,M A N,J E D,et al.Global expression analysis of endometrial cancer cells in response to progesterone identifies new therapeutic targets[J].The Journal of Steroid Biochemistry and Molecular Biology,2023,234:106399.
[3]TANG H C,LIN T C,WU M H,et al.Progesterone resistance in endometriosis:Apathophysiological perspective and potential treatment alternatives[J].Systems Biology in Reproductive Medicine,2024,23(1):e12588.
[4]沈偲,滕银成.子宫内膜癌孕激素耐药机制及新型疗法的研究进展[J].上海交通大学学报(医学版),2020,40(12):1677-1682.
[5]EMMANUEL B,MOUSTAPHA M,ISABELl B,et al.Antimalarial artesunate-mefloquine versus praziquantel in African children with schistosomiasis:An open-label,randomized controlled trial[J].Nature medicine,2024,30(1):130-137.
[6]FAN X,YAN Y,LI Y,et al.Anti-tumor mechanism of artesunate[J].Frontiers in Pharmacology,2024,15:1483049.
[7]MA Z,CHEN W,LIU Y,et al.Artesunate sensitizes human hepatocellular carcinoma to sorafenib via exacerbating AFAP1L2-SRC-FUNDC1 axis-dependent mitophagy[J].Autophagy,2023,20(3):541-556.
[8]郭志想,杨光,杨波,等.根皮素包合物对ARPE-19细胞损伤的保护效果的研究[J].工业微生物,2024,54(6):75-81.
[9]LI Y,ZHOU X,LIU J,et al.Therapeutic potentials and mechanisms of Artemisinin and its derivatives for tumorigenesis and metastasis[J].Anti-cancer Agents in Medicinal Chemistry,2020,20(5):520-535.
[10]HUANG Z,GAN S,ZHUANG X,et al.Artesunate inhibits the cell growth in colorectal cancer by promoting ROS-dependent cell senescence and autophagy[J].Cells,2022,11(16):2472.
[11]BERKÖZ M,ÖZKAN-Y1LMAZ F,ÖZLÜER-HUNT A,et al.Artesunate inhibits melanoma progression in vitro via suppressing STAT3 signaling pathway[J].Pharmacological Reports,2021,73(2):1-14.










