两性霉素B微生物限度检查方法适用性试验研究论文
2026-04-10 15:40:09 来源: 作者:xuling
摘要:文章旨在建立两性霉素B原料药的微生物限度检查方法。根据《中华人民共和国药典》(2020年版)要求,对两性霉素B原料药进行方法学适用性试验。
摘要:文章旨在建立两性霉素B原料药的微生物限度检查方法。根据《中华人民共和国药典》(2020年版)要求,对两性霉素B原料药进行方法学适用性试验。由于两性霉素B具有抗真菌活性,采用常规方法进行微生物回收试验时,白色念珠菌和黑曲霉回收率不合格。在培养基中加入自制中和剂后,可消除供试品的抑菌活性,提高白色念珠菌和黑曲霉的试验菌株回收率。试验以pH 7.0氯化钠-蛋白胨缓冲液为稀释液,将供试品稀释成1:50的供试液,并采用倾注法检查需氧菌总数和霉菌和酵母菌总数。该方法(稀释法和中和法相结合)可用于两性霉素B原料药的微生物限度检查。
关键词:两性霉素B;微生物限度;稀释法;中和法
两性霉素B(Amphotericin B,AmB)是一种由结节链霉菌发酵得到的多烯大环内酯类抗生素,被广泛用于治疗深部真菌感染的药物制造[1-5]。AmB对《中华人民共和国药典》(2020年版)试验菌中的白色念珠菌和黑曲霉等真菌的生长具有抑制作用。在微生物限度检查中,霉菌和酵母菌总数计数检查方法面临适用性难题。因AmB产品具有抗真菌活性,只有采用适宜的方法去除或中和AmB抑菌活性,才可能检出污染药品的微生物,避免出现假阴性检验结果[6-8]。河北亚诺生物科技集团股份有限公司研究了两性霉素B原料药微生物限度检查方法,确定了微生物计数方法和控制菌(大肠埃希菌)检查方法。本文旨在探讨两性霉素B的微生物限度检查,为其他抑菌药品的方法建立提供参考。
1仪器与材料
1.1仪器
立式压力蒸汽灭菌器,购自上海博迅实业有限公司医疗设备厂;生化培养箱,购自天津市泰斯特仪器有限公司;电子天平,购自常熟市双杰测试仪器厂;生物安全柜,购自苏净集团苏州安泰空气技术有限公司;微生物检验仪,购自浙江泰林生物技术股份有限公司;药品冷藏箱,购自重庆康诚永生试验设备有限公司;多功能漩涡混匀仪,购自群安实验仪器有限公司。
1.2药品、试剂和培养基
两性霉素B样品由沧州临港亚诺生物医药有限公司提供。
微孔滤膜,购自浙江泰林生物技术股份有限公司;聚山梨酯80,购自成都市科隆化学品有限公司;卵磷脂和L-组氨酸,购自北京奥博星生物技术有限责任公司;自制中和剂,购自河北亚诺生物科技集团股份有限公司。
胰酪大豆胨琼脂培养基(TSA)、胰酪大豆胨液体培养基(TSB)、沙氏葡萄糖琼脂培养基(SDA)、沙氏葡萄糖液体培养基(SDB)、麦康凯琼脂培养基、麦康凯液体培养基、pH 7.0氯化钠-蛋白胨缓冲液,均购自北京陆桥技术股份有限公司。
1.3菌种
试验用菌种包括金黄色葡萄球菌(Staphylococcus aureus)[CMCC(B)26 003]、铜绿假单胞菌(Pseudomonas aeruginosa)[CMCC(B)10104]、枯草芽孢杆菌(Bacillus subtilis)[CMCC(B)63 501]、白色念珠菌(Candida albicans)[CMCC(F)98 001]、黑曲霉(Aspergillus niger)[CMCC(F)98 003]、大肠埃希菌(Escherichia coli)[CMCC(B)44 102],均购自中国食品药品检定研究院。
2实验方法与结果
2.1菌液制备
按《中华人民共和国药典》(2020年版)规定培养各试验菌株。取金黄色葡萄球菌、铜绿假单胞菌、枯草芽孢杆菌、大肠埃希菌、白色念珠菌的新鲜培养物,用0.9%无菌氯化钠溶液制成适宜质量浓度的菌悬液;取黑曲霉的新鲜培养物加入适量含0.05%(V/V)吐温80的0.9%无菌氯化钠溶液,洗脱孢子,用胶头滴管吸出适量孢子悬液,用含0.05%聚山梨酯80的0.9%无菌氯化钠溶液制成适宜质量浓度的黑曲霉孢子悬液。
2.2供试液制备
称取两性霉素B 10 g,用pH 7.0氯化钠-蛋白胨缓冲液制成1:10的供试液。取1:10供试液,用pH 7.0氯化钠-蛋白胨缓冲液稀释制成1:50、1:100供试液,或其他适宜质量浓度的供试液。
2.3控制菌(大肠埃希菌)检查
2.3.1大肠埃希菌检查方法适用性试验
按照《中华人民共和国药典》(2020年版)非无菌产品微生物限度检查:控制菌检查法(通则1106)检查。
阳性对照组:取1:10供试液10 mL(相当于1 g供试品),接种至100 mL胰酪大豆胨液体培养基中,再加入1 mL大肠埃希菌菌液(不大于100 CFU/mL),混匀,30~35℃培养18 h。取上述培养物1 mL接种至100 mL麦康凯液体培养基中,42~44℃培养24 h。取麦康凯液体培养物划线接种于麦康凯琼脂培养基平板上,30~35℃培养18 h。
阴性对照组:同阳性对照组操作,以稀释液代替供试液和菌液。
供试品对照组:同阳性对照组操作,以稀释液代替菌液。
2.3.2大肠埃希菌试验结果
对AmB样品进行大肠埃希菌检查方法适用性试验,结果如表1所示。
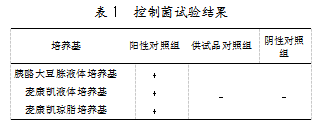
结果显示,阳性对照组检出大肠埃希菌,而供试品对照组和阴性对照组均未检出,表明AmB样品可采用上述方法检出大肠埃希菌。
2.4两性霉素B抑菌活性确定
2.4.1平皿倾注法
试验组:分别取1:10、1:50、1:100的供试液9.9 mL,各加入0.1 mL试验菌菌液,混匀,使供试液含菌量不大于100 CFU/mL。
供试液对照组:取制备好的供试液,以稀释液代替菌液,同试验组操作。
菌液对照组:取pH 7.0氯化钠-蛋白胨缓冲液代替供试液,同试验组操作。
阴性对照组:取pH 7.0氯化钠-蛋白胨缓冲液代替供试液,稀释液代替菌液,同试验组操作。
供试品中微生物的回收:
需氧菌总数:取各组制备的试液1 mL于90 mm无菌平皿中,注入15~20 mL温度不超过45℃的TSA,混匀,待凝固后倒置培养(黑曲霉正置培养)。在30~35℃条件下,金黄色葡萄球菌、铜绿假单胞菌、枯草芽孢杆菌培养不超过3 d;白色念珠菌、黑曲霉培养不超过5 d。
霉菌和酵母菌总数:试验菌种白色念珠菌和黑曲霉,取各组制备的试液1 mL于90 mm无菌平皿中,注入15~20 mL温度不超过45℃的SDA,混匀,凝固后,于20~25℃培养不超过5 d。
针对每一试验菌株,平行制备2个平皿培养基,以平均数计数。
试验菌回收率计算方法:(试验组菌落数-供试品对照组菌落数)/菌液对照组菌落数×100%,回收率在0.5~2。
2.4.2平皿倾注法试验结果
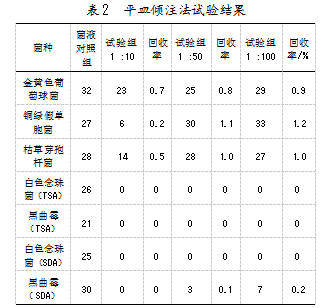
考察AmB样品的不同稀释级别:阴性对照组无菌落生长;供试品对照组无菌落生长。菌液对照组和试验组结果如表2所示。
研究发现,菌液对照组菌落数不大于100 CFU/mL,符合要求。由于两性霉素B样品为黄色粉末,当供试品稀释级为1:10时,平皿中颜色较深,影响菌落观察计数,故排除1:10稀释级。当供试品稀释级为1:50、1:100时,平皿中颜色较浅,不影响菌落观察计数。试验组培养3 d,金黄色葡萄球菌、铜绿假单胞菌、枯草芽孢杆菌在TSA上长出菌落,且回收率合格(为0.5~2),说明细菌对两性霉素B不敏感;试验组在TSA和SDA上培养5 d,白色念珠菌和黑曲霉回收率不合格,说明AmB对白色念珠菌和黑曲霉具有较强的抑制作用。白色念珠菌和黑曲霉是试验敏感菌。根据《中华人民共和国药典》的规定,在不影响试验结果判断的前提下,采用能使微生物生长的更高稀释级供试液进行计数方法适用性试验,选定供试品稀释级为1:50。
2.5抗菌活性的去除或灭活
因AmB具有抗真菌活性,且白色念珠菌和黑曲霉为试验敏感菌,以下试验以敏感菌为试验菌。
2.5.1稀释法
2.5.1.1稀释法试验过程
通过提高供试品稀释级别和增加培养基体积去除AmB抗真菌活性。采用TSA培养基,供试品稀释级别为1:500和1:1 000,分别采用90 mm平皿(注入15~20 mL培养基)和120 mm平皿(注入27~36 mL培养基),其他同2.4.1。
因霉菌和酵母菌总数微生物限度标准为不超过100 CFU/g,供试品稀释级别大于1:100时得出的结果参考意义不大。因此,未用SDA进行试验。
2.5.1.2稀释法试验结果
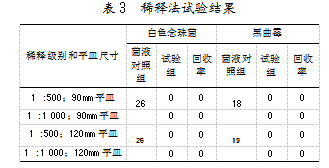
采用稀释法培养5 d,阴性对照组和供试品对照组均无菌落生长。菌液对照组和试验组的结果如表3所示。
研究发现,菌液对照组菌落个数不大于100CFU/mL,符合要求。试验组中白色念珠菌和黑曲霉回收率均为0,说明稀释法未去除AmB抑菌活性。
2.5.2中和法
聚山梨酯80、卵磷脂和组氨酸等作为常用中和剂,对微生物细胞膜可起到保护作用[9]。因此,试验尝试用3%聚山梨酯80,0.3%卵磷脂和0.1%组氨酸比例的中和剂,消除药品的抗真菌活性。
2.5.2.1中和法试验过程
采用的培养基为加入中和剂的TSA和SDA。供试品稀释级别为1:50(SDA)、1:500和1:1 000(TSA),每一试验菌株每种培养基平行制备2个平皿。另外,设置中和剂对照组,确认试验有效性和对微生物的无毒性。中和剂对照组的菌落数与菌液对照组的菌落数比值应为0.5~2,其他同2.4.1。
2.5.2.2中和法试验结果
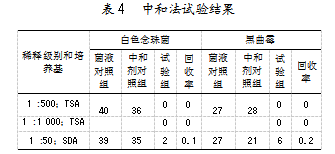
采用中和法培养5 d,阴性对照组和供试品对照组均无菌落生长。菌液对照组和试验组结果如表4所示。
研究发现,菌液对照组菌落个数都不大于100 CFU/mL,符合要求。中和剂对照组的白色念珠菌和黑曲霉的菌落数与菌液对照组的菌落数相差不大,比值为0.5~2,确认中和剂无毒性。1:500和1:1 000试验组在TSA培养基上,白色念珠菌和黑曲霉回收率为0;1:50试验组在SDA培养基上,白色念珠菌回收率为0.1、黑曲霉回收率为0.2,回收率均不合格,说明通过中和法未将AmB抑菌活性去除。
2.5.3中和剂法-薄膜过滤法
尝试用3%聚山梨酯80,0.3%卵磷脂和0.1%组氨酸比例的中和剂和薄膜过滤法联用的方式,消除药品的抗真菌活性。
2.5.3.1中和剂法-薄膜过滤法试验过程
试验组:取1:50和1:500的供试液1 mL,进行薄膜过滤处理,用pH 7.0无菌氯化钠-蛋白胨缓冲液(含1%吐温80)冲洗滤膜。每膜冲洗量1 000 mL(每次冲洗量为100 mL)。在最后一次冲洗液中加入1 mL不大于100 CFU/mL的试验菌液。
阴性对照组:取稀释缓冲液1 mL,在最后一次冲洗液中加入1 mL稀释液,其他同上。
供试品对照组:取1:50和1:500供试液各1 mL,在最后一次冲洗液中加入1 mL稀释液,其他同上。
菌液对照组:用pH 7.0氯化钠-蛋白胨缓冲液代替供试液及冲洗液,按试验组操作加入试验菌进行实验。
中和剂对照组:用含中和剂的稀释液代替供试液,按试验组操作加入试验菌进行实验。
将滤膜贴至TSA(供试品稀释级1:500)和SDA(供试品稀释级1:50)平板上,菌面朝上。
TSA培养基培养温度30~35℃,SDA培养基培养温度20~25℃,培养时间不超过5 d,计数。
2.5.3.2中和剂法-薄膜过滤法试验结果
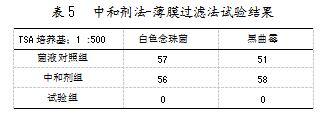
1:50供试液的薄膜过滤法过滤不动,SDA组无数据。1:500供试液薄膜过滤完后贴在TSA平皿上,培养5 d,发现阴性对照组和供试品对照组均无菌落生长。菌液对照组、中和剂组和试验组结果如表5所示。
研究显示,菌液对照组菌落个数都不大于100 CFU/mL,中和剂对照组白色念珠菌和黑曲霉的菌落数与菌液对照组的菌落数相差不大,比值在0.5~2,确认中和剂无毒性。试验组在TSA上无菌落长出,回收率为0,说明通过中和剂法-薄膜过滤法未去除AmB抑菌活性。
2.5.4 MPN法
虽然《中华人民共和国药典》指出,MPN法不适用于霉菌计数,但研究仍采用该方法展开了相关检查。
2.5.4.1 MPN法试验过程
试验组:取制备好的1:103的供试品2份分装于无菌试管,每管9.9 mL;分别向试管中加入制备好的104 CFU/mL黑曲霉和白色念珠菌各0.1 mL,混匀,使供试液含菌量不大于100 CFU/mL。依次进行10倍稀释,共3个连续稀释级,每一个稀释级取3份各1 mL分别接种于3管装有9~10 mL TSB。
供试品对照组:取1:103、1:104和1:105稀释级,各取3份各1 mL分别接种于3管装有9~10 mL的TSB的接种管中。
菌液对照组:取pH 7.0氯化钠-蛋白胨缓冲液代替供试液,按照试验组的操作加入试验菌。依次进行10倍稀释,共3个连续稀释级,每一个稀释级均取3份各1 mL分别接种于3管装有9~10 mL TSB的接种管中。
阴性对照组:取3份pH 7.0氯化钠-蛋白胨缓冲液各1 mL,分别接种于3管装有9~10 mL TSB的接种管中。
接种管于30~35℃培养不超过3 d,逐日观察各管的微生物生长情况。因供试品呈黄色且难溶,结果难以判断,试验将培养物转接至TSA,在相同条件下培养1~2 d,观察是否有微生物生长。
2.5.4.2 MPN法试验结果
在TSA上,各组生长结果如下(管数)。
阴性对照组0,0,0;供试品对照组0,0,0;试验组:白色念珠菌0,1,0;黑曲霉0,0,0;菌液对照组:白色念珠菌3,3,1;黑曲霉3,2,0。
扩大100倍前,菌液对照组白色念珠菌460MPN/g,95%置信限90~1 980 MPN/g,试验组白色念珠菌3 MPN/g,未在90~1 980 MPN/g范围内;菌液对照组黑曲霉93 MPN/g,95%置信限18~360 MPN/g,试验组黑曲霉<3 MPN/g,未在18~360 MPN/g范围内,试验组菌数在菌液对照组菌数的95%置信限外。重复其他2批次样品,结果均为试验组菌数在菌液对照组菌数的95%置信限外,说明MPN法不适用。
2.5.5自制中和剂法
采用公司自制中和剂,供试品稀释级别1:50,阴性对照组和供试品对照组菌落数均为0。菌液对照组和试验组结果如表6所示。
研究发现,菌液对照组菌落个数都不大于100 CFU/mL,中和剂对照组白色念珠菌和黑曲霉的菌落数与菌液对照组的菌落数相差不大,在0.5~2范围内,确认中和剂无毒性。
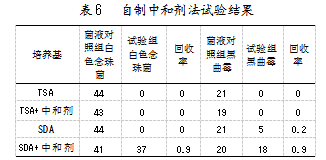
利用TSA培养基或TSA+中和剂,试验组白色念珠菌和黑曲霉不生长;利用SDA培养基,试验组白色念珠菌和黑曲霉回收率不合格;利用SDA+中和剂培养基,试验组白色念珠菌和黑曲霉回收率达0.9,合格。结果表明,该中和剂部分消除了两性霉素B对敏感菌的抑制作用。对其他2批次进行重复试验,利用SDA+中和剂培养基,白色念珠菌和黑曲霉回收率均合格,说明AmB霉菌和酵母菌总数可采用该法进行微生物限度检查。
3结论
由于两性霉素B是抗真菌药物,采用常规方法进行微生物限度方法学验证时,白色念珠菌和黑曲霉的回收率不符合《中华人民共和国药典》的要求。选用公司自制的中和剂后,可部分消除供试品的抑菌活性,使白色念珠菌和黑曲霉在添加中和剂的SDA上回收率合格,且中和剂经验证对微生物无毒性。查阅相关文献,推测中和剂的作用原理是加入富有游离的巯基,使蛋白分子间形成二硫键网络,并通过疏水作用和氢键负载疏水性抗菌药物AmB,将AmB包裹在蛋白分子间,减少与微生物细胞膜的接触,部分消除AmB的抗真菌活性。根据《中华人民共和国药典》要求,在计数方法适用性试验中,若采用各方法仍存在一株或多株试验菌回收率达不到要求的现象,则选择回收最接近要求的方法和试验条件进行供试品检查。最终选择以下方法进行微生物计数。
取1:50供试液1 mL,接种于含0.1%中和剂的SDA中,依法检查霉菌和酵母菌总数。取1:50供试液1 mL,接种于TSA中,依法检查,将菌落总数与霉菌和酵母菌总数之和计作需氧菌总数。按照非无菌产品微生物限度检查法微生物计数法(四部通则1105)检查,供试品中需氧菌总数不得过103 CFU/g,霉菌和酵母菌总数不得过102 CFU/g。取1:10供试液10 mL,接种至100 mLTSB中,按照非无菌产品微生物限度检查法控制菌检查法(四部通则1106)检查,每1 g供试品中不得检出大肠埃希菌。
参考文献
[1]黄志伟,张菁.两性霉素B临床药理研究概述[J].中国真菌学杂志,2021,16(3):188-193,210.
[2]卢贵全,沙嫣懿,张军民,等.两性霉素B抗真菌治疗进展[J].中国真菌学杂志,2022,17(3):247-250.
[3]宋明华.临床应用的两性霉素B活性及毒性研究进展[J].生物化工,2022,8(5):166-169.
[4]杨虹.抗深部真菌药两性霉素B的研究进展[J].中国医疗前沿,2009,4(8):3-4.
[5]王春晖,叶晓芬,吕迁洲.两性霉素B脂质体治疗肺真菌病的疗效及安全性[J].上海医药,2016,37(1):39-42.
[6]国家药典委员会.中华人民共和国药典(2020年版)[M].北京:中国医药科技出版社.2020.
[7]蒋波,刘冬玲,刘浩.西罗莫司胶囊微生物限度方法学适用性试验的研究[C]//中国药学会(Chinese Pharmaceutical Association).中国药学会第四届药物检测质量管理学术研讨会资料汇编.上海市食品药品检验所,2017.
[8]张翠所,高燕霞.两性霉素B阴道泡腾片微生物限度检查方法探讨[J].中国药品标准,2015,16(1):27-30.
[9]张光华,余立.聚山梨酯80和卵磷脂在化学药微生物限度检查时的中和作用[J].药物分析杂志,2008,28(7):1127-1130.










