负载聚六亚甲基双胍的壳聚糖温敏水凝胶敷料对几种普通伤口常见致病菌的抗菌特性研究论文
2026-04-09 16:25:40 来源: 作者:xuling
摘要:普通伤口感染防控是全球公共卫生领域的重大挑战之一。文章以普通伤口的常见致病菌及其混菌为目标,探讨了负载聚六亚甲基双胍(PHMB)的壳聚糖温敏水凝胶的抗菌性能。
摘要:普通伤口感染防控是全球公共卫生领域的重大挑战之一。文章以普通伤口的常见致病菌及其混菌为目标,探讨了负载聚六亚甲基双胍(PHMB)的壳聚糖温敏水凝胶的抗菌性能。研究表明,PHMB在水凝胶中缓释性良好,6 h释放率可达79.9%;PHMB质量浓度提升可显著增强水凝胶的抑菌及杀菌作用。当PHMB负载量为1 mg/mL时,水凝胶敷料对大肠杆菌、金黄色葡萄球菌、铜绿假单胞菌及白色念珠菌具有良好的抑菌作用,且可在30 s内完全杀灭大肠杆菌、金黄色葡萄球菌和铜绿假单胞菌,30 min内完全杀灭白色念珠菌。该水凝胶敷料对模拟普通伤口的混菌也有良好的抑菌作用,可在30 min内实现100%杀菌。研究结果为开发高效抗菌伤口敷料提供了重要参考。
关键词:壳聚糖;水凝胶;普通伤口;聚六亚甲基双胍;抑菌
我国每年因创伤就医者约6 200万人次,产生的直接医疗费用达650亿元人民币[1]。其中,摩擦、切割及烧灼等造成的普通伤口是临床常见的组织损伤类型[2]。伤口愈合是一个复杂的生理过程,常因细菌感染受阻,形成慢性伤口、导致组织修复延迟,甚至引发全身性并发症[3]。普通伤口常见的致病菌包括金黄色葡萄球菌、大肠杆菌、铜绿假单胞菌、白色念珠菌等[4-5]。这些细菌通过在创面形成生物膜、释放毒素和产生耐药性,引发持续性炎症反应,破坏组织修复进程[6]。目前,普通伤口的感染防控是全球公共卫生领域的重大挑战之一。敷料在伤口管理中发挥重要作用,不仅可为受伤组织提供必要的物理保护,更是调控伤口微环境、阻断感染链的关键工具[7]。尽管传统敷料(如纱布、泡沫敷料等)在吸收渗液和维持湿润环境方面具有一定效果,但其仍缺乏主动抗菌功能,难以应对高感染风险环境,因此亟须开发兼具物理防护与高效抑菌性能的新型敷料。
近年来,水凝胶敷料因3D网状结构、高含水率(模拟细胞外基质)和良好的生物相容性,成为创面护理领域的研究热点[8]。其中,壳聚糖温敏水凝胶因具有良好的生物相容性、适应性和可控制药物释放能力等引起了广泛关注[9]。然而,仅基于壳聚糖的水凝胶敷料的抗菌性能仍相对有限,亟须通过负载抗菌剂赋予其功能性。例如,Ansari等[10]构建了负载薄荷精油的壳聚糖水凝胶,有效增强了水凝胶对白色念珠菌、大肠杆菌和金黄色葡萄球菌的抗菌作用;Ni等[11]将Ag MoF添加到壳聚糖中形成抗菌层,并与聚乙烯醇/藻酸钠分离层组装,形成的双层抗菌敷料在体外抗菌和小鼠实验中均对金黄色葡萄球菌和大肠杆菌展现出了良好的抗菌作用,显著促进了伤口愈合。
聚六亚甲基双胍(Polyhexamethylene biguanide,PHMB)是一种阳离子表面活性剂,具有优良的杀菌性能、环境稳定性和安全性[12],可与细菌细胞壁相互作用[13],或吸附在磷脂双层膜上[14],通过与DNA磷酸骨架相互作用阻止DNA复制和修复[15],达到抑菌目的。PHMB常被用作革兰氏阳性和革兰氏阴性细菌、病毒、真菌、酵母菌的优良抗菌剂[16]。研究表明,将PHMB负载于伤口敷料中,有助于提高敷料的抗菌性能[17]。Li等[18]将负载PHMB的透明质酸水凝胶应用于糖尿病伤口修复,发现该混合水凝胶具有优秀的抗菌性能,对大肠杆菌和金黄色葡萄球菌的抑菌率高达97.85%和98.56%。Dilamian等[19]发现,在壳聚糖/聚氧乙烷中负载PHMB制得的静电纺丝纳米纤维膜对大肠杆菌和金黄色葡萄球菌有良好的抑菌作用。但当前相关研究多围绕对敷料常见致病菌(如金黄色葡萄球菌、大肠杆菌)的杀灭作用展开,与实际伤口表面共存的多种微生物组成存在明显区别,导致所制备的敷料在实际伤口中的应用不佳。
本研究就前期构建的负载不同质量浓度PHMB的壳聚糖温敏水凝胶敷料的抑菌特性展开研究。在探讨敷料PHMB缓释特性的基础上,以普通伤口中常见的4种致病菌(大肠杆菌、金黄色葡萄球菌、铜绿假单胞菌和白色念珠菌)为对象,研究PHMB质量浓度对单一菌株和混合菌的抑菌及杀菌作用,为开发具有优良抗菌性能的壳聚糖基水凝胶伤口敷料提供参考。
1材料和方法
1.1试验材料
1.1.1菌株
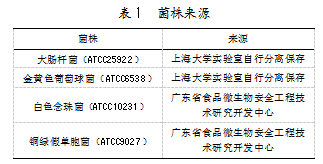
试验所用菌株来源如表1所示。
1.1.2试剂
壳聚糖(CS,CAS:9012-76-4,脱乙酰度为≥95%,黏度100~200 mPa·s,Mw≈161 kDa);壳聚糖季铵盐(HACC,脱乙酰度>95%),购自酷尔化学科技(北京)有限公司;β-甘油磷酸钠五水合物(β-GP,CAS:13408-09-8,纯度>95%),购自上海阿拉丁生化科技股份有限公司;聚六亚甲基双胍(PHMB,CAS:27083-27-8,纯度为99%)、碳酸氢钠(NaHCO3,分析纯)、氯化钠(NaCl,分析纯),购自国药集团化学试剂有限公司;营养肉汤、营养琼脂、沙氏葡萄糖液体培养基、马铃薯葡萄糖琼脂培养基、CAMHB肉汤、Mueller-Hinton琼脂,购自青岛高科园海博生物技术有限公司。
1.2设备与仪器
精密分析天平(PWC254),购自上海越平科学仪器有限公司;打孔器(6孔),购自得力集团有限公司;立式压力蒸汽灭菌器(YXQ-75G),购自上海博迅实业有限公司医疗设备厂;隔水式恒温培养箱(GHP),购自上海一恒科学仪器有限公司;恒温培养摇床(THZ),购自上海一恒科学仪器有限公司;无菌操作台(VD-850),购自上海沪净实业有限公司;浊度比较仪(ZDY-Ⅱ),购自上海复星佰珞生物科技有限公司;电热恒温鼓风干燥箱(102-2A),购自上海慧泰仪器制造有限公司;细菌培养皿和细胞培养板(直径90 mm、48孔),购自广州洁特生物过滤股份有限公司;紫外分光光度计(UV 9100D),购自北京莱伯泰科仪器股份有限公司。
1.3试验方法
1.3.1负载PHMB的壳聚糖温敏水凝胶的制备
参照Yao等[20]的方法制备壳聚糖温敏水凝胶。
称取一定量的CS和HACC粉末(10:2),溶于0.1 mol/L醋酸溶液,室温磁力搅拌至完全溶解。在冰浴及磁力搅拌条件下,向CS/HACC溶液中逐滴加入一定量的0.1 mol/L NaHCO3溶液,使体系中NaHCO3溶液最终质量浓度为5.6%。磁力搅拌2 min,向CS/HACC/NaHCO3溶液中逐滴加入一定量的β-GP溶液,使体系中β-GP溶液的最终质量浓度为7%。搅拌30 min,将得到的CS/HACC/NaHCO3/β-GP温敏水凝胶溶液置于4℃冰箱静置1 h。
准确称取100 mg PHMB,溶于10 mL去离子水中,得到10 mg/mL的PHMB溶液。稀释10倍,得到1 mg/mL的PHMB溶液。在冰浴及磁力搅拌条件下,将1 mL不同质量浓度的PHMB溶液加入9 mL CS/HACC/NaHCO3/β-GP温敏水凝胶溶液中,使体系中PHMB溶液的最终质量浓度为0.1 mg/mL和1 mg/mL,磁力搅拌30min,将得到的温敏水凝胶溶液于4℃冰箱静置1h,分别记为CS-0.1PHMB和CS-1PHMB。不含PHMB的壳聚糖温敏水凝胶记为CS-0PHMB。
1.3.2负载PHMB的壳聚糖的药物缓释能力
采用紫外分光光度计,参照Walker等[21]的方法并稍作修改,在235 nm波长处评估PHMB从温敏水凝胶中的释放特性。步骤如下:将2 mL壳聚糖温敏水凝胶溶液在37℃下放置30 min,完全形成凝胶后,加入50 mL磷酸盐缓冲液(PBS),37℃、100 r/min恒温摇床分别振荡30 min、1 h、2 h、3 h、4 h、5 h、6 h后,收集3 mL上清液,测量其在235 nm处的吸光度。同时,向体系中补充3 mL PBS,使液体总体积保持不变。将吸光度代入PHMB标准曲线确定溶液质量浓度,并按下式计算PHMB的累积药物释放率[22]。
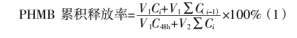
式中:V1为PBS液体的总体积(50 mL);V2为收集的上清液体积(3 mL);Ci为PHMB在第i小时的质量浓度;C48h为PHMB在48 h时测得的质量浓度。
1.3.3负载PHMB的壳聚糖温敏水凝胶的抑菌性能
参考GB/T 20944.1-2007[23],以琼脂平皿扩散法检测定性负载PHMB的壳聚糖敏温敏水凝胶对4种致病菌和模拟伤口混菌的抑菌作用。培养基、去离子水、0.9%氯化钠溶液和玻璃器皿等均在121℃下灭菌15 min,备用。
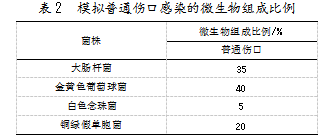
菌液制备:采用直接菌悬液法制备大肠杆菌、金黄色葡萄球菌、白色念珠菌、铜绿假单胞菌的菌液[24]。活化的大肠杆菌、金黄色葡萄球菌、铜绿假单胞菌在营养琼脂平板上培养18~24 h;白色念珠菌在马铃薯葡萄糖琼脂培养基上培养18~24 h。分别挑取各菌的单菌落置于10 mL无菌0.9%氯化钠溶液中,调整活菌浓度为1.5×108 CFU/mL(0.5 McF)。模拟普通伤口感染的混合菌悬液的制备:将上述1.5×108 CFU/mL的纯菌悬液按照表2的体积比混匀。
琼脂菌板制备:分别将200μL各菌的菌悬液(1.5×108 CFU/mL)滴加于Mueller-Hinton琼脂平板上,涂布均匀并静置3~5 min;将CS-0PHMB、CS-0.1PHMB、CS-1PHMB凝胶(高2 mm,直径8 mm)依次置于Mueller-Hinton琼脂平板,37℃倒置培养24 h后,记录抑菌圈直径。
1.3.4负载PHMB的壳聚糖温敏水凝胶的杀菌性能
参照Zheng[25]和Dong[26]的方法,以平板菌落计数法测定水凝胶的表面杀菌特性。将200μL的CS-0PHMB、CS-0.1PHMB、CS-1PHMB溶液分别注入48孔板,37℃孵育30 min,形成凝胶。在水凝胶表面滴加10μL菌悬液(1.5×108 CFU/mL),37℃分别孵育30 s、1 min、15 min、30 min、1 h,向试验孔中加入1 mL无菌0.9%氯化钠溶液重悬细菌,吸取100μL(大肠杆菌、金黄色葡萄球菌、铜绿假单胞菌、普通伤口混菌)的菌悬液于营养琼脂平板,白色念珠菌滴加于马铃薯葡萄糖琼脂平板,37℃培养18 h后进行菌落计数。将10μL菌悬液加入1 mL无菌PBS溶液中作为对照组。表面杀菌率计算公式如下。

1.4数据分析
所有试验均进行3次平行,结果以平均值±标准差表示。应用SPSS 26.0软件对结果进行单因素方差分析(ANOVA)和显著性检验,P<0.05表示差异具有统计学意义。应用Origin 2021软件进行图形绘制。
2结果与分析
2.1负载PHMB的壳聚糖温敏水凝胶的药物释放性能
负载PHMB的壳聚糖温敏水凝胶在37℃孵育6 h的PHMB的释放曲线如图1所示。
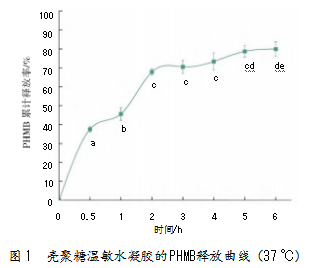
结果表明,壳聚糖温敏水凝胶中的PHMB在孵育过程中释放良好。在最初的2 h内,水凝胶中的PHMB迅速释放,累积释放率达67.9%,随后趋于稳定,并维持在70%以上;6 h时,PHMB的释放率进一步增加至79.9%,表明PHMB在水凝胶中释放效率较高。这与Dilamian等[19]的研究结果相符,证实壳聚糖水凝胶的3D网络结构延长了PHMB的释放过程并确保了其安全性[27],有助于迅速抑制伤口表面细菌生长,最终达到杀菌的目的。
2.2负载PHMB的壳聚糖温敏水凝胶的抑菌作用
负载不同质量浓度PHMB的壳聚糖温敏水凝胶对大肠杆菌、金黄色葡萄球菌、铜绿假单胞菌和白色念珠菌的抑菌作用如图2所示。
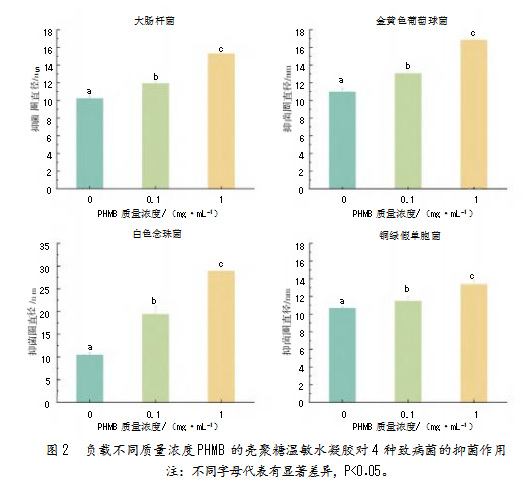
结果显示,基于壳聚糖及壳聚糖季铵盐,对照组(壳聚糖温敏水凝胶,CS-0PHMB)对大肠杆菌、金黄色葡萄球菌、铜绿假单胞菌均有一定的抑菌作用,抑菌圈直径为10.23~11.82 mm,但对白色念珠菌几乎无抑制作用。添加PHMB能增强水凝胶的抑菌效果,且随着PHMB质量浓度升高,壳聚糖温敏水凝胶对各致病菌的抑制作用相对增强,抑菌圈直径增大。例如,添加1 mg/mL的PHMB,大肠杆菌、白色念珠菌、铜绿假单胞菌和金黄色葡萄球菌的抑菌圈直径分别增加至15.29、28.88、13.35和16.82 mm。PHMB显著增强了壳聚糖温敏水凝胶对白色念珠菌的抑制作用。作为一种聚合物双胍,PHMB的亲水基具有强烈的正电性,易与细菌负电性的细胞壁组分相互作用,转移至细胞质和细胞质磷脂,导致微生物死亡[28]。
2.3负载PHMB的壳聚糖温敏水凝胶对4种致病菌的灭杀作用
进一步研究负载PHMB的壳聚糖温敏水凝胶对4种致病菌的杀菌效果,结果如图3所示。
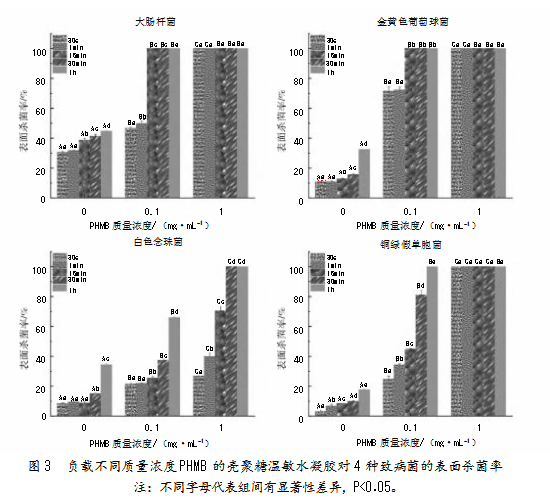
数据表明,PHMB质量浓度与壳聚糖温敏水凝胶对4种致病菌的表面杀菌率密切相关。不含PHMB的壳聚糖温敏水凝胶(CS-0PHMB)对各菌的杀菌率均较低,即使作用1 h,CS-0PHMB对大肠杆菌、金黄色葡萄球菌、白色念珠菌和铜绿假单胞菌的表面杀菌率也仅为44.75%、32.49%、34.38%和17.64%。添加PHMB有效增强了壳聚糖温敏水凝胶的杀菌能力。随PHMB质量浓度增加,水凝胶对上述4株致病菌的灭杀能力明显增强。例如,CS-1PHMB凝胶作用30 s即可100%杀灭大肠杆菌、金黄色葡萄球菌和铜绿假单胞菌;作用30 min时,对白色念珠菌的表面杀菌率也能达到100%。
此外,同等PHMB质量浓度下,延长接触时间也会提高该水凝胶对致病菌的表面杀菌率。例如,接触1 min后,CS-0.1PHMB凝胶对大肠杆菌、金黄色葡萄球菌、白色念珠菌、铜绿假单胞菌的杀灭率可达49.83%、72.3%、21.93%、34.32%;接触15 min,CS-0.1PHMB凝胶对大肠杆菌、金黄色葡萄球菌的杀灭率已达100%,但对白色念珠菌和铜绿假单胞菌的杀灭率仍相对较低,分别为25.38%、44.80%;继续延长作用时间至1 h,则对白色念珠菌和铜绿假单胞菌的杀菌能力提升至65.97%和100%。负载PHMB的壳聚糖温敏水凝胶敷料表现出持续且高效的杀菌能力,这与其药物释放特性的结果相符。对比发现,含1 mg/mL PHMB的壳聚糖温敏水凝胶对4种致病菌均有快速高效的杀灭能力。
2.4负载PHMB的壳聚糖温敏水凝胶对模拟普通伤口混菌的抑制作用
为进一步验证负载PHMB的壳聚糖温敏水凝胶敷料在实际伤口感染控制中的作用,试验以普通伤口常见的菌相组成为例展开研究。负载不同PHMB质量浓度的壳聚糖温敏水凝胶对普通伤口模拟混菌的抑菌作用如图4所示。
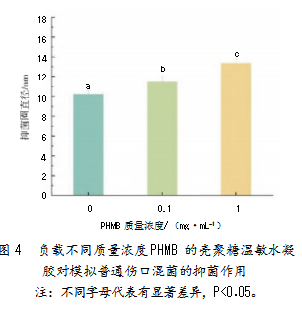
结果表明,壳聚糖温敏水凝胶敷料负载的PHMB质量浓度对普通伤口模拟混菌的抑制作用有显著影响,随着PHMB质量浓度增大,温敏水凝胶对普通伤口混菌的抑制能力增强。CS-0PHMB对混菌的抑制作用相对较弱,抑菌圈直径仅为10.21 mm;CS-1PHMB温敏水凝胶的抑菌作用显著增强,抑菌圈直径扩大至13.33 mm。但与对单菌抑制作用相比,水凝胶敷料对混菌的抑制效果仍相对较弱,说明伤口混合菌的抵抗能力更强。伤口混合感染中,多种细菌共存并非简单的物种叠加,而是通过复杂的生物学互作形成协同抗性网络,显著增强菌群对抗菌剂的抵抗能力[29]。
2.5负载PHMB的壳聚糖温敏水凝胶对模拟伤口混菌的杀灭作用
采用表面抗菌实验研究负载不同质量浓度PHMB的壳聚糖温敏水凝胶对模拟普通伤口混菌的杀灭作用,结果如图5所示。
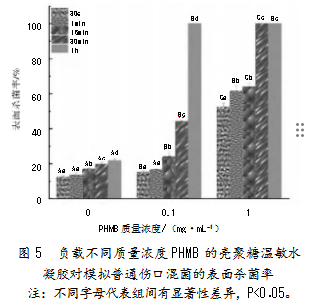
数据表明,壳聚糖温敏水凝胶敷料负载的PHMB质量浓度对模拟普通伤口混菌的杀灭率有重要影响。CS-0PHMB对伤口混菌杀灭率较低,1 h后的表面杀菌率仅为21.79%。负载PHMB有效增强了温敏水凝胶的杀菌能力,随PHMB质量浓度增加,杀菌效果显著增强。例如,作用30 s时,CS-0.1PHMB凝胶的表面杀菌率仅为15.14%,而CS-1PHMB的表面杀菌率已显著升至52.46%;延长至30 min,CS-1PHMB杀菌率可达100%;作用1 h后,负载较低质量浓度PHMB的CS-0.1PHMB也可实现100%杀灭细菌。结果表明,负载CS-1PHMB能应对普通伤口致病菌的复杂情况,实现短时间内杀灭细菌、促进伤口愈合的目标。
3结论
为预防普通伤口感染,本文以普通伤口常见的4种致病菌及其混菌为目标,研究了负载PHMB的壳聚糖温敏水凝胶的抗菌性能。结果表明,该水凝胶能够在6 h释放79.9%的PHMB,并维持稳定释放,有效延长抗菌作用时间。抑菌实验证明,PHMB质量浓度增加可显著增强水凝胶的抑菌及杀菌作用,当PHMB质量浓度达1 mg/mL时,水凝胶对大肠杆菌、金黄色葡萄球菌、铜绿假单胞菌及白色念珠菌均表现出显著的抑菌作用。该水凝敷料可在30 s内完全杀灭大肠杆菌、金黄色葡萄球菌和铜绿假单胞菌,30 min内完全杀灭白色念珠菌,同时对普通伤口混菌也有良好的抑菌效果,能在30 min内实现100%杀菌。研究成果为负载PHMB的壳聚糖温敏水凝胶在普通伤口上的应用提供了有益参考。
参考文献
[1]JIANG B,LIANG S,PENG Z R,et al.Transport and public health in China:The road to a healthy future[J].Lancet,2017,390(10104):1781-1791.
[2]蒋琪霞.创伤性伤口感染处理现况及应对策略[J].创伤外科杂志,2019,21(6):401-404.
[3]RAJU N R,SILINA E,STUPIN V,et al.Multifunctional and smart wound dressings-A review on recent research advancements in skin regenerative medicine[J].Pharmaceutics,2022,14(8):1574.
[4]CHELKEBA L,MELAKU T.Epidemiology of staphylococci species and their antimicrobial-resistance among patients with wound infection in Ethiopia:A systematic review and meta-analysis[J].Journal ofGlobal Antimicrobial Resistance,2022,29:483-498.
[5]MOHAMMEDAMAN M,ALEMSEGED A,TSEGAYE S.Antimicrobial susceptibility pattern of bacterial isolates from wound infection and their sensitivity to alternative topical agents at Jimma University Specialized Hospital,South-West Ethiopia[J].Annals of Clinical Microbiology and Antimicrobials,2014,13(1):14.
[6]WARDLAW J L,SULLIVAN T J,LUX C N,et al.Photodynamic therapy against common bacteria causing wound and skin infections[J].Veterinary Journal,2012,192(3):374-377.
[7]沈佳斌,朱怡蓉,杨金花,等.高性能慢性伤口敷料的研究进展[J].四川师范大学学报(自然科学版),2025,48:143-153,140.
[8]MALEKI A,HE J,BOCHANI S,et al.Multifunctional photoactive hydrogels for wound healing acceleration[J].ACS Nano,2021,15(12):18895-18930.
[9]GU R,ZHOU H,ZHANG Z,et al.Research progress related to thermosensitive hydrogel dressings in wound healing:A review[J].Nanoscale Advances,2023,5(22):6017-6037.
[10]ANSARI M,MEFTAHIZADEH H,ESLAMI H.Physical and antibacterial properties of Chitosan-guar-peppermint gel for improving wound healing[J].Polymer Bulletin,2023,80(7):8133-8149.
[11]NI Y,WANG R,ZHANG W,et al.Graphitic carbon nitride(g-C3N4)-based nanostructured materials for photodynamic inactivation:Synthesis,efficacy and mechanism[J].Chemical Engineering Journal,2021,404.
[12]王奎涛,王玉亚,任欢欢,等.聚六亚甲基双胍消毒剂含量测定方法及消毒效果的研究[J].应用化工,2019,48(6):1506-1509.
[13]KUROKI A,TCHOUPA A K,HARTLIEB M,et al.Targeting intracellular,multi-drug resistant Staphylococcus aureus with guanidinium polymers by elucidating the structure-activity relationship[J].Biomaterials,2019,217:119249.
[14]HORNER I J,KRAUT N D,HURST J J,et al.Effects of polyhexamethylene biguanide and polyquaternium-1 on phospholipid bilayer structure and dynamics[J].Journal of Physical Chemistry B,2015,119(33):10531-10542.
[15]SOWLATI-HASHJIN S,CARBONE P,KARTTUNENM.Insights into the polyhexamethylene biguanide(PHMB)mechanism of action on bacterial membrane and DNA:A molecular dynamics study[J].Journal of Physical Chemistry B,2020,124(22):4487-4497.
[16]SZKOŁUDA P,KARPINSKI T M.Polyhexanide(PHMB)properties and applications in medicine[J].European Journal of Biological Research,2020,10:225-231.
[17]JIN J,CHEN Z L,XIANG Y,et al.Development of a PHMB hydrogel-modified wound scaffold dressing with antibacterial activity[J].Wound Repair and Regeneration,2020,28(4):480-492.
[18]LI Y,ZHENG H,LIANG Y,et al.Hyaluronic acid-methacrylic anhydride/polyhexamethylene biguanide hybrid hydrogel with antibacterial and proangiogenic functions for diabetic wound repair[J].Chinese Chemical Letters,2022,33(12):5030-5034.
[19]DILAMIANM,MONTAZERM,MASOUMI J.Antimicrobial electrospun membranes of chitosan/poly(ethylene oxide)incorporating poly(hexamethylene biguanide)hydrochloride[J].Carbohydrate Polymers,2013,94(1):364-371.
[20]YAO M,CHEN Y,ZHANG J,et al.Chitosan-based thermosensitive composite hydrogel enhances the therapeutic efficacy of human umbilical cord MSC in TBI rat model[J].Materials Today Chemistry,2019,14:100192.
[21]WALKER R M,GILLESPIE B M,THALIB L,et al.Foam dressings for treating pressure ulcers[J].Cochrane Database of Systematic Reviews,2017,(10):CD011332.
[22]LEUNG B,DHARMARATNE P,YAN W,et al.Development of thermosensitive hydrogel containing methylene blue for topical antimicrobial photodynamic therapy[J].Journal of Photochemistry and Photobiology B-Biology,2020,203:111776..
[23]江创生,陈海宏.纺织品抗菌性能评价方法概述[J].纺织标准与质量,2012(3):5.
[24]余兴,孔庆军,任雪艳.3种精油对水果病原菌的抑菌效果研究[J].食品与生物技术学报,2017,36(7):714-719.
[25]ZHENG Z,BIAN S,LI Z,et al.Catechol modified quaternized chitosan enhanced wet adhesive and antibacterial properties of injectable thermo-sensitive hydrogel for wound healing[J].Carbohydrate Polymers,2020,249:116826.
[26]DONG Q,ZHONG X,ZHANG Y,et al.Hyaluronic acid-based antibacterial hydrogels constructed by ahybrid crosslinking strategy for pacemaker pocket infection prevention[J].Carbohydrate Polymers,2020,245(C):116525.
[27]XIONG Y,WANG L,XU W,et al.Electrostatic induced peptide hydrogel containing PHMB for sustained antibacterial activity[J].Journal of Drug Delivery Science and Technology,2022,75:103717.
[28]BUENO C Z,MORAESÅM.Influence of the incorporation of the antimicrobial agent polyhexamethylene biguanide on the properties of dense and porous chitosan-alginate membranes[J].Materials Science and Engineering:C,2018,93:671-678.
[29]周琳,蔡文静,杨慧,等.MTAN用于抑制血链球菌、具核梭杆菌、牙龈卟啉单胞菌混合菌的体外研究[J].安徽医科大学学报,2021,56(8):1328-1331.










