发酵源 N- 乙酰氨基葡萄糖和氨基葡萄糖盐酸盐药代动力学研究论文
2026-04-09 15:34:27 来源: 作者:xuling
摘要:文章集中比较生物发酵来源的N-乙酰氨基葡萄糖(NAG)与氨基葡萄糖盐酸盐(GH)的药代动力学特征。
摘要:文章集中比较生物发酵来源的N-乙酰氨基葡萄糖(NAG)与氨基葡萄糖盐酸盐(GH)的药代动力学特征。在静脉注射与口服给药后,运用液相色谱-二级质谱联用技术(LC-MS/MS)检测SD大鼠血浆药物质量浓度。静脉注射后,NAG的Cmax、MRT0→t、AUC0→t均显著高于GH(P<0.05);口服后,NAG的Cmax、AUC0→t也显著高于GH(P<0.05)。结果表明,相较于GH,NAG在2种给药途径下均具有更好的系统暴露量与吸收速率。
关键词:生物发酵;N-乙酰氨基葡萄糖;氨基葡萄糖盐酸盐;LC-MS/MS;药代动力学
氨基葡萄糖(简称氨糖)是人体关节软骨基质中合成蛋白聚糖的必需物质[1],主要包括氨基葡萄糖盐酸盐(GH)、氨基葡萄糖硫酸盐(GS)与N-乙酰氨基葡萄糖(NAG)等形式。NAG在修复关节软骨、缓解关节疼痛、增强机体免疫力、帮助皮肤补水保湿等方面效用良好[2-4]。临床研究显示,NAG具有较高的吸收利用率,对人体骨关节的作用活性高于GH[5]。相比化学水解法和酶转化法,微生物发酵法具有安全、绿色、成本低、海鲜过敏人群不受限等优势[6]。本文以微生物发酵法生产的NAG和GH为对象,探讨其在大鼠体内的药代动力学特征。
1材料
1.1主要试剂与仪器
食品级RUDDERNAGⓇN-乙酰氨基葡萄糖,含量>98%,批号:DB250326016,购自山东润德生物科技有限公司;氨基葡萄糖盐酸盐,含量>98%,批号:A250226071-1-80,购自山东润德生物科技有限公司;TBTM(三苯甲基胺,内标物质),纯度≥99%,批号:TBTM-001,购自美国Sigma-Aldrich公司;SCIEX ExionLC-TQ5500高效液相色谱-串联质谱仪,购自SCIEX公司;Phenomenex Kinetex C18色谱柱(2.1×50 mm,2.6μm),购自Phenomenex公司。
1.2实验动物
SD大鼠,SPF级,雄性,5~6周龄,体质量(200±20)g,动物合格证号:SCXK(鲁)2022-0006,购自济南朋悦实验动物繁育有限公司。
2方法
2.1溶液配制
2.1.1标准工作液配制
分别配制成30 mg/mL的灌胃工作液和2 mg/mL的静脉注射工作液,现配现用。
2.1.2内标工作液配制
精密称取适量TBTM(三苯甲基胺),用甲酸-乙腈溶液(0.1∶99.9,V∶V)配制成质量浓度200 ng/mL的内标工作液,现配现用。
2.2动物分组、给药方法和样本采集
SD大鼠24只,随机分为4组,每组6只:NAG灌胃组、NAG注射组、GH灌胃组、GH注射组。分别进行灌胃(300 mg/kg)或静脉注射(10 mg/kg)处理,于5、15、30、45、60、120、240、360 min,眼内眦取血置于EP管中,-80℃保存。
2.3样本预处理
取血液样本解冻,1 500 r/min涡旋混匀10 min,取20μL至96孔板,加200μL内标工作液。空白样本加不含TBTM的甲酸-乙腈溶液(0.1∶99.9,V/V)。500 r/min涡旋混匀30 min,离心15 min(8℃,3 500 r/min)。取上清液100μL,置于96孔板,加入纯水100μL,500 r/min涡旋混匀30 min,进样。
2.4 LC-MS/MS条件
色谱条件:色谱柱为Phenomenex C18(2.1×50 mm.2.6μm)。流动相:流动相A,甲酸-水(0.1∶99.9,V/V);流动相B,甲酸-乙腈(0.1∶99.9,V/V)。梯度洗脱:0~0.3 min,5%流动相B;0.3~0.8 min,5%~80%流动相B;0.8~1.5 min,80%流动相B;1.5~1.6 min,80%~5%流动相B;1.6~3 min,5%流动相B。流速为0.5 mL/min;柱温为35℃;进样器温度为15℃;进样体积为2μL。
质谱条件:采用电喷雾离子源(ESI)、正离子模式检测。多反应监测扫描模式(MRM):NAG监测离子m/z 222.1/138.1;GH监测离子对m/z 180.0/162.1;内标监测离子对m/z 271.1/155.1。
2.5数据分析
采用Spass和Origin软件进行数据分析。实验数据以均值±标准差(x±s)表示。采用t检验,P<0.05表示差异显著,P<0.01表示差异极显著。
3结果
3.1 NAG和GH的平均血浆浓度-时间曲线
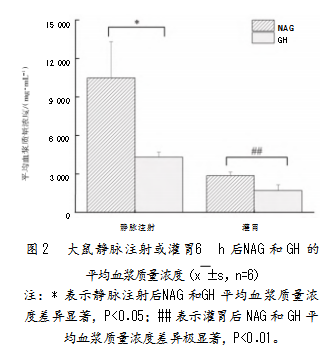
静脉注射与灌胃给药后,NAG在血浆中的驻留时间长于GH。6 h后,NAG平均血浆质量浓度分别为10 479.06±2 828 ng/mL和2 857.35±282 ng/mL,均显著高于GH的4 305.48±399 ng/mL(P<0.05)和1 700.44±446 ng/mL(P<0.01)(见图1、图2)。
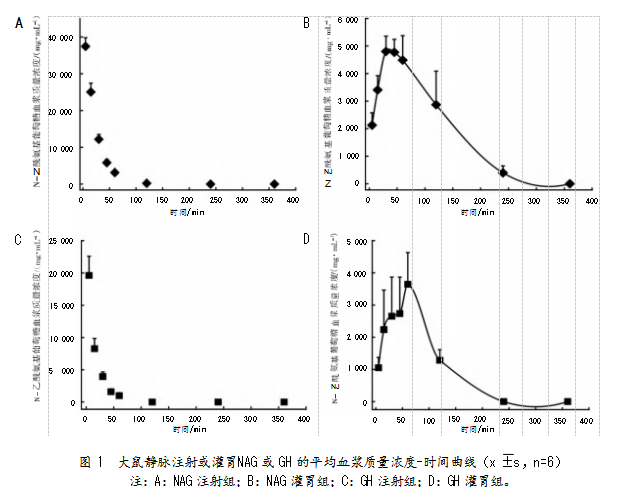
3.2 NAG和GH静脉注射(iv)药代动力学特征
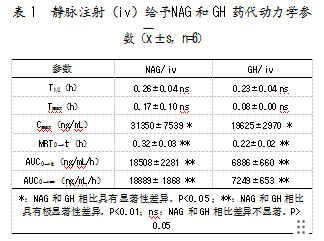
静脉注射NAG的半衰期(T1/2)和达峰时间(Tmax)与GH相比均无显著差异(P>0.05),如表1所示。但NAG的最大血浆质量浓度(Cmax)、平均驻留时间(MRT0→t)、从初始时间0 h到最后一个可测定时间的药物浓度-时间曲线下的面积(AUC0→t)均显著高于GH,分别是GH的1.60、1.45、2.69倍。结果表明,NAG比GH的系统暴露量更大、驻留时间更长、吸收速率更快。
3.3 NAG和GH灌胃(ig)药代动力学特征
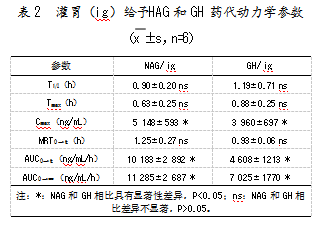
灌胃给药NAG的Cmax与AUC0→t均显著高于GH(P<0.05),分别是GH的1.30倍和2.21倍,表明NAG在大鼠体内的系统暴露量更大,吸收速率更快(见表2)。
4讨论与分析
研究显示,NAG与GH在大鼠体内的药代动力学特征存在显著差异。静脉注射NAG的Cmax、AUC0→t及MRT0→t均显著高于GH,这可能与NAG的乙酰基结构有关—乙酰化修饰可延缓肾小球滤过并减少酶解代谢,延长其在血液中的驻留时间[7];灌胃给药NAG的吸收效率也显著优于GH(P<0.05),可能因为NAG可直接被吸收利用,而GH需先转化为氨基葡萄糖再被吸收[8]。综上,NAG在2种给药途径下均表现出了更优的系统暴露和吸收特性,具有更好的应用潜力。
参考文献
[1]喻斌,刘卓群,柴川,等.给予盐酸氨基葡萄糖和硫酸氨基葡萄糖后的氨基葡萄糖药动学和生物利用度研究[J].中国药理学通报,2019,35(2):278-282.
[2]KEISUKE K.Chitin and chitosan:Functional biopolymers from marine crustaceans[J].Marine Biotechnology(New York,N.Y.),2006,8(3):203-26.
[3]J R,K C,V H,et al.Collagen-induced arthritis:Severity and immune response attenuation using multivalent N-acetyl glucosamine[J].Clinical and Experimental Immunology,2014,177(1):121-133.
[4]KIKUCHI K,MATAHIRA Y.Oral N-acetylglucosamine supplementation improves skin conditions of female volunteers:Clinical evaluation by a microscopic three-dimensional skin surface analyzer[J].Journal of Applied Cosmetology,2002,20(2):143-152.
[5]横井香里.N-ア七チルグルコサミン含有食品の膝関節痛および軟骨代謝マ-カ-に対する効果[J].新薬と臨床(新薬と臨牀),2013,62(9):1758-1768.
[6]刘延峰.代谢工程改造枯草芽孢杆菌高效合成N-乙酰氨基葡萄糖[D].无锡:江南大学,2015.
[7]WANG S S,CHEN C C,Reddy M G,et al.Chemoenzymatic modular assembly of O-GalNAc glycans for functional glycomics[J].Nature Communications,2021,12(1):3573-3573.
[8]ALYSTA P,HARVEY F,JULIA Z,et al.The hexosamine biosynthesis pathway:Regulation and function.[J].Genes,2023,14(4):933.










