二甲基砷胁迫对淹水稻田中古菌群落结构及功能类群的影响论文
2026-04-09 15:20:21 来源: 作者:xuling
摘要:古菌是一类重要的微生物类群,稻田是广古菌门、深古菌门等微生物的特殊栖息地,古菌不仅在砷的迁移转化过程中发挥着重要作用,而且具有多样性功能。
摘要:古菌是一类重要的微生物类群,稻田是广古菌门、深古菌门等微生物的特殊栖息地,古菌不仅在砷的迁移转化过程中发挥着重要作用,而且具有多样性功能。但稻田古菌群落对砷污染的响应机制尚不明确,因此本研究选取浙江嘉兴稻田土壤进行淹水培养,探究不同质量浓度的二甲基砷(DMAs)胁迫对稻田土壤古菌群落组成的影响。结果发现,DMAs胁迫导致土壤pH和溶解性有机碳(DOC)含量显著升高(P<0.05);实时荧光定量PCR结果表明,DMAs胁迫使古菌16S rRNA基因丰度显著降低(P<0.05);高通量测序结果表明,泉古菌门(Crenarchaeota)、纳古菌门(Nanoarchaeaeota)和奇古菌门(Thaumarchaeota)是土壤中的主要古菌门类,深古菌纲(Bathyarchaeia)、沃斯古菌纲(Woesearchaeia)和亚硝化球形菌纲(Nitrososphaeria)是纲水平上的主要古菌类群;主坐标分析(PCoA)表明,DMAs胁迫下稻田古菌群落组成发生了显著变化,Woesearchaeia和Nitrososphaeria是DMAs胁迫下的主要敏感古菌类群。研究结果可为砷污染土壤的生物修复提供一定的理论支撑和实践指导。
关键词:水稻土;二甲基砷;定量PCR;古菌群落
稻田中,砷主要以亚砷酸盐[As(Ⅲ)]的形式存在,其甲基化易加剧[1]。水稻对砷的吸收积累量远超其他作物,会加剧砷经食物链传播的风险[2-3]。尽管甲基砷毒性低于无机砷,但高质量浓度二甲基砷(DMAs)可致水稻患直穗病进而减产[4],该现象在江淮地区时有发生。因水稻自身无砷甲基化能力,其体内甲基砷主要源于土壤微生物作用[5],故研究DMAs对微生物结构的影响对土壤砷污染修复和水稻增产意义重大[6]。古菌作为土壤关键微生物,直接影响着土壤物质代谢和营养转换。土壤重金属污染与微生物群落的相关性是目前国内外学者关注的焦点,尽管不同微生物对重金属的敏感性存在差异,但大部分研究结果显示,重金属对微生物群落多样性影响很大[7]。本研究通过微宇宙土壤培养实验,添加不同质量浓度的DMAs,探究稻田古菌群落响应,旨在为稻田砷污染微生物修复提供理论依据和实践指导。
1材料与方法
实验采用浙江嘉兴水稻土,每组重复取200 g水稻土过孔径2 mm筛选取土样,根据农用地土壤污染风险管制值[8],设空白对照组(CK),60 mg/kg DMAs和120 mg/kg DMAs 3个处理组,各重复4次。土样置锥形瓶,加去离子水混匀,淹水水层保持2 cm。封口膜密封后25℃、180 r/min振荡30 min,接通气装置,25℃避光培养。第0、3、7、14、28、42、56、70、84、98天采样,测孔隙水pH、DOC、砷(CAs)质量浓度及古菌16S rRNA基因丰度,及时补水。实验结束混匀土样保存待测。
2结果与讨论
2.1土壤基本理化性质分析
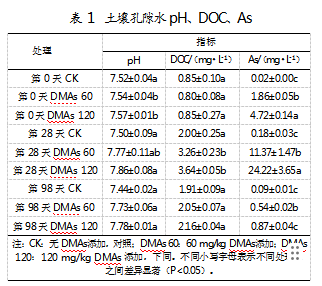
选取第0天、第28天(微生物变化剧烈期)和第98天的实验结果进行分析。结果显示,3个处理组的土壤酸碱度整体呈中性或弱碱性。培养过程中,土壤pH随时间延长逐渐上升,至第28天达到峰值后回落,到第98天趋于稳定。与对照组相比,处理级初始砷质量浓度越高,pH变化幅度越大。第0天时,各处理组土壤孔隙水pH无显著差异(见表1);第28天,添加DMAs后孔隙水pH显著高于对照组,120 mg/kg DMAs处理组土壤孔隙水pH升至7.86。第98天,60 mg/kg和120 mg/kg DMAs处理组的孔隙水pH分别比对照组高出0.29和0.34个单位,但不同质量浓度DMAs处理组的组间差异不显著。结果表明,DMAs胁迫显著提升了土壤孔隙水的pH,可能进一步影响微生物群落组成,包括古菌。在DOC含量方面,第28天,60 mg/kg和120 mg/kg DMAs处理组的土壤DOC含量显著提高,120 mg/kg组略高于60 mg/kg组。DOC含量随时间延长逐步上升,至第28天达到峰值后回落,到第98天趋于稳定。这表明DMAs胁迫显著提高了土壤孔隙水的DOC含量,可能进一步影响微生物群落。在砷质量浓度方面,外源添加DMAs后,土壤砷质量浓度显著增加。随着培养时间延长,砷质量浓度先升至峰值后回落至初始值以下。初始砷质量浓度越高,砷质量浓度增加量越大。总体而言,各处理组的砷质量浓度随时间推移而逐步下降,暗示微生物可能通过脱甲基或气态挥发作用参与砷转化。
2.2土壤中古菌16S rRNA基因丰度
采用QuantStudioTM Real-Time PCR Software v1.3分析基因丰度,用Excel 2019处理数据并制图,用SPSS进行显著性分析。qPCR结果显示,随着循环数增加,扩增产物增加,荧光信号增强,40循环后可达到89.1%的效率。溶解曲线为单峰,表明产物特异性良好。CT值与log拷贝数成反比,标准曲线方程为y=-4.058 8x+47.436,R2=0.999 9,说明log拷贝数与CT值线性关系显著。通过CT值和标准曲线定量,经不同处理的古菌16S rRNA基因丰度如下。CK组:6.61×109±0.38a拷贝数/克(干土);60 mg/kg DMAs组:2.68×109±0.30c拷贝数/克(干土);120 mg/kg DMAs组:4.58×109±0.19b拷贝数/克(干土)。基因丰度范围为2.68×109~6.61×109拷贝数/克(干土)。CK组基因丰度最高,DMAs处理组显著降低,且60 mg/kg组的抑制作用强于120 mg/kg组。结果表明,DMAs胁迫对古菌增殖具有剂量依赖性,但高质量浓度处理组抑制作用减弱,这可能与耐性菌群富集相关。
2.3多样性分析
2.3.1α-多样性分析
与对照组相比,DMAs处理组的古菌Chao1指数显著降低(P<0.01),表明DMAs胁迫显著削弱了古菌群落的丰富度,但60 mg/kg和120 mg/kg DMAs处理组的Chao1指数差异不显著。同时,DMAs处理组的Simpson指数显著降低(P<0.05),说明古菌群落的多样性显著提升,可能促进了优势类群扩张,但60 mg/kg和120 mg/kg DMAs处理组的Simpson指数差异不显著。
2.3.2β-多样性分析
主坐标分析(PCoA)表明,DMAs处理显著改变了古菌群落结构。对照组与60 mg/kg DMAs处理组在PCo1轴上显著分离,解释率为79.3%;对照组与120 mg/kg DMAs处理组在PCo2轴上显著分离,解释率为6.6%。两轴合计解释了85.9%的变异,表明DMAs胁迫对土壤古菌群落结构产生了显著影响。
2.3.3门水平和纲水平上的古菌群落结构分析
在所检测样品中,古菌群落的门水平上共鉴定出7个门类,其中Crenarchaeota(泉古菌门)、Nanoarchaeaeota(纳古菌门)和Thaumarchaeota(奇古菌门)为主要类群。60 mg/kg和120 mg/kg DMAs处理组Nanoarchaeaeota的相对丰度均显著降低,Thaumarchaeota的相对丰度显著提高。在纲水平上,Bathyarchaeia(深古菌)、Woesearchaeia(乌斯古菌)和Nitrososphaeria(亚硝基菌)为主要类群。60 mg/kg和120 mg/kg DMAs处理组Woesearchaeia的相对丰度均显著降低,Nitrososphaeria的相对丰度显著提高。这些结果表明,研究土壤的碳循环过程较为复杂,而DMAs胁迫可能通过改变Woesearchaeia和Nitrososphaeria的相对丰度,影响土壤氮循环等生态功能。
3结语
本研究通过微宇宙土壤培养实验系统揭示了DMAs胁迫与稻田古菌群落的剂量-效应关系,发现高质量浓度DMAs(120 mg/kg)未呈现更强的抑制作用,这可能与其挥发性特征相关;Woesearchaeia纲相对丰度随DMAs质量浓度升高呈梯度下降,表明其可作为潜在的砷污染生物指示物。DOC含量升高与Bathyarchaeia纲富集显著相关(r=0.73,P<0.01),且Nitrososphaeria纲相对丰度显著增加,共同提示DMAs可能通过改变碳氮代谢平衡诱导古菌群落功能重组。此外,pH持续碱性化可能抑制产甲烷古菌活性,为砷甲基化-脱甲基动态平衡研究提供了新视角。未来研究需聚焦古菌介导的甲基砷挥发途径、根际古菌-水稻相互作用对砷吸收的影响机制,以及有机质组分变化与古菌砷代谢功能的耦合关系,同时结合宏基因组学、田间验证和耐砷菌株筛选,推动砷污染修复技术的开发。
参考文献
[1]CHEN C,LI L Y,HUANG K,et al.Sulfate-reducing bacteria and methanogens are involved in arsenic methylation and demethylation in paddy soils[J].The ISME Journal,2019,13(10):2523-2535.
[2]DUAN G L,LIU W J,CHEN X P,et al.Association of arsenic with nutrient elements in rice plants[J].Metallomics,2013,5(7):784-792.
[3]WILLIAMS P N,VILLADA A,DEACON C,et al.Greatly enhanced arsenic shoot assimilation in rice leads to elevated grain levels compared to wheat and barley[J].Environmental Science&Technology,2007,41(19):6854-6859.
[4]LIMMER M A,WISE P,DYKES G E,et al.Silicon decreases dimethylarsinic acid concentration in rice grain and mitigates straighthead disorder[J].Environmental Science&Technology,2018,52(8):4809-4816.
[5]LOMAX C,LIU W J,WU L,et al.Methylated arsenic species in plants originate from soil microorganisms[J].New Phytologist,2012,193(3):665-672.
[6]杨雨萍.土壤-植物系统中砷迁移转化的关键调控因子研究[D].北京:中国科学院大学,2020.
[7]WASILKOWSKI D,MROZIK A,PIOTROWSKA-SEGET Z,et al.Changes in enzyme activities and microbial community structure in heavy metal-contaminated soil under in situ aided phytostabilization[J].CLEAN-Soil,Air,Water,2014,42(11):1618-1625.










