肠道菌群与脊柱侧凸相关性研究进展论文
2026-04-09 11:25:29 来源: 作者:xuling
摘要:脊柱侧凸作为一种常见的脊柱畸形,其发病机制尚未完全明确。研究发现,肠道菌群失调可能在脊柱侧凸发生发展中发挥重要作用。
摘要:脊柱侧凸作为一种常见的脊柱畸形,其发病机制尚未完全明确。研究发现,肠道菌群失调可能在脊柱侧凸发生发展中发挥重要作用。文章综述了脊柱侧凸与肠道菌群失调的关系,探讨了肠道菌群通过短链脂肪酸、免疫调节及血浆蛋白等机制影响脊柱侧凸的可能途径,并介绍了益生菌、益生元及粪便微生物群移植等调节肠道菌群的治疗方法在脊柱侧凸中的潜在应用。
关键词:脊柱侧凸;肠道菌群;益生菌
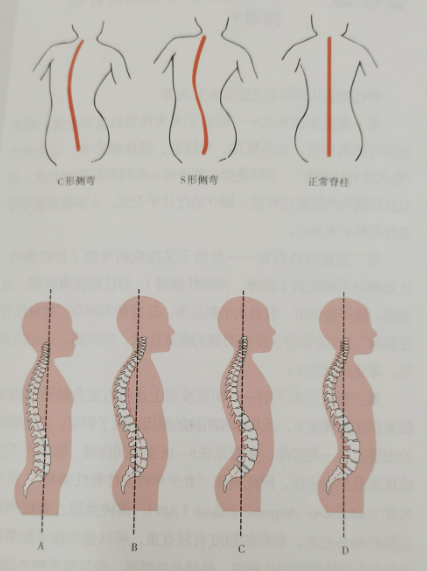
脊柱侧凸是一种复杂的三维脊柱畸形,主要分为先天性、综合征性、神经肌肉性和特发性4种类型[1-2]。青少年特发性脊柱侧凸(AIS)是最常见的脊柱侧凸类型,影响着全球约4%的青少年[3]。脊柱侧凸研究学会(SRS)建议,当Cobb角≥10。并伴有轴向旋转时,应明确诊断为脊柱侧凸[4]。严重的脊柱侧凸可能导致脊柱进一步畸形,需要进行支具治疗甚至手术干预,并且还会面临一系列并发症,如心理障碍、慢性腰痛以及心肺功能受损等[5]。脊柱侧凸的发病机制涉及遗传、代谢、生物力学、神经和环境等多种因素[6],但其确切病因尚未明确。已有研究表明,肠道微生物群和免疫系统在脊柱侧凸的发展中可能发挥重要作用[7]。
肠道菌群由定栖于消化道中的多种原核与真核微生物组成,包括细菌、古细菌及真菌等,与宿主共生,对新陈代谢、炎症和免疫反应等生理功能具有重要影响[8]。肠道菌群参与维持生理平衡和代谢过程,对免疫系统成熟、维生素合成和营养同化等具有重要意义[9]。研究表明,肠道微生物组失调会损害激素稳态并引发代谢紊乱[10-11]。在女性青少年特发性脊柱侧凸患者骨密度较低的个体中,已观察到代谢紊乱和激素水平变化[12]。鉴于微生物群落结构及宿主对微生物群的反应改变与异常骨骼生长和吸收密切相关,研究人员提出“肠-肌肉骨骼轴”和“肠-骨骼轴”的概念[13-14]。肠道微生物群与肌肉骨骼疾病的关联性受到了广泛关注,其在脊柱侧凸中的作用机制值得深入探讨。本文旨在通过回顾已有文献,深入分析肠道菌群与脊柱侧凸的相关性,为脊柱侧凸的预防、诊断和治疗提供新的视角和理论依据。
1肠道微生态失调与脊柱侧凸
1.1不同菌群的丰度在脊柱侧凸中有所不同
脊柱侧凸的病因一直是研究热点。研究证实,遗传因素[15]、雌激素[16]和瘦素[17]均与AIS存在关联。当前研究聚焦肠道微生物与骨骼健康的关联性,如骨质减少和骨形成间的平衡[18-20]。研究发现,AIS患者中低BMI及骨质减少患者肠道菌群的相对丰度显著偏低[21-22]。Fang等[22]研究显示,AIS患者与健康人及先天性脊柱侧凸患者的肠道菌群存在差异——AIS患者粪便中厚壁菌门(Firmicutes)与拟杆菌门(Bacteroidetes)的比值(F/B),以及瘤胃球菌属(Ruminococcus)的相对丰度显著降低,说明肠道菌群可能在AIS的后天发展中发挥一定的作用。Shen等[23]发现,与同龄同性别的健康个体相比,轻中度AIS患者肠道中,普雷沃菌属(Prevotella)的相对丰度增加,且其相对丰度与Cobb角呈正相关。此外,另有研究发现,重度AIS患者肠道中普雷沃菌属的相对丰度与骨质减少呈负相关,表明该菌种可能对AIS具有保护作用[21]。综上,AIS患者肠道菌群变化复杂,从单一研究中识别出的物种不良复制现象可能无法反映与脊柱侧凸真正相关的肠道菌群变化。
1.2肠道菌群与脊柱侧凸的孟德尔随机化分析
孟德尔随机化(MR)研究利用遗传变异而非暴露因素分析肠道菌群与脊柱侧凸的因果联系,避免了潜在混杂因素和反向因果关系的影响[24]。在肠道菌群和脊柱侧凸的孟德尔随机化分析中发现,肠道菌群与脊柱侧凸具有统计相关性[25-27]。嗜胆菌属(Bilophila)、优杆菌属群(Eubacterium eligens group)、普雷沃菌属9(Prevotella 9)与AIS风险降低相关;瘤胃球菌科UCG009(Ruminococcaceae UCG009)、毛螺菌科FCS020群(Lachnospiraceae FCS020 group)、瘤胃梭菌属6(Ruminiclostridium 6)可能会增加脊柱侧凸发生率[25-26]。
2肠道微生态失调影响脊柱侧凸的机制
2.1肠道代谢产物与脊柱侧凸
肠道菌群的稳定生态增强了肠道通透性,减轻了炎症,并积极参与免疫调节。然而,菌群失调会促使某些微生物选择性富集,导致微生物衍生物或代谢物产生,加速了各种全身性疾病的发展[28]。肠道微生物释放的代谢物对宿主的免疫功能和健康起着不可或缺的作用。其主要代谢产物——短链脂肪酸(SCFA)是关键的代谢和免疫介质,用于调节G蛋白偶联受体,影响激素分泌、神经递质释放并调节炎症和情绪。此外,还包括醋酸盐、丙酸盐和丁酸盐,其以特定比例存在,维持肠道菌群平衡[29]。作为研究最深入的细菌代谢物,SCFA被认为在“肠-骨骼轴”中发挥重要作用[14]。相关机制研究表明,SCFA通过Treg细胞介导的WNT10b通路,既能增强骨骼的合成代谢,又能抑制破骨细胞形成[30]。并且,在AIS患者中,高骨转换状态被发现参与脊柱侧凸的起始和进展[31]。梭菌纲的瘤胃球菌属是公认的主要的SCFA产生菌[32]。已有研究发现,血清的1,25(OH)2D水平与产生丁酸的细菌呈正相关,提示肠道菌群可能通过维生素D的代谢影响骨骼健康[33]。关于瘤胃球菌属产生SCFA的相关研究,可能为临床干预脊柱侧凸患者的潜在新治疗靶点提供新思路。此外,还有研究发现,AIS骨量减少的患者淀粉和蔗糖代谢降低,与SCFA密切相关[19]。
2.2血浆蛋白与AIS
研究发现,AIS患者与健康个体的血浆AHNAK、FN1和VDAC1蛋白存在差异,且普雷沃菌属(Prevotella)与血浆AHNAK、FN1和VDAC1蛋白存在相关性[23]。这表明,肠道菌群可能通过调节与骨骼组织发育和功能相关的血浆蛋白参与脊柱侧凸进程。AHNAK在细胞结构与迁移、心脏钙通道调节和肿瘤转移等多种生物过程中发挥作用[34]。多项研究证实,AHNAK与肌肉疾病相关,在骨骼肌再生过程中仍表现显著[35]。由此推断,AHNAK在脊柱侧凸发展过程中参与骨骼肌重塑。FN1基因编码的纤维连接蛋白不仅能促进胶原蛋白、纤维连接蛋白-1等蛋白质的组装,还能通过成骨细胞、软骨细胞和间充质干细胞的分泌在骨骼组织中发挥作用。已有研究证实,FN1基因突变可导致严重的脊柱侧凸[36]。VDAC1是线粒体外膜的主要成分,有助于代谢物和离子在线粒体外膜上交换,并可能调节线粒体功能[37]。VDAC1主要参与线粒体蛋白介导的细胞凋亡途径及细胞凋亡存活调控。通过在肌质网和线粒体间形成连接,VDAC1在骨骼肌功能中发挥重要作用[38]。由于骨骼肌功能障碍参与脊柱侧凸的发展,VDAC1可能通过损害骨骼肌功能参与AIS的发生。血浆蛋白与AIS及肠道菌群的关联性表明,肠道菌群可能基于这些机制对骨骼产生影响。上述结果为理解“肠-肌肉骨骼轴”和“肠-骨骼轴”机制奠定了基础,有助于深入探究肠道微生物群落对脊柱侧凸形成与进展的影响。
3干预肠道菌群或影响疾病进程
目前,脊柱侧凸轻度患者通常采用保守治疗并定期随访观察;重度患者则需进行支具治疗,甚至手术干预。这给患者带来了巨大的经济、心理和生理负担。肠道菌群与脊柱侧凸的相关研究有望开辟新的治疗途径,延缓病情进展。研究发现,肠道菌群通过动态相互作用调节和刺激宿主胰岛素样生长因子I(IGF-I),而IGF-I是骨骼生长的关键因素[39]。
此外,益生菌和益生元的给药、粪便微生物群移植(FMT)和口服SCFA等方法已被证明能稳定并增强肠道菌群组成[40]。益生菌是有益活细菌和酵母的组合,被证实是最具希望的缓解各种神经系统疾病相关症状的辅助疗法。其治疗效果可能归因于抗凋亡机制,包括Bax和caspase-3下调、Bcl-2表达上调,以及其他抗炎途径[41]。双歧杆菌和乳酸菌具有抗炎特性,能增强维生素D的吸收并抑制破骨细胞发育,减轻小鼠卵巢切除术后的骨质流失[42-43]。益生元是促进特定细菌生长的有益纤维。在HLA-B27转基因大鼠中,鼠李糖乳杆菌(Lactobacillus rhamnosus)可有效改善结肠炎[44],益生元也能有效减轻HLA-B27转基因大鼠的结肠炎症状[45]。益生菌和益生元已被证实对逆转体内骨质流失有积极影响,揭示未来或可使用肠道菌群疗法抑制重度脊柱侧凸患者骨质减少。
FMT作为一种新兴技术,在神经损伤恢复中大受欢迎。其优势在于通过增加SCFA的产生和减少有害代谢物,如三甲胺N-氧化物(TMAO)等,改善动物模型的功能,促进其行为恢复[40]。然而,目前关于该主题的人体临床研究还不够充分,在提出临床建议前,需要进一步研究,确定干预措施在患者群体中的安全性和有效性。此外,受AIS影响的青少年处于生长突增期,鉴于肠道菌群组成和功能转变对宿主的全身影响,需要谨慎对待肠道菌群的治疗干预。
4结语
研究表明,肠道微生物失调与脊柱侧凸的发生发展存在密切关联,但其潜在机制尚未完全阐明。已有研究多为小样本、单中心的短期观察,缺乏大样本量、多中心、长期随访的对照试验。不同研究结果差异较大,尚未明确特定有害菌及有益菌的种类。未来研究可尝试在脊柱侧凸模型小鼠体内引入已知可促进或抑制脊柱侧凸进展的菌群,以探究菌群在动物模型中的作用,并揭示其潜在机制。随着多组学研究的深入,这些功能变化将成为脊柱侧凸营养干预的希望目标。
参考文献
[1]FARHAAN A,ALEXANDER G,ZAHER D,et al.Adolescent idiopathic scoliosis[J].BMJ(Clinical Research Edition),2013,346(1):2508.
[2]ALLAM M A,SCHWABE L A.Neuromuscular scoliosis[J].PM&R,2013,5(11):957-963.
[3]CHENG J C,CASTELEIN R M,CHU W C,et al.Adolescent idiopathic scoliosis[J].Nature Reviews Disease Primers,2015,1(1):1-21.
[4]NEGRINI S,DONZELLI S,AULISA A G,et al.2016 SOSORT guidelines:Orthopaedic and rehabilitation treatment of idiopathic scoliosis during growth[J].Scoliosis and Spinal Disorders,2018,13:1-48.
[5]WEINSTEIN S L,DOLAN L A,SPRATT K F,et al.Health and function of patients with untreated idiopathic scoliosis:A 50-year natural history study[J].Jama,2003,289(5):559-567.
[6]PENG Y,WANG S R,QIU G X,et al.Research progress on the etiology and pathogenesis of adolescent idiopathic scoliosis[J].Chinese Medical Journal,2020,133(4):483-493.
[7]SAMAAN M C,MISSIUNA P,PETERSON D,et al.Understanding the role of the immune system in adolescent idiopathic scoliosis:Immunometabolic CONnections to Scoliosis(ICONS)study protocol[J].BMJ Open,2016,6(7):e011812.
[8]KURILSHIKOV A,MEDINA-GOMEZ C,BACIGALUPE R,et al.Large-scale association analyses identify host factors influencing human gut microbiome composition[J].Nature Genetics,2021,53(2):156-165.
[9]O'HARA A M,SHANAHAN F.The gut flora as a forgotten organ[J].EMBO Reports,2006,7(7):688-693.
[10]BRUNKWALL L,ORHO-MELANDER M.The gut microbiome as a target for prevention and treatment of hyperglycaemia in type 2 diabetes:From current human evidence to future possibilities[J].Diabetologia,2017,60(6):943-951.
[11]R魪GNIER M,VAN HUL M,KNAUF C,et al.Gut microbiome,endocrine control of gut barrier function and metabolic diseases[J].Journal of Endocrinology,2021,248(2):R67-R82.
[12]WANG Y J,YU H G,ZHOU Z H,et al.Leptin receptor metabolism disorder in primary chondrocytes from adolescent idiopathic scoliosis girls[J].International Journal of Molecular Sciences,2016,17(7):1160.
[13]RIZZOLI R.Microbiota and bone health:The gut-musculoskeletal axis[Z].Springer,2018:385-386.
[14]ZAISS M M,JONES R M,SCHETT G,et al.The gut-bone axis:How bacterial metabolites bridge the distance[J].The Journal of Clinical Investigation,2019,129(8):3018-3028.
[15]HALLER G,ALVARADO D,MCCALL K,et al.A polygenic burden of rare variants across extracellular matrix genes among individuals with adolescent idiopathic scoliosis[J].Human Molecular Genetics,2016,25(1):202-209.
[16]LEBOEUF D,LETELLIER K,ALOS N,et al.Do estrogens impact adolescent idiopathic scoliosis?[J].Trends in Endocrinology&Metabolism,2009,20(4):147-152.
[17]LIU Z,TAM E M,SUN G Q,et al.Abnormal leptin bioavailability in adolescent idiopathic scoliosis:An important new finding[J].Spine,2012,37(7):599-604.
[18]IBÁÑEZ L,ROULEAU M,WAKKACH A,et al.Gut microbiome and bone[J].Joint Bone Spine,2019,86(1):43-47.
[19]LI J,HO W T P,LIU C,et al.The role of gut microbiota in bone homeostasis:a systematic review of preclinical animal studies[J].Bone&Joint Research,2021,10(1):51-59.
[20]ZHANG J,LU Y,WANG Y,et al.The impact of the intestinal microbiome on bone health[J].Intractable&Rare Diseases Research,2018,7(3):148-155.
[21]LI J,LIU C,XU Y,et al.Gut microbiota alterations in adolescent idiopathic scoliosis are associated with aberrant bone homeostasis[J].Orthop Surg,2024,16(4):965-975.
[22]FANG Y,TIAN Z,LI W,et al.Gut microbiota alterations in adolescent idiopathic scoliosis:a comparison study with healthy control and congenital scoliosis[J].Spine Deform,2025,13(2):497-507.
[23]SHEN N,CHEN N,ZHOU X,et al.Alterations of the gut microbiome and plasma proteome in Chinese patients with adolescent idiopathic scoliosis[J].Bone,2019,120:364-370.
[24]M N D,V M H,George S D.Reading Mendelian randomisation studies:a guide,glossary,and checklist for clinicians[J].BMJ(Clinical Research Edition),2018,362:k601.
[25]LAI B,JIANG H,GAO Y,et al.Causal effects of gut microbiota on scoliosis:A bidirectional two-sample mendelian randomization study[J].Heliyon,2023,9(11):e21654.
[26]LUO K,ZENG W,LI Q,et al.Causal effects of specific gut microbiota on spinal stenosis diseases:a two-sample mendelian randomization study[J].Front Genet,2024,15:1400847.
[27]ZHAO X,LIU J,ZHANG L,et al.Gut microbiota,inflammatory factors,and scoliosis:a Mendelian randomization study[J].Medicine(Baltimore),2024,103(24):e38561.
[28]KHO Z Y,LAL S K.The human gut microbiome a potential controller of wellness and disease[J].Frontiers in Microbiology,2018,9:356589.
[29]MUSSO G,GAMBINO R,CASSADER M.Obesity,diabetes,and gut microbiota:the hygiene hypothesis expanded?[J].Diabetes Care,2010,33(10):2277-2284.
[30]TYAGI A M,YU M,DARBY T M,et al.The microbial metabolite butyrate stimulates bone formation via T regulatory cell-mediated regulation of WNT10B expression[J].Immunity,2018,49(6):1116-1131.e7.
[31]ZHANG J,WANG Y,CHENG K-L,et al.Association of higher bone turnover with risk of curve progression in adolescent idiopathic scoliosis[J].Bone,2021,143:115655.
[32]MACFARLANE S,MACFARLANE G T.Regulation of short-chain fatty acid production[J].Proceedings of the Nutrition Society,2003,62(1):67-72.
[33]THOMAS R L,JIANG L,ADAMS J S,et al.Vitamin D metabolites and the gut microbiome in older men[J].Nature Communications,2020,11(1):5997.
[34]DAVIS T,LOOS B,ENGELBRECHT A-M.AHNAK:The giant jack of all trades[J].Cellular Signalling,2014,26(12):2683-2693.
[35]HUANG Y,LAVAL S H,VAN REMOORTERE A,et al.AHNAK a novel component of the dysferlin protein complex,redistributes to the cytoplasm with dysferlin during skeletal muscle regeneration[J].The FASEB Journal,2007,21(3):732-742.
[36]LEE C S,FU H,BARATANG N,et al.Mutations in fibronectin cause a subtype of spondylometaphyseal dysplasia with“corner fractures”[J].The American Journal of Human Genetics,2017,101(5):815-823.
[37]LI H,ZHENG L,MO Y,et al.Voltage-dependent anion channel 1(VDAC1)participates the apoptosis of the mitochondrial dysfunction in desminopathy[J].PLOS One,2016,11(12):e0167908.
[38]LIU Z,DU X,DENG J,et al.The interactions between mitochondria and sarcoplasmic reticulum and the proteome characterization of mitochondrion associated membrane from rabbit skeletal muscle[J].Proteomics,2015,15(15):2701-2704.
[39]YAN J,CHARLES J F.Gut microbiota and IGF-1[J].Calcified Tissue International,2018,102:406-414.
[40]PANTHER E J,DODD W,CLARK A,et al.Gastrointestinal microbiome and neurologic injury[J].Biomedicines,2022,10(2):500.
[41]LI H,SUN J,DU J,et al.Clostridium butyricum exerts a neuroprotective effect in a mouse model of traumatic brain injury via the gut brain axis[J].Neurogastroenterology&Motility,2018,30(5):e13260.
[42]BRITTON R A,IRWIN R,QUACH D,et al.Probiotic L.reuteri treatment prevents bone loss in a menopausal ovariectomized mouse model[J].Journal of Cellular Physiology,2014,229(11):1822-1830.
[43]REIGSTAD C S,SALMONSON C E,RAINEY III J F,et al.Gut microbes promote colonic serotonin production through an effect of short-chain fatty acids on enterochromaffin cells[J].The FASEB Journal,2014,29(4):1395.
[44]DIELEMAN L A,GOERRES M S,ARENDS A,et al.Lactobacillus GG prevents recurrence of colitis in HLA-B27 transgenic rats after antibiotic treatment[J].Gut,2003,52(3):370-6.
[45]HOENTJEN F,WELLING G W,HARMSEN H J,et al.Reduction of colitis by prebiotics in HLA-B27 transgenic rats is associated with microflora changes and immunomodulation[J].Inflammatory Bowel Diseases,2005,11(11):977-985.










