产 NMN 转移酶工程菌高密度发酵研究论文
2026-04-09 11:19:45 来源: 作者:xuling
摘要:文章将含有烟酰胺单核苷酸腺苷酰转移酶(Nmnat)基因的重组大肠杆菌在5 L生物反应器中分批培养,以评估细胞生长情况和酶产量,系统考察包括生物量积累(OD600)和Nmnat活性在内的发酵参数,重点优化发酵策略和诱导时间。
摘要:文章将含有烟酰胺单核苷酸腺苷酰转移酶(Nmnat)基因的重组大肠杆菌在5 L生物反应器中分批培养,以评估细胞生长情况和酶产量,系统考察包括生物量积累(OD600)和Nmnat活性在内的发酵参数,重点优化发酵策略和诱导时间。实验菌株在5 L生物反应器中分批发酵培养12 h,OD600达到最大值10.05,Nmnat活性峰值为16.77 U/mg,较摇瓶培养(9.36 U/mg)提高79.17%。补料策略的比较分析表明,恒速流加补料在细胞生长和Nmnat产量方面均优于DO-Stat补料方式。当诱导时间为10 h时,发酵达到最佳状态,获得最大OD600值(46.69)、最高Nmnat活性(21.95 U/mg)和总酶活(190.5 kU)。研究确定的5 L规模发酵参数,为潜在的工业化放大应用提供了重要参考。
关键词:重组大肠杆菌;NMN转移酶;分批发酵;恒速流加补料
NMN转移酶(Nmnat)是生物体内唯一可催化合成烟酰胺腺嘌呤二核苷酸(NAD)的生物酶,对于维持生物体NAD稳定至关重要[1]。研究发现,NAD可参与生物体的多种氧化反应,如细胞物质代谢、能量合成、细胞DNA修复等,在细胞生命活动中发挥着重要作用[2]。在生物代谢途径中,以烟酰胺单核苷酸(NMN)和ATP为前体,在NMN转移酶催化作用下,可生成NAD和焦磷酸盐[3]。
研究表明,NMN转移酶在衰老、神经退行性疾病(如阿尔茨海默病)和代谢紊乱(如糖尿病)中发挥关键作用,其活性下降会导致NAD水平降低,影响细胞能量代谢和修复能力[4]。在合成生物学方面,微生物过表达Nmnat可显著提高NAD+产量,为工业发酵提供新思路[5]。研究表明,通过基因工程改造大肠杆菌、酵母等微生物,提高Nmnat表达水平,能有效提升NAD+的合成效率,同时优化辅因子供应,促进目标产物高密度发酵[6]。此外,结合动态调控策略(如诱导型启动子或代谢传感器),可进一步提高NAD+积累,减少中间代谢物的毒性抑制,提升工业发酵的经济性和可持续性[7]。
基因工程菌的目标产物产量主要受发酵液菌体密度和外源基因表达效率调控[8]。在表达水平相对稳定的条件下,提高产物产量的核心策略在于实现高密度发酵(high cell density fermentation,HCDF)。HCDF通过优化培养条件延长对数生长期并缩短衰亡期,使菌体密度显著高于传统发酵水平。根据行业标准,HCDF通常指菌体干重(Dry Cell Weight,DCW)超过50 g/L的培养体系[9]。该技术可显著提升体积生产率,具有缩小培养体积、缩短生产周期和降低综合成本等优势[10]。理论研究表明,大肠杆菌的最大理论发酵密度可达160~200 g/L(DCW)。实际生产报道显示,产聚-3-羟丁酸的重组大肠杆菌的峰值密度能达到175.4 g/L(DCW)[11]。
相较于传统摇瓶培养,HCDF需要更精确的环境控制体系。摇瓶培养存在明显的局限性,包括无法实时监测微生物生长动力学参数、缺乏对关键培养参数(如溶解氧、pH、营养物质量浓度)的动态调控能力,以及培养环境非均一性导致的代谢条件波动[12]。这些限制,使得摇瓶实验结果不能直接外推至规模化HCDF体系。
HCDF效率的影响因素构成复杂的调控网络。其中,营养调控尤为关键。培养基组分需满足碳氮平衡、微量元素供给和渗透压调节[13],而补料策略需平衡营养供给与代谢副产物积累之间的矛盾。当抑制性代谢物(如乙酸、乳酸)超过阈值时,菌种会通过反馈抑制影响细胞生长和蛋白表达[14]。环境参数方面,温度调控存在生长-表达权衡效应:较高温度可促进生物量积累;较低温度则有利于蛋白质正确折叠和保持稳定[15]。溶解氧(DO)需维持>30%的空气饱和度以满足氧化代谢需求;DO不足会导致代谢流重组[16]。此外,pH稳态通过缓冲系统或在线调节维持最适范围;pH波动会影响膜电位和酶活性。
在过程控制策略上,补料分批发酵已成为HCDF的标准模式。其优势包括避免底物抑制、采用动态补料策略,以及基于过程参数的反馈控制[17]。现代生物反应器已实现多参数在线监测(如生物量、代谢通量等),但细胞代谢网络的实时解析仍需结合组学技术(如代谢通量分析)展开[18]。
本研究在摇瓶发酵基础上对前期实验室构建的重组大肠杆菌pET30α(+)-Nmnat进行5 L发酵罐高密度发酵,并对微生物生长和产物NMN转移酶活性实施监控,为后期大规模发酵产NMN转移酶提供参考。
1材料与方法
1.1材料
1.1.1质粒与菌株
重组大肠杆菌E.coli BL21(DE3)pET30α(+)-Nmnat由本实验室提供。
1.1.2培养基和培养方法
一级种子:挑取重组表达质粒pET30α(+)-Nmnat的E.coli BL21(DE3)单菌落接种于10 mL LB液体培养基(含30μg/mL KA),37℃、200 r/min培养过夜。二级种子:将一级种子液按1%接种量接种于100 mL TB培养基(含30μg/mL KA),37℃、200 r/min培养12 h。将二级种子液按体积1.5%接种于含3 L发酵培养基(含30μg/mL KA)的发酵罐中,37℃培养。
1.1.3主要试剂和仪器
异丙基硫代-β-D-半乳糖苷(IPTG),购自上海生工生物工程公司;其他实验用试剂均为国产分析纯。5 L发酵罐和空压机,购自上海百伦生物科技有限公司。
1.2方法
1.2.1酶活测定方法
参照文献[19]酶活测定方法。
1.2.2发酵罐中甘油含量测定
采用比色法测定甘油含量。其原理是甘油属于糖类化合物,酸性高碘酸盐可与糖醇类化合物发生氧化作用生成甲醛。加入Nash试剂生成的物质呈黄色,且在波长412 nm处有最大吸收峰。因此,可测定OD412处的吸光度,计算反应液的甘油质量浓度。
1.2.3分批发酵
按说明书校正发酵罐pH电极和溶氧电极。将3 L发酵液121℃灭菌处理25 min,冷却至室温,加入终浓度为30μg/L的KA。将二级种子液按体积1.5%接种量接种于5 L发酵罐中,37℃培养。通过回流水控制温度在37℃,同时控制转速和空气流量,使发酵罐氧气含量保持在20%~30%。加2.0 mol/L的HCl和NH3·H2O,将培养基pH调至7.0左右。培养一段时间后,加入终浓度为0.4 mmol/L的诱导剂IPTG,实时监测种子生长量OD600、甘油质量浓度、Nmnat活力。
1.2.4分批补料(FBC)发酵
恒速流加补料模式:将发酵罐培养基温度和溶氧量控制在37℃和20%~30%;在菌体生长量达到对数期时,按一定速率补加25%甘油,直至发酵结束。
DO-stat流加模式:将发酵罐培养基温度控制在37℃左右;当溶氧升高超过30%时,流加浓度为25%的甘油,直至溶氧维持在20%~30%,停止补料。反复操作至发酵结束。
1.3结果与分析
1.3.1发酵方式对重组菌的生长及NMN转移酶的影响
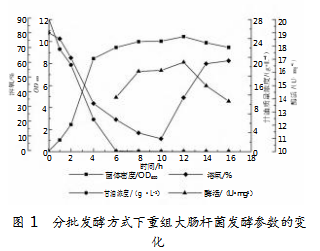
研究采用5 L发酵罐进行大肠杆菌发酵,按照1.5%的接种量接种于3 L发酵培养基中,采用分批发酵方式(关联搅拌转速和空气流量,维持灌氧浓度20%~30%)实时监测大肠杆菌生长量OD600、甘油残余量、pH、溶氧量,结果如图1所示。
0~2 h期间,大肠杆菌处于适应调整期,罐内维持较高的甘油和溶氧水平;2~8 h期间,重组大肠杆菌呈对数生长,由于对数期菌体需要大量消耗碳源和氧气,监控到甘油质量浓度和氧气含量随菌体生长急剧下降;8~12 h为大肠杆菌生长稳定期,此时菌体量OD600处于较高水平;10 h时,溶氧水平最低;12 h后,大肠杆菌进入衰亡期,菌体生长量降低。
在5 L发酵罐进行大肠杆菌分批发酵,菌体密度OD600在12 h达到最大值10.05,较摇瓶优化后发酵提高76.04%;发酵12 h Nmnat酶活力达到最大值16.77 U/mg,较摇瓶发酵(9.36 U/mg)提高79.17%。由此可见,分批发酵方式有利于重组大肠杆菌产Nmnat;通过分批发酵,各参数变化可为下一步补料发酵方式提供数据参考。
1.3.2 DO-Stat模式对重组大肠杆菌的生长及NMN转移酶的影响
DO-Stat模式指当发酵体系的溶氧含量发生反弹时,根据溶氧变化情况调节流加碳源何时开始和结束。
根据前期分批发酵方式的数据分析,5 L发酵罐中的甘油含量在一段时间后消耗为零。因此,有必要通过适时增加碳源含量提高重组菌的生长量OD600和Nmnat酶活力,并采用DO-Stat反馈补料方式考察重组菌的生长和产Nmnat活力。
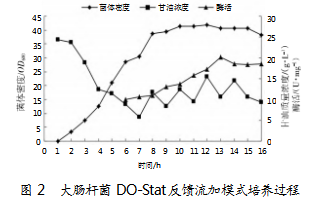
重组大肠杆菌在DO-Stat方式下的培养过程如图2所示。发酵3 h后,大肠杆菌进入对数生长期;发酵4 h后,在发酵罐中溶氧含量高于30%时以一定速率流加25%甘油,直至溶氧降至20%~30%。反复步骤操作直至发酵结束。
发酵4 h时,重组菌处于对数生长期,甘油质量浓度逐渐降低;7 h时,甘油质量浓度降至30.48 g/L,已无法维持菌体快速增长的需求,此时溶氧水平逐渐升高到30%以上,需以一定速率流加碳源甘油,使菌体迅速增长;8 h后,菌体进入稳定期;16 h发酵结束,菌体密度最大值达38.38,较分批发酵(10.54)提高2.64倍,Nmnat的酶活达20.12 U/mg,发酵罐中总酶活为128.8 kU,较分批发酵方式提高173.1%。
1.3.3恒速流加模式对重组大肠杆菌的生长及NMN转移酶的影响
分批补料方式分为2种:恒速流加补料模式和DO-Stat反馈补料方式。其中,恒速流加模式指当微生物处于对数前期时,以一定速率向发酵罐中流加碳源,考察菌体生长和酶活力情况。实验采用恒速流加补料模式考察重组菌的生长和产Nmnat活力。
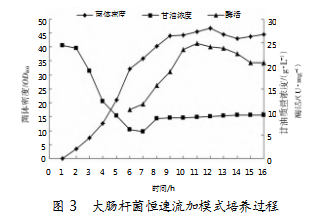
重组大肠杆菌在恒速流加模式下的发酵培养过程如图3所示。在大肠杆菌处于对数前期(3 h)时,以一定速率流加碳源(25%甘油)直至发酵结束。恒速流加甘油过程中,重组菌的对数生长期由8 h延长至10 h;发酵结束(16 h)后种子生长量为46.69,较分批发酵(10.54)和DO-Stat反馈流加模式(38.38)分别提高3.2倍和21.7%,Nmnat酶活最大达21.95 U/mg,总酶活为190.5 kU,较DO-Stat反馈流加模式提高47.9%,较分批发酵模式提高303.9%。
由以上2种补料发酵方式可知,恒速流加模式显著提高了重组大肠杆菌的生长量,且Nmnat的酶活提高较DO-Stat模式更为明显。综合比较,选择恒速流加模式进行后续研究。
1.3.4诱导时间对重组大肠杆菌的生长和NMN转移酶活力的影响
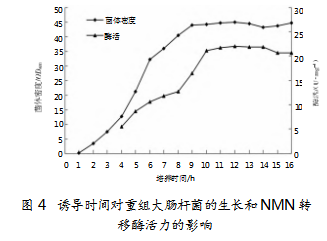
诱导时间的选择对Nmnat积累和菌体生长量OD600具有重要影响。摇瓶试验结果证明,大肠杆菌生长量OD600和菌体产Nmnat的趋势不一定完全一致。因此,选择合适的诱导时间对于改善大肠杆菌生长和产Nmnat能力至关重要。本研究采用恒速流加模式对OD600和产Nmnat能力展开研究。数据显示,5 L发酵罐中的发酵培养曲线与摇瓶发酵培养趋势类似,呈现部分偶联现象(见图4)。发酵12 h时,菌体生长量OD600达到最大值,而Nmnat酶活的最大值则出现在14 h,揭示2个因变量最大值的出现时间不同。通过满意度函数分析可得,发酵12 h(诱导10 h)时,重组菌生长量和Nmnat酶活总体达到最大值,此时菌体量OD600为44.56、Nmnat活力为22.35 U/mg,总酶活达198.57 kU。因此,选择10 h为最佳诱导时间,既可获得高密度菌体生长量又能得到较高的Nmnat活力,有利于后续发酵研究。
2结论
本研究从小型摇瓶发酵实验出发,采用5 L发酵罐,对重组菌产Nmnat的高密度发酵体系展开分析。维持发酵罐体系pH 7.5、20%~30%的溶氧条件,考察分批发酵对重组大肠杆菌生长量、碳源质量浓度和Nmnat活性等参数的影响,最终确定恒速流加补料方式为最佳补料方法,可使细胞密度提高到46.69,酶活提高到21.95 U/mg,总酶活达190.5 kU。大肠杆菌高密度发酵成功的关键在于补料策略,即根据菌体生长特点和目标蛋白表达方式合理流加营养物质。后续可基于本实验研究结果,将经验放大法、数学模型法等运用于工厂生产规模的放大试验中。
参考文献
[1]ZHAO Y.NMNAT-mediated NAD synthesis is essential for cellular homeostasis[J].Nature Metabolism,2023,5(3):256-270.
[2]FANG F E,LAUTRUP S,HOU Y,et al.NAD+in aging:Molecular mechanisms and translational implications[J].Trends in Molecular Medicine,2017,23(10):899-916.
[3]LAUTRUP S.NMNAT enzymes in NAD biosynthesis:Structural insights and therapeutic potential[J].Trends in Biochemical Sciences,2023,48(4):321-335.
[4]COVARRUBIAS A J.NAD+metabolism and its roles in cellular processes during aging[J].Nature Reviews Molecular Cell Biology,2023,24(2):119-138.
[5]LI Y.Metabolic engineering of Escherichia coli for enhanced NAD+production via Nmnat overexpression[J].Metabolic Engineering,2023,75:102-115.
[6]ZHANG H.Synthetic biology approaches to boost NAD+biosynthesis in Saccharomyces cerevisiae[J].Nature Communications,2024,15(1):1234.
[7]WANG X.Dynamic control of NAD+metabolism in industrial fermentation using optogenetic regulation[J].ACS Synthetic Biology,2023,12(5):1567-1582.
[8]Y S L,H S H,H S L,et al.Fermentative production of chemicals that can be used for polymer synthesis[J].Macromolecular Bioscience,2004,4(3):157-164.
[9]SHILOACH J,FASS R.GROWING E.coli to high cell density—A historical perspective on method development[J].Biotechnology Advances,2005,23(5):345-357
[10]CHOI H J,KEUM C K,LEE Y S.Production of recombinant proteins by high cell density culture of Escherichia coli[J].Chemical Engineering Science,2005,61(3):876-885.
[11]WANG F,ZHANG H,ZHANG L,et al.Metabolic engineering of Escherichia coli for poly(3-hydroxybutyrate)production via the citrate synthase pathway[J].Metabolic Engineering,2018,47:201-208.
[12]BÄCKLUND E,MARKLAND K,LARSSON G.Cell engineering and fermentation of recombinant Escherichia coli for protein production[J].Current Opinion in Biotechnology,2008,19(5):446-453.
[13]HO S Y,MEE-JUNG H,YUP S L,et al.Combined transcriptome and proteome analysis of Escherichia coli during high cell density culture[J].Biotechnology and Bioengineering,2003,81(7):753-767.
[14]KASPAR V,KAAREL A,RANNO N,et al.Systems biology approach reveals that overflow metabolism of acetate in Escherichia coli is triggered by carbon catabolite repression of acetyl-CoA synthetase[J].BMC Systems Biology,2010,4(1):166.
[15]FRANK H,URSULA R.Stress induced by recombinant protein production in Escherichia coli[J].Advances in Biochemical Engineering/Biotechnology,2004,89:73-92.
[16]R A L,ENRIQUE G,T O R,et al.Living with heterogeneities in bioreactors:Understanding the effects of environmental gradients on cells[J].Molecular Biotechnology,2006,34(3):355-381.
[17]MARTfNEZ K,DE ANDA R,HERN iNDEZ G,et al.Recombinant protein production by high cell density cultures of Escherichia coli[J].Biotechnology Letters,2008.
[18]O'FLAHERTY R,BERGIN A,FLAMPOURI E,et al.Mammalian cell culture for production of recombinant proteins:Past,present,and future[J].Biotechnology Letters,2020,42(5):657-670.
[19]段琳琳,李红梅.来源于大肠杆菌的NMN转移酶的克隆表达与酶学性质研究[J].工业微生物,2016,46(2):30-35.










