载有他克莫司的透明质酸凝胶在去细胞异体神经移植中抑制瘢痕的实验研究论文
2026-04-02 16:55:52 来源: 作者:xuling
摘要:文章研究周围神经损伤经同种异体神经移植后,添加载有他克莫司(FK506)的透明质酸(HA)对抑制神经吻合口周围瘢痕的影响。健康雄性体重200~250 g SD大鼠60只,20只作为神经供体,40只随机分4组:联合组、FK506组、HA组和对照组。
摘要:文章研究周围神经损伤经同种异体神经移植后,添加载有他克莫司(FK506)的透明质酸(HA)对抑制神经吻合口周围瘢痕的影响。健康雄性体重200~250 g SD大鼠60只,20只作为神经供体,40只随机分4组:联合组、FK506组、HA组和对照组。取材:切取双侧坐骨神经15 mm,并用Sondell脱细胞方法处理。移植神经:切取左侧坐骨神经造成10 mm缺损并移植神经,在每组SD大鼠神经吻合口分别注射药物。检测:Petersen评分、Masson染色、胶原及有髓神经纤维计数分析。利用统计学软件SPSS 25.0对数据进行处理分析。结果显示,联合组、FK506组和HA组中,神经吻合口与周围组织的黏连较轻,均优于对照组;联合组瘢痕最少,且有髓神经纤维数量多于其他3组。载有FK506的HA凝胶对瘢痕的抑制作用优于FK506和HA凝胶单独使用,可促进神经再生。
关键词:神经移植;他克莫司;透明质酸
自体神经移植被认为是周围神经损伤修复的金标准[1]。神经移植主要解决2个难点:一是如何去除异体神经的组织相容性复合物;二是如何减少神经周围瘢痕的形成。自体神经移植物因含有施万细胞、固有细胞外基质和多种神经营养因子,在周围神经损伤治疗中得到了广泛应用,并取得了良好效果[2],但实践中仍存在一定局限性[3]。同种异体神经移植能弥补自体神经移植的缺陷,是自体神经移植的替代材料[4-8]。神经瘢痕作为抑制神经再生的重要因素,新生的神经轴突一旦遇到瘢痕组织会造成神经修复失败[9]。免疫抑制剂他克莫司和透明质酸在组织器官移植中效果良好[10]。本研究将他克莫司和透明质酸作为研究因素,探讨其对神经吻合口周围瘢痕生长的抑制作用。
1材料和方法
1.1材料
实验于2021年11月—2022年4月在牡丹江医科大学医药研究中心完成。
实验动物:健康成年雄性SD大鼠,体重200~250 g,由牡丹江医科大学实验室提供。实验对动物的处置符合动物伦理学要求。
试剂与设备:他克莫司(25 mg),购自上海碧云天生物技术有限公司;透明质酸(1 g),购自上海麦克林生化科技有限公司;Masson三色染色试剂盒,购自福州迈新生物技术开发有限公司;图像分析系统(CIAS-1000型),购自北京大恒图像视觉有限公司。
1.2方法
分组:总计SD大鼠60只,20只作为神经供体,40只被随机分为4组:对照组、HA组、FK506组和联合组,每组10只,供体神经取材及制备。
SD大鼠3%戊巴比妥钠腹腔注射麻醉,下肢背侧入路,梨状肌下缘向远侧切取约15 mm坐骨神经,并采用Sondell脱细胞方法[11]处理。
神经移植:麻醉及手术入路与取材相同,在梨状肌下缘锐性切除坐骨神经,造成10 mm缺损。取10mm神经供体完成神经移植,9-0线神经吻合口4等分吻合。吻合口采用微量注射法:HA组注射HA凝胶(注射量约15μL);FK506组注射FK506溶液[12](注射量约15μL);联合组吻合口注射载有FK506的HA凝胶,且HA和FK506均为15μL;对照组移植后不做处理。术后,单笼饲养,不限制活动。
动物模型造模成功标准:神经吻合可靠,吻合后神经无张力,术后无深部感染或脓肿形成。
1.3主要观察指标(术后12周取材)
大体观察:按照PETERSEN等[13]的分级标准进行评估。
瘢痕检测:采用Masson三色染色法,使细胞核呈黑蓝色,胶原纤维呈蓝色,神经胶质纤维、肌纤维、红细胞呈红色。
Ⅲ型胶原相对含量分析:Ⅲ型胶原100倍光镜下采图,进行图像分析;640倍光镜下测定灰度,胶原含量与灰度值成反比。
有髓神经纤维计数分析:甲苯胺蓝染色,观察各组有髓神经纤维生长情况。
统计学分析:采用SPSS 25.0统计分析软件和Graph pad Prism 8.0对数据进行统计学分析,并制作图表。
2结果
2.1实验动物数量分析
实验40只SD大鼠全部进入结果分析,无脱失。
2.2大体观察
各组SD大鼠的皮肤及肌肉、筋膜无裂开及感染,均存在不同程度的神经黏连。评分统计结果显示,对照组与其余3组均存在显著差异(P<0.05)。
2.3 Masson染色
在400倍光镜下观察到吻合口胶原沉积(见图1)。其中,联合组胶原含量最少,纤维排列紧密(见图1A);FK506组胶原纤维量较少(见图1B);HA组胶原纤维量稍多(见图1C);对照组胶原纤维含量最多,走行杂乱无序(见图1D)。

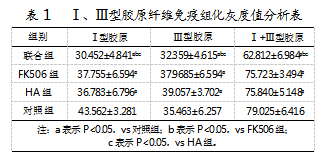
2.4Ⅰ、Ⅲ型胶原相对含量灰度值分析
总胶原、Ⅰ型、Ⅲ型灰度值:联合组与其余3组均存在显著差异(P<0.05),具体如表1所示。
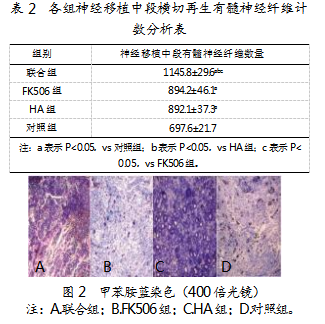
2.5神经移植中段有髓神经纤维计数结果分析
联合组有髓神经纤维数量(1 145.8±29.6个/单位视野)优于其余3组,具体如表2、图2所示。
3讨论
实验观察到以下4个特点:1.联合组神经吻合口与周围组织黏连最轻,对照组神经吻合口与周围组织黏连最重;2.总胶原纤维测定中,联合组胶原纤维总量最少,对照组胶原纤维总量最多;3.Ⅰ、Ⅲ型胶原免疫组化分析结果:联合组总胶原纤维灰度值含量最少,对照组总胶原纤维灰度值含量最多;Ⅰ型胶原灰度值:联合组灰度值含量最少,对照组灰度值含量最多;Ⅲ型胶原灰度值:联合组灰度值含量最少,HA组灰度值含量最多;4.联合组移植神经中段的有髓神经纤维数目最多,对照组的数目最少。在已有研究中,去细胞同种异体神经移植吻合口局部应用HA减少,通过抑制神经吻合口周围炎症反应减少瘢痕生成[9]。本实验得到了同样的研究结果。出现上述结果的原因可能是神经缺损经去细胞异体神经移植物后,在移植段吻合口周围添加载有FK506的HA凝胶、FK506或HA,可调节Ⅰ、Ⅲ型胶原纤维比例或降低总胶原纤维含量,最终抑制神经吻合口周围瘢痕形成。FK506可能通过与胞浆中的FKBP12受体结合形成功能复合体,阻碍T细胞去磷酸化过程,抑制后续相关炎症因子(IL2、IL3、rINF)的表达,进而使成纤维细胞聚集进程受阻,减少成纤维细胞向瘢痕组织的转化[14]。FK506和HA联合应用时,出现叠加效应或协同效应。究其原因,可能是去细胞异体神经移植物后,载有FK506的HA凝胶可抑制神经吻合口周围瘢痕生长,促进神经再生。但其抑制瘢痕生长和促进神经再生的机制较为复杂,尚不明确是叠加效应还是协同促进,需进一步探讨具体作用机制。
4结论
载有FK506的HA凝胶在去细胞同种异体神经移植中的效果优于单独应用FK506和HA凝胶。载有FK506的HA凝胶有促进神经再生的作用,可通过调节Ⅰ、Ⅲ型胶原分布,降低总胶原含量,减少神经周围瘢痕形成,促进神经再生。
参考文献
[1]C A P,S J K,B R B,et al.Mass spectrometry comparison of nerve allograft decellularization processes[J].Journal of Materials Science.Materials in Medicine,2017,28(1):20.
[2]GLAUS W S,JOHNSON J P,MACKINNON E S.Clinical strategies to enhance nerve regeneration in composite tissue allotransplantation[J].Hand Clinics,2011,27(4):495-509.
[3]FEENEY D M,BOYESON M G,LINN R T,et al.Responses to cortical injury:Methodology and local effects of contusions inthe rat[J].Brain Research,1981,211:67-77.
[4]黄永旺,范学政.几丁糖与聚乳酸合成生物材料修复周围神经缺损[J].中国组织工程研究,2015,19(25):4059-4063.
[5]刘奔.聚己内酯/壳聚糖神经导管复合骨髓间充质干细胞促进大鼠坐骨神经损伤修复的研究[D].锦州:辽宁医学院,2014.
[6]张孙富,王斌.合成可生物降解神经导管修复损伤周围神经:生物相容性良好[J].中国组织工程研究,2015,19(25):4054-4058.
[7]王华松,吴刚,黄继锋,等.新型仿生人工神经导管修复周围神经缺损的初步临床观察[J].中国临床解剖学杂志,2014,32(6):735-738.
[8]李玢,郝立君.不同神经导管材料的研究进展[J].中国美容整形外科杂志,2014,25(1):62-64.
[9]刘英伟,张万里,池成涛,等.透明质酸在去细胞异体神经移植中对瘢痕的影响[J].中国组织工程研究,2016,20(42):6317-6323.
[10]蒋延超,蒋世云,傅凤鸣,等.透明质酸生物合成途径及基因工程研究进展[J].中国生物工程杂志,2015,35(1):104-110.
[11]SONDELL M,LUNDBORG G,KANJE M.Regeneration of the rat sciatic nerve into allografts made acellular through chemical extraction[J].Brain Research,1998,795(1-2):44-54.
[12]Y A M,A A M,SUZANA M,et al.Electrophysiological and functional evaluation of peroneal nerve regeneration in rabbit following topical hyaluronic acid or tacrolimus application after nerve repair[J].The Nigerian Postgraduate Medical Journal,2015,22(3):179-184.
[13]PETERSEN J,RUSSELL L,ANDRUS K,et al.Reduction of extraneural scarring by ADCON-T/N after surgical intervention[J].Neurosurgery,1996,38:976-983.
[14]何新泽,田冲,李芹,等.大鼠颅脑损伤联合FK506诱导促进坐骨神经再生的研究[J].吉林医学,2020,41(1):5-8.










