口腔微生物群与龋齿发生的关联性研究论文
2026-04-02 15:18:19 来源: 作者:xuling
摘要:口腔微生物群在龋齿发生与进展中的角色已逐渐从“伴生者”转向“主导者”。文章借助纵向观察,细致分析从初始定殖到修复后再定殖的4个生态阶段,揭示菌群结构、代谢特性与宿主环境间的动态耦合。
摘要:口腔微生物群在龋齿发生与进展中的角色已逐渐从“伴生者”转向“主导者”。文章借助纵向观察,细致分析从初始定殖到修复后再定殖的4个生态阶段,揭示菌群结构、代谢特性与宿主环境间的动态耦合。分析显示,高载量变形链球菌可显著提升婴幼儿早期脱矿风险;正畸托槽周缘的厚层生物膜是釉质白斑扩大的催化区;酸耐受菌在低pH微环境中加速矿质流失并推动深龋形成;修复体边缘粗糙与微漏为复发龋提供二次生态位。研究表明,菌群生态稳态的破坏与龋损演变呈线性递进关系,需随阶段动态调整干预窗口。
关键词:口腔微生物群;龋齿;菌斑生态
龋齿以高发、难自愈与累积性破坏著称。WTO将其列为全球最常见的慢性疾病之一。第4次全国口腔流调数据显示,我国12岁儿童恒牙患龋率34.5%,较10年前上升了7.8%,15岁儿童恒牙患龋率44.4%,成人35~44岁恒牙患龋率89.0%。儿童时期未能养成良好口腔卫生习惯,导致龋病高发[1]。本文基于4阶段框架,系统阐释口腔微生物群如何驱动龋齿从微观斑点演变至深部病灶,再到修复体周缘复发,以期为精准预防与个体化干预提供依据。
1口腔微生物群与龋齿发生机制
1.1口腔微生物群
口腔微生物群泛指定殖于牙面、龈缘、舌背、颊黏膜、唾液等部位的微生物共同体,涵盖细菌、真菌、古菌、病毒及噬菌体。其并非松散拼凑,而是形成相互依赖的“网络群落”—核心菌种维系基本代谢途径;旁系成员通过代谢互补、信号分泌或基质共建维持生态弹性。菌群在时间与空间上呈高度异质:同一人日间饮食波动即可触发群落相对丰度与功能谱的细微震荡;牙面与舌背的氧张力差异则塑造了需氧与兼性厌氧菌截然不同的分布格局[2]。
从功能视角看,菌群承担多重角色:一方面,代谢氨基酸、硝酸盐与多糖为宿主提供维生素、调节唾液pH、抑制外来病原;另一方面,若生态平衡被高糖摄入、口腔干燥或宿主免疫力下降打破,菌群结构会出现“功能漂移”,增强酸产能、减弱缓冲能力,进入龋病易感状态[3]。
1.2龋齿发生机制
龋病,又称“虫牙”“蛀牙”,是一种以细菌为主要病原体,多因素作用下发生在牙齿硬组织上的慢性、进行性破坏性疾病。目前公认的龋病发生原因为“四联因素理论”,即细菌、食物、宿主和时间。已有研究证明,牙菌斑中的致龋细菌是龋的主要病原体。致龋细菌通过在牙菌斑中代谢从食物中获得的糖或碳水化合物,生成以乳酸为主的有机酸,导致牙齿中的磷灰石结构脱矿溶解。在蛋白酶的作用下,结构中的有机物支架遭到破坏,临床上表现为牙齿上发生不能为自体修复的龋洞。若龋洞得不到及时治疗,病变会向深层发展,可能感染牙齿内部的牙髓组织,甚至进入根尖周组织引起更严重的机体炎症性病变[4]。
2口腔微生物群与龋齿发生的关系
2.1研究设计与方法概述
本文采用单中心、多亚组并行的观察性研究设计,覆盖婴幼儿、青少年与成年人群的龋病风险链条与微生态特征。方案经伦理审查批准,所有受试者及监护人签署书面知情同意书,能确保数据采集的合规性与可重复性。通过建立横跨发育阶段的纵向观察路径,力图揭示微生物群与龋病发生、进展、复发间的因果关联。
研究对象与样本配置:设置3个核心研究队列:婴幼儿队列(n=180)聚焦定殖建立与早期龋;正畸青少年队列(n=134,含对照组n=120)用于分析菌斑成熟与脱矿风险;成人龋损及修复子队列(n=162,修复随访子样n=120)用于探讨深龋扩展与治疗后生态重建。各亚组设定科学样本量,保障统计效能与推论广度。
核心暴露因子与结局指标:研究重点暴露因素涵盖口腔变形链球菌(SM)与乳酸杆菌(LB)定量、糖摄入频率、唾液流量、正畸托槽与修复边缘形态等;主要结局包括白垩样斑出现、釉质/牙本质脱矿、龋损进展与继发龋形成等。运用行为问卷与临床评估相结合的方式,获得生物、行为与环境多维度的暴露数据。
检测路径与统计策略:综合应用16S rRNA测序(QIIME2流程)、qPCR菌量分析、共聚焦显微成像、微硬度测试、口腔pH追踪、电极测唾液参数与标准化行为问卷,协同获取定量与可视化数据。统计分析采用χ2/t检验、Logistic回归等多元方法,保障推论严谨性与研究内部效度。
2.2口腔微生物群与龋齿发生的关系
2.2.1定殖建立与早期龋的直接联系
婴幼儿期的口腔生态位在乳牙萌出与行为暴露的双重作用下迅速成形:未完全成熟的釉质提供黏附基底;照护者的唾液交换与共用餐具则增加初始菌源输入。以变形链球菌为代表的早期定殖者依赖葡聚糖合成形成不溶性胞外多糖,使生物膜由可逆吸附转向稳定附着,并在高频含糖喂养的脉冲作用下获得选择性优势。夜间唾液流速显著下降(<0.2 mL/min),酸清除与缓冲延迟,牙面在“低pH-短间隔重复暴露”模式中难以完成再矿化。实证资料显示,当看护者SM负荷较高时,儿童18月龄出现白垩样斑的比值约3~4;夜间瓶喂与高频点心使风险进一步叠加,但规律含氟暴露与规范刷牙可产生保护效应(OR<1)。临床上,上颌前牙颈部与舌侧为典型滞留区,白斑的空间分布与喂养节律具有一致性。
理论上,早期龋的发生可被概括为“菌源输入增加-黏附位点充足-碳水频率升高-酸性选择加剧”的连续过程。干预应聚焦减少唾液交换、拉长含糖间隔、提升含氟清洁可达性,以在定殖-成熟前打断生态建立。
2.2.2菌斑成熟与釉质白斑的因果指向
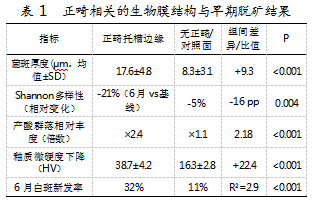
学龄期与青春期因饮食自主性提升与随手可得的含糖饮料,菌斑更易由稀薄层快速过渡为厚层生物膜。扩散屏障形成后,酸在牙面邻近富集,釉质表层首先表现为失光与粉白。正畸托槽与弓丝制造广泛微滞留区,若缺乏边缘定点清洁,生物膜在托槽周缘呈“冠状环”堆积,使白斑与附件周界高度重合,提示成熟生物膜对初发脱矿具有直接因果作用。微区测量数据表明,托槽边缘菌斑厚度约17.6μm,而未矫治同类牙面约8.3μm,随访6个月间,菌群Shan-non多样性下降约21%,产酸群体(SM/LB)相对丰度增加约2.4倍;在pH 4.5模拟唾液中,托槽边缘釉质微硬度下降值显著高于对照组(见表1)。该阶段的核心机制在于“频繁碳水-pH恢复受限-代谢产物内聚-矿物质溶解位移”。其中,清洁可达性与含氟离子可用性是影响再矿化窗口宽度的关键。围托槽的定点刷牙、牙线/间隙刷与稳定氟暴露,能通过削弱扩散屏障与提升矿化驱动力逆转成熟趋势。
2.2.3脱矿加深与酸耐受群落的作用关系
当釉质表层长期处于低pH并出现微孔,病变前沿向牙本质推进,生态选择由“产酸优势”转为“耐酸优势”。乳酸杆菌、放线菌及部分低氧隙定植者在pH 4.5~5.5区间仍可持续代谢,促使软化带扩大;牙本质小管与有机基质降低扩散系数,延长代谢酸与螯合物滞留时间,形成“酸-基质-微隙”正反馈。实证观察提示,唾液流速偏低(<0.7 mL/min)与高黏性甜点频率可显著提升进展风险,而规律含氟暴露与裂隙深部清洁则具备保护效应。影像学上,窝沟龋呈裂隙底向髓侧的三角形扩展,反映深部生态位持续处于低pH。理论分析认为,病变加深并非单由细菌“毒力”决定,而是由频率、时间、扩散3要素协同调控:当含糖脉冲密度超过再矿化阈值,耐酸群落获得稳定位点,加速进展;反之,通过拉长进食间隔、引入裂隙可达清洁与高效氟资源,上调临界pH并缩短酸暴露时长,从群落层面重设选择压力。
2.2.4治疗后生态重建与复发龋的风险关联
修复完成后,口腔并不会“复位”为原始稳态,而是基于人工材料-天然牙体界面形成新的生态边缘。边缘台阶与微渗漏提升初始膜吸附与菌斑再定殖概率—表面粗糙度若超过约0.2μm更利于微生物持留;若抛光与边缘优化不足,生物膜沿边缘带呈线性分布,清洁可达性明显下降。数据表明,边缘台阶>50μm者1年内继发龋风险约为≤50μm者的2~3倍;牙线依从性差也与风险升高相关,按期专业抛光与含氟巩固可显著降低事件率。机制上,复发龋体现为界面微生态位被高频碳水与低可达清洁共同塑形,即产酸/耐酸成员优先回归粗糙或微渗漏区域,形成稳定酸源,矿物质外流阈值被反复触发。治疗后的策略应从“材料学-可达性-化学防护”3层并进:优化边缘几何与抛光,建立邻面机械清洁习惯,配合持久氟暴露与复诊监测,以导向修复体周围的再稳态重建。
3结语
本文从定殖建立、菌斑成熟、脱矿加深到治疗后生态重建4个角度构建了“微生物群-龋齿进展”的连续图像:婴幼儿阶段,亲缘传播与高糖喂养让变形链球菌迅速占位;学龄及青春期,厚层菌斑与酸性代谢共同塑造可视白斑;成人深龋阶段,酸耐受群落借低pH微环境扩张。修复完成后,粗糙边缘与微漏再度为产酸生物提供庇护。阶段性差异提示干预不宜“一刀切”:早期需聚焦菌源屏障与饮食节律;中期强调生物膜控制与脱矿逆转;后期则应关注材料优化与维护依从。未来,多组学并行、实时监测与智能算法有望捕捉菌群波动的早期信号,在病变尚未不可逆前启动精确调控。
参考文献
[1]陈婷.不同年龄龋齿患者口腔微生物群的差异:低丰度类群的启示[J].中国微生态学杂志,2024,36(4):420-430.
[2]陈敏珊,郑娟,李平.口腔微生态的研究进展及益生菌在口腔护理中的应用研究[J].口腔护理用品工业,2023,33(1):4-12.
[3]刘诚敬.口腔微生物及益生菌对口腔疾病的防治[J].罕少疾病杂志,2024,31(2):1-2,8.
[4]闫震,闫秀薇,薛晖,等.儿童防龋齿涂氟对口腔菌群和真菌群的双重影响[J].中国病原生物学杂志,2025,20(2):164-170.










