近十五年国内外茅膏菜化学成分及药理作用的研究进展论文
2026-04-02 14:57:36 来源: 作者:xuling
摘要:茅膏菜是重要的食虫植物和传统药用资源,具有广泛的药理活性。文章查阅了近15年国内外文献资料,综述了茅膏菜化学成分及药理作用的研究进展。
摘要:茅膏菜是重要的食虫植物和传统药用资源,具有广泛的药理活性。文章查阅了近15年国内外文献资料,综述了茅膏菜化学成分及药理作用的研究进展。在化学成分方面,分离鉴定出多种结构的化合物,包括茅膏菜醌、羟萘醌衍生物、黄酮类、酚酸类等。在药理作用方面,国内外研究证实,茅膏菜提取物及其活性成分具有显著的抗菌、抗炎、抗肿瘤等药理活性。
关键词:茅膏菜属;化学成分;药理作用;研究进展
1研究背景
茅膏菜(Drosera peltata Sm.ex Willd.)为茅膏菜科茅膏菜,属多年生食虫草本植物,广泛分布于我国华南、中南及西南各省区,在西藏地区也被藏医广泛应用。其叶片密布紫红色腺毛,能分泌黏液捕食昆虫,有“捕虫草”“苍蝇草”等别称。作为传统中药,茅膏菜全草入药,性味甘辛而平,归肺、脾、胃经,具有祛风除湿、行血止痛、抗菌消炎等功效,在民间常用于治疗风湿痹病、跌打损伤、胃痛、小儿疳积、痢疾及皮肤病等症。茅膏菜化学成分复杂且药理活性多样,近15年(2010—2025年)国内外相关研究逐步深入。本文系统梳理研究进展,为后续开发提供参考。
2茅膏菜化学成分的研究
茅膏菜属植物的化学成分主要包括黄酮类、萘醌类和酚酸类,以及一些植物甾醇类和其他类物质。目前已分离鉴定出37个化合物,具体如图1所示。
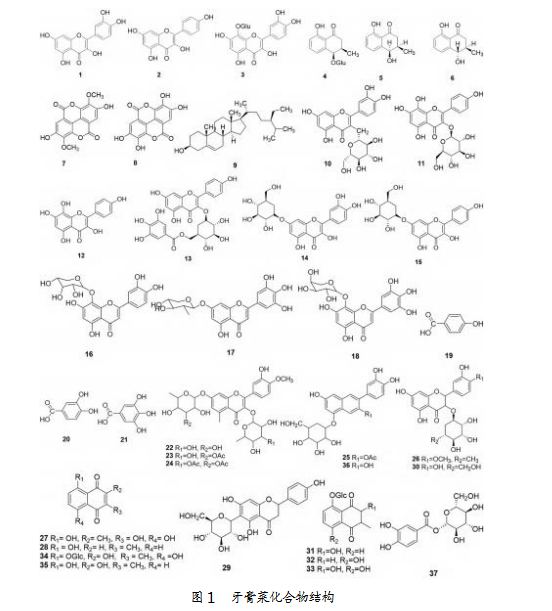
李琳等[1]对茅膏菜的乙醇提取物进行分离鉴定,在乙醇乙酯和水层发现3个黄酮类化合物(1~3),同时分离鉴定出3个萘酮类化合物(4~6)和2个多酚二内酯类化合物(7~8)。此外,化合物9是首次从茅膏菜中分离得到的植物甾醇类化合物。
Braunberger等[2]采用LC-NMR、NMR、LC-MS and LC-DAD等技术对茅膏菜进行定性定量分析,分离鉴定出6种黄酮类化合物(10~15)。其中,化合物14和15为同一黄酮醇母核苷。另外,其团队[3]首次从圆叶茅膏菜植物中发现3个黄酮苷类化合物(16~18),丰富了茅膏菜属植物黄酮类化合物的种类。刘卫建等[4]从西藏产茅膏菜中分离出3个酚酸类化合物(19~21),并确定其化学结构。
OWEN等[5]对麦格纳茅膏菜的粗提取物进行分离鉴定,确定存有3种新的黄酮醇二糖苷(22~24)、一种新的黄烷-3-醇糖苷(25)和12种黄酮醇化合物(26,30)、黄烷-3-醇(36)、黄烷酮(29)、1,4-萘醌(27,28,34,35)、2,3-二羟基萘-1,4-二酮(31,32,33),以及酚酸类(37)。
随着茅膏菜化学成分研究的深入,研究人员采用多种鉴定技术制定了相应的质量标准。白央等[6]采用LC-NMR、NMR和LC-MS方法对总黄酮类含量及鞣花酸衍生物类化合物进行鉴别和含量测定,利用高效液相色谱法对槲皮素进行含量测定,提出黄酮类化合物槲皮素可作为茅膏菜药材真伪的鉴别依据。Sandy等[7]为开发制定统一的茅膏菜质量标准,使用宏观、微观和色谱方法区分多种茅膏菜品种,强调类黄酮和萘醌的含量可作为评价茅膏菜重要的质量参数。
3茅膏菜的药理作用
3.1抑菌作用
现代药理研究发现,茅膏菜醇提物组分及其分离的成分具有良好的抗菌作用。例如,Grevenstuk等[8]通过福林酚法(FC)、托洛克斯等效抗氧化能力(TEAC)和氧自由基抗氧化能力(ORAC)测定法评估长叶茅膏菜的甲醇、水和正己烷提取物的抗氧化活性。结果表明,甲醇提取物具有最高的抗氧化活性(FC:378.6±31.5μmolGAE/mgextract;TEAC:332.2±29.1μmolTE/mgextract;ORAC:64.7±7.8μmolTE/mgextract)。在此基础上,使用琼脂扩散测定法检测长叶茅膏菜的甲醇、水和正己烷提取物对7种细菌和8种酵母菌株的抗菌活性。最低抑菌浓度数据显示,各提取物均表现出强效的抗菌效果和广谱活性。其中,对正己烷提取物最敏感的微生物是表皮葡萄球菌ATCC 12228和白色念珠菌YP0175,最小抑菌质量浓度为13.0μg/mL。正己烷提取物表现出比水和甲醇提取物更强的活性。
李琳等[1]对茅膏菜乙醇提取物的乙醇乙酯和水层进行抑菌实验,发现茅膏菜含有的矶松素、茅膏醌、山柰酚和3,3/-二甲氧基鞣花酸等化学成分能有效抑制稻瘟霉P-2b菌株生长,且矶松素对金黄色葡萄球菌有显著抑制作用。周生军等[9]研究发现,光芎茅膏菜中含有的2种腐蚀性色素和氢氰酸均有抗真菌和角质溶解作用,可杀死皮肤损伤部位的真菌。黄文清[10]指明,茅膏菜水提物及醇提物对沙门氏菌、大肠杆菌和金黄色葡萄球菌生长均有较强的抑制作用。其中,茅膏菜水提物对沙门氏菌、大肠杆菌的最低抑菌浓度(MIC)与最低杀菌浓度(MBC)一致,为62.50 mg/mL;醇提物对金黄色葡萄球菌的MIC与MBC相同,为15.63 mg/mL,且茅膏菜水提物及醇提物对羟自由基有较强的清除作用。
Sandy等[11]测试2种欧洲茅膏菜(圆叶茅膏菜和长叶茅膏菜)及市售单体化合物萘醌、黄酮类和鞣花酸类对3种不同多重耐药大肠杆菌菌株中生物膜基质成分——纤维素和鞭毛状菌毛的形成过程的抑制作用,发现圆叶茅膏菜和长叶茅膏菜粗提物抑制生物膜形成的最低浓度显著低于市售的萘醌、黄酮类和鞣花酸类化合物。与单体化合物相比,圆叶茅膏菜和长叶茅膏菜粗提物对3种多重耐药大肠杆菌菌株均表现出更强的抑制效果,这可能是由于粗提物组分协同作用提高了抑菌效果。
3.2其他药理作用
Paper等[12]在比较圆叶茅膏菜和马达加斯加茅膏菜的抗炎作用中发现,圆叶茅膏菜的乙醇和水提取物、马达加斯加茅膏菜的乙醇提取物均具有良好的抗炎作用,且对炎症的抑制强度明显优于化学药物氢化可的松。进一步实验结果证实,茅膏菜属植物的抗炎作用与黄酮类化合物联系密切,且鞣酸类物质在抗炎效果中也发挥了协同作用。
研究表明,心肌梗死患者的血循环中,血小板中性粒细胞的黏附花结明显增加。黏附花结在血管内皮表面滚动,使紧密接触的细胞相互作用并释放多种生物活性物质,进一步激活损伤内皮细胞并加重栓塞程度。张小超等[13]发现,茅膏菜科中的矶松素能显著减少血小板与中性粒细胞间的黏附作用,以及黏附花结的形成,提示矶松素在限制血栓栓塞疾病方面具有一定的苗头作用。
罗培等[14]研究显示,矶松素可通过抑制NF-κB的活化发挥抗炎镇痛作用。实验指出,矶松素可能通过抑制IκB-α的磷酸化和降解,减缓NF-κB的p65磷酸化而发挥抗炎作用。
7-甲基-5-羟基萘醌(Ramentaceone)是茅膏菜科植物毛毡苔(Drosera aliciae)提取得到的萘醌成分,对各种肿瘤细胞系具有有效的细胞毒活性。ANNA等[15]研究表明,在Ramentaceone处理的人白血病HL-60细胞中观察到凋亡的典型形态学和生化特征。Ramentaceone在细胞周期的sub-G1期呈浓度依赖性增加,诱导细胞凋亡,并使线粒体跨膜电位(ΔΨm)降低。Ramentaceone降低了抗凋亡蛋白Bcl-2与促凋亡蛋白Bax和Bak的比例,诱导细胞色素c的释放,并提高caspase-3的表达。此外,在经Ramentaceone处理的HL-60细胞中还检测到活性氧(ROS)的产生,且自由基清除剂N-乙酰半胱氨酸(NAC)预处理细胞后减弱了Ramentaceone诱导细胞释放ROS及sub-G1期比例。实验结果表明,Ramentaceone可通过ROS介导的线粒体途径诱导细胞发生凋亡。
Asirvatham等[16]通过用茅膏菜的乙醇和水提取物作用道尔顿腹水淋巴瘤和艾尔利希腹水癌模型小鼠了解茅膏菜的乙醇和水提取物对肿瘤相关代谢综合征发展的保护程度。实验结果显示,茅膏菜的乙醇和水提取物在250和500 mg/kg的剂量下促进了模型小鼠血糖升高、激素和脂质谱的变化。结果证实,茅膏菜的乙醇和水提取物可稳定荷瘤小鼠的荷尔蒙、血糖和血脂变化。这可能是由于茅膏菜提取物中存在药理活性植物成分。但其后续工作中并没有对茅膏菜提取物中存在的药理活性植物成分展开分析鉴定。
4结语
茅膏菜作为一种具有悠久药用历史的食虫植物,其化学成分主要包括萘醌类、黄酮类及酚酸类等活性物质。近年来,研究人员不仅从茅膏菜中分离鉴定出多种新化合物,还逐步建立起以黄酮和萘醌为核心的质量评价体系。在药理作用方面,茅膏菜展现出显著的抗菌、抗炎、抗肿瘤及调节代谢综合征等活性,尤其对多重耐药菌的生物膜抑制和通过ROS介导的凋亡机制抑制肿瘤细胞生长具有突出潜力。然而,已有研究仍存在活性成分构效关系不明确、体内药理机制探讨不足等问题。未来应聚焦关键药效物质的作用机制解析,以及资源保护与可持续利用,为茅膏菜在药物开发中的应用提供更充分的科学依据。
参考文献
[1]李琳,黄靖,徐翔华,等.茅膏菜化学成分的研究[J].中国中药杂志,2012,37(2):222-225.
[2]BRAUNBERGER C,ZEHL M,CONRAD J,et al.LC NMR,NMR,and LC MS identification and LC DAD quantification of flavonoids and ellagic acid derivatives in Drosera peltata[J].Journal of Chromatography B,2013,932:111-116.
[3]BRAUNBERGER C,ZEHL,M,CONRAD J,et al.Flavonoids as chemotaxo nomic markers in the genus Drosera[J].Phytochemistry,2015,118:74-82.
[4]刘卫建,胡晓斌,杨培全.西藏产茅膏菜化学成分的研究[J].华西药学杂志,1992(4):201-202.
[5]OWEN E N,HAYDEN T,DAVID P,et al.Phytochemical Profiling and Biological Activity of the Australian Carnivorous Plant,Drosera magna[J].Journal of natural products,2021,84(4):964-971.
[6]白央,王玮,格桑索朗.藏药材茅膏菜质量标准的研究[J].西藏科技,2015(8):73-77.
[7]SANDY G,NICLAS N,NADIN S,et al.Quality parameters for the medicinal plant Drosera rotundifolia L.:A new approach with established techniques[J].Archiv der Pharmazie,2023,357(1):e2300436.
[8]GREVENSTUK T,GONCALVES S,ALMEIDA S,et al.Evaluation of the Antioxidant and Antimicrobial Properties of in vitro Cultured Drosera intermedia Extracts[J].Natural Product Communications,2009,4(8):1063.
[9]周生军,秦临喜,郭柳,等.濒危藏药光萼茅膏菜研究现状与分析[J].中国现代中药,2014,16(3):262-264.
[10]黄文清.茅膏菜不同提取物的抑菌效果及抗氧化能力的研究[J].饲料研究,2019,42(3):54-57.
[11]SANDY G,SEBASTIAN G,CHRISTIAN S.Antibiofilm Activity of Sundew Species against Multidrug-Resistant Escherichia coli Strains[J].International Journal of Molecular Sciences,2022,23(22):13720-13720.
[12]HD P,ELISABETH K,MICHAELA K,et al.Comparison of the antiinflammatory effects of Drosera rotundifolia and Drosera madagascariensis in the HET-CAM assay[J].Phytotherapy research:PTR,2005,19(4):323-326.
[13]张小超,陈鹏,何波,等.矶松素对中性粒细胞与血小板之间相互作用的影响[J].昆明医学院学报,2007(6):10-15.
[14]罗培,黄远帆,葛麟,等.百花丹醌通过抑制NF-κB的活化发挥抗炎镇痛作用[C]//中华中医药学会科技部卫生部.第三届中医药现代化国际科技大会论文集.成都:第三届中医药现代化国际科技大会,2010:223-224.
[15]ANNA K,JOANNA Z,ALEKSANDRA W,et al.Induction of apoptosis in HL-60 cells through the ROS-mediated mitochondrial pathway by ramentaceone from Drosera aliciae[J].Journal of natural products,2012,75(1):9-14.
[16]ASIRVATHAM R,RAJ S S,CHRISTINA M J A.MODULATORY EFFECT OF Drosera peltata JESm ON DEVELOPMENT OF METABOLIC SYNDROME IN TUMOR BEARING MICE[J].Indonesian Journal of Pharmacy,2016,27(4):203-210.










