超高效液相色谱—飞行时间质谱仪筛查动物源性食品中165种兽药残留论文
2024-12-19 11:39:35 来源: 作者:liziwei
摘要:利用超高效液相色谱—飞行时间质谱仪筛查动物源性食品中165种兽药残留。采用含0.2%甲酸的乙腈:水(8:2)作为提取剂,Oasis PRIME HLB通过式净化,以甲醇(含0.1%甲酸)和2.0 mmol甲酸铵溶液(含0.1%甲酸)为流动相梯度洗脱,采用Waters Acquity HSS T3 UPLC色谱柱(100 mm×2.1 mm,1.7μm)分离,电喷雾离子源MSE正离子模式下进行扫描,根据化合物的保留时间、母离子和子离子碎片信息鉴定165种化合物。在猪肉、鱼肉、鸡肉、鸡蛋4种基质165种化合物
摘要:利用超高效液相色谱—飞行时间质谱仪筛查动物源性食品中165种兽药残留。采用含0.2%甲酸的乙腈:水(8:2)作为提取剂,Oasis PRIME HLB通过式净化,以甲醇(含0.1%甲酸)和2.0 mmol甲酸铵溶液(含0.1%甲酸)为流动相梯度洗脱,采用Waters Acquity HSS T3 UPLC色谱柱(100 mm×2.1 mm,1.7μm)分离,电喷雾离子源MSE正离子模式下进行扫描,根据化合物的保留时间、母离子和子离子碎片信息鉴定165种化合物。在猪肉、鱼肉、鸡肉、鸡蛋4种基质165种化合物的平均回收率在53.15%~132.35%。该方法前处理方法简单,能在短时间内实现大批量样品的处理和筛查定性,筛查结果准确可靠,可应用于实际样品的检测。
关键词:动物源性食品;兽药残留;超高效液相色谱—飞行时间质谱;筛查
0引言
兽药是促进畜牧产业发展的重要物质,在农产品的产量提高和品质改善方面发挥着重要作用。它的正确使用直接关系到畜牧产品的质量安全和人们的身体健康。随着动物源性食品的日常消费量不断地增加,越来越多兽药的使用不可避免,在利益驱使下,存在以提高经济利益为目的而非法违规滥用的现象,对兽药残留的监督检验工作也提出了更高的要求。例如2020年4月实施的GB 31650—2019《食品安全国家标准食品中兽药最大残留限量》中规定了104种已批准最大残留限量规定的兽药、154种允许使用但不需要制定残留限量的兽药和9种不得检出的兽药。欧盟与美国相关组织也早已颁布了相关禁限令。
现有的兽药残留的检测技术主要有液相色谱法、气相色谱法、液相色谱串联三重四级杆质谱法、气相色谱串联质谱法和酶联免疫法等。其优点是使用仪器设备较为常规,可以对一部分兽药定性定量检测,缺点是覆盖较多兽药时需要多个方法协同处理,时间成本和工作量较多,难以实现对不同类型不同结构的多种兽药残留进行同时检测、检测耗费时间长。
高分辨质谱是一种分辨率和质量准确度都很高的质量分析器,可在仅使用一种前处理条件和仪器参数下获得抗基质干扰能力强的数据,能够高通量非靶向的分析全部兽药,也具备一定的定量能力,很好的互补了三重四级杆质谱检测宽泛性差、未知化合物筛查能力欠缺的弱点。因此,本文依据农业农村部公告第197号-9-2019、2023年食品安全监督抽检实施细则和2023年国家食品安全评价性抽检实施细则中所有兽药残留化合物,选取165种化合物应用超高效液相色谱—飞行时间高分辨质谱建立标准数据库,在此基础上建立了适用于不同基质(猪肉、鸡肉、鱼肉、鸡蛋)中兽药残留筛查和确证方法,并用于实际样品分析。
1材料与方法
1.1仪器
超高效液相色谱-飞行时间质谱仪(美国Waters公司);Masslynx4.1数据采集软件(美国Waters公司);Unify数据处理软件(美国Waters公司);Milli-Q Reference超纯水发生器(美国Millipore公司);台式高速冷冻离心机(美国Sigma公司)。
1.2试剂
165种兽药标准物质(纯度≥98%,北京振翔科技有限公司和上海安谱实验科技有限公司);甲酸、甲酸钠(质谱级,美国Sigma Aldrich公司);亮氨酸脑腓肽(美国Waters公司);甲醇、乙腈(色谱级,美国天地有限公司)。
1.2.1试剂配制
0.5 mmol甲酸钠溶液:准确称取甲酸钠0.017 g,溶解在500 mL异丙醇:水(90:10)中,将配置好的甲酸钠溶液500 mL于-20℃保存待用,倒入质谱仪上约30 mL的C瓶中,用于每日校正。
200 ng/mL亮氨酸脑啡肽溶液:准确称取亮氨酸脑啡肽3.00 mg,加入7.5 mL水,充分摇匀,超声5 min,配置成400μg/mL储备液(冷冻保持3个月)。准确移取浓度为400μg/mL的储备液50μL置20 mL容量瓶中,用含0.1%甲酸的乙腈:水(1:1)定容至刻度,得到浓度为1μg/mL的中间液(冷冻保存1个月)。准确移取浓度为1μg/mL的中间液4 000μL置20 mL容量瓶中,用含0.1%甲酸的乙腈:水(1:1)定容至刻度,得到浓度为200 ng/mL的使用液。倒入质谱仪上约30 mL的B瓶中,用于样品进样过程中时时校正。
1.2.2标准溶液配制
分别称取固体或移取液体165种兽药的标准品适量,用甲醇配置成1 mg/mL、100μg/mL、10μg/mL的单个标准储备液。在各个标准品推荐温度下保存,1 mg/mL、100μg/mL保存12月,10μg/mL保存6个月。取各个标准储备液适量,用甲醇:水(1:1)稀释成浓度为100 ng/mL标准工作液。165种化合物包括苯甲酰磺胺、磺胺嘧啶、磺胺地索辛、磺胺二甲(基)嘧啶、磺胺多辛、磺胺甲嘧啶、磺胺甲(噻)二唑、磺胺甲氧哒嗪、磺胺苯吡唑、磺胺吡啶、磺胺吡唑、磺胺喹噁啉、磺胺噻唑、磺胺二甲异嘧啶、甲氧苄啶磺胺醋酰(乙酰磺胺)、磺胺对甲氧嘧啶、磺胺间甲氧嘧啶、磺胺氯哒嗪、磺胺甲恶唑(苯磺酰胺)、磺胺二甲异噁唑、西诺沙星、达氟沙星(单诺沙星)、双氟沙星、恩诺沙星、氟甲喹、加替沙星、洛美沙星、麻保沙星、萘啶酸、氧氟沙星、奥比沙星、恶喹酸(奥索利酸)、沙拉沙星、司帕沙星、诺氟沙星、培氟沙星、环丙沙星、依诺沙星、阿苯达唑(丙硫咪唑)、阿苯达唑-2-氨基砜、氨基甲苯咪唑、噻苯达唑(噻苯咪唑)、二甲硝咪唑(地美硝唑)、芬苯达唑(苯硫苯咪唑)、氟苯达唑(氟苯咪唑)、羟基异丙硝唑、异丙硝唑、甲苯咪唑、噻苯咪唑酯(坎苯达唑)、羟基甲苯咪唑、5-羟基噻苯咪唑、左旋咪唑、甲硝唑、奥芬哒唑、丙氧苯咪唑、罗硝唑(洛硝哒唑)、噻克硝唑、替硝唑、三氯苯达唑、苯硫胍、甲基盐霉素、克林霉素、多拉菌素、柱晶白霉素、螺旋霉素、替米考星、泰乐菌素、维吉尼霉素M1、林可霉素、竹桃霉素、红霉素、交沙霉素、倍氯米松、、倍氯米松双丙酸酯、倍他米松双丙酸酯、乙酸氯地孕酮、氯倍他索丙酸酯、氯倍他松丁酸酯、可的松、地夫可特、地塞米松、表睾酮、氟氢可的松、氟米松、氟轻松、氟氢缩松、氟米龙、氟替卡松丙酸酯、哈西奈德、氢化可的松、甲地孕酮、醋酸美仑孕酮、甲基泼尼松龙、莫米他松糠酸酯、泼尼卡酯、睾丸酮、曲安奈德、诺龙、泼尼松、泼尼松龙、班布特罗、羟甲基克伦特罗、克伦塞罗、异克伦潘特、克伦潘特、克伦普罗、非诺特罗、福莫特罗、莱克多巴胺、利托君、沙美特罗、索他洛尔、特布他林、妥布特罗、克伦特罗、溴布特罗、马布特罗、西马特罗、氯苯那林、喷布特罗、对乙酰氨基酚、氯丙嗪、氯羟吡啶、氨苄砜、氟哌啶醇、氮哌醇(阿扎哌醇)、氮哌酮(阿扎哌隆)、丙酰丙嗪、甲苯噻嗪、卡马西平、苯海拉明、氟西汀、丙米嗪、舒必利、氯普鲁卡因、辛可卡因、利多卡因、普鲁卡因胺、普鲁卡因、丁卡因、溴苯那敏、西替利嗪、氟奋乃静、羟嗪、异丙嗪、特菲那定、联苯苄唑、益康唑、灰黄霉素、酮康唑、萘替芬、氟尼辛(氟尼辛葡甲胺)、酮替芬、美利曲辛、奥沙普嗪、安替比林、地西泮、四环素、土霉素、青霉素G、头孢匹林、头孢噻肟、金刚烷胺、金刚乙胺。
1.3样品前处理
准确称取2.0 g(精确至0.01 g)匀浆的样品于50 mL聚丙烯离心管中,加入80%(V/V)乙腈溶液(含0.2%甲酸)10 mL,静置10 min。加入陶瓷均质子,以2 500 r/min旋涡混匀30 min。9 500 r/min高速离心5 min。移取5 mL上清液,以1滴/s流速过Oasis PRiME HLB固相萃取柱(6 mL,200 mg),将过滤液收集后进行氮吹,近干时用1.0 mL初始流动相复溶,过0.22μm滤膜上机检测。
1.4仪器条件
1.4.1色谱条件
色谱柱:Acquity HSS T3 UPLC色谱柱(2.1 mm×100 mm,1.8μm)或等效色谱柱;流动相A为0.1%甲酸甲醇,B为0.1%甲酸+2 mmol甲酸铵水,进样体积2μL;流速0.4 mL/min;柱温40℃;梯度洗脱程序:0~1.0 min,2%A;1.0~15.0 min,2%~98%A;15.0~20.0 min,98%A;20.0~25.0 min,2%A。
1.4.2飞行时间质谱条件
电离模式:ESI+;扫描模式:MSE Continuum;毛细管电压:1.0 kV;脱溶剂气温度:250℃;脱溶剂气流速:600 L/h;采集范围:50~1 000 m/z;低碰撞能量(Low Collision Energy):4 V;高碰撞能量(High Collision Energy):10~40 V;锥孔电压:30 V。
1.5高分辨Unify筛查数据库的构建
利用超高效液相色谱—飞行时间质谱仪对浓度为100 ng/mL的单个标准工作溶液在全扫描模式下检测,通过单因素变量法找到它们的色谱峰保留时间、离子对的精确质量数等信息。采用飞行时间质谱仪自带的Unify软件构建165种兽药残留筛查数据库(化合物名称、离子对精确质量数、保留时间等)。
1.6样品筛查与确证
鉴别分析依据MSE Continuum模式下采集的数据保留时间及精确质量数测定值。检出化合物色谱峰的保留时间和已建立数据库的偏差应不大于±2.5%,同理,母离子精确质量数与已建立数据库的偏差应不大于≤5μg/mL,则初步判断样品中含有该化合物。进一步对疑似阳性样品在MSE Continuum模式下采集的高碰撞能量下的质谱图进行对比,若存在2个及以上丰度较高的碎片离子与数据库中碎片离子质量数的偏差≤10μg/mL,则可以确证试样中含有该种兽药。
1.7样品抽样
此次样品抽样范围主要在省内,主要抽取以种生产企业、养殖户等生产环节和超市、农贸市场等流通环节的样品。抽样人员由3名成员组成,其中至少1名有抽样经验,确保抽样人员身心健康,有良好的沟通和解决问题的能力。其中,鱼肉的的抽样种类包括鲤鱼、草鱼、鲈鱼、鲟鱼等。4种基质样品抽样数量均不少于25个。
2结果与分析
2.1回收率试验
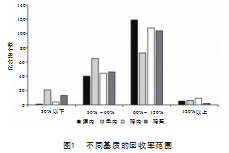
选取空白猪肉、鸡肉、鱼肉、鸡蛋空白样品加入混合标准溶液进行添加回收试验,净化方式考察了Oasis PRiME HLB和Captiva EMR Lipid 2种净化柱的回收率情况,结果表明,165种化合物经Captiva EMR Lipid净化后分析,将4种基质的提取回收率分为4个阶段进行统计,见图1。虽然在4种基质中回收率范围为60%~120%的占比最高,其次为30%~60%,30%以下和120%以上占比最低。但是回收率最低化合物在10%左右,最高200%左右,反映本净化方法存在可改进之处。而经Oasis PRiME HLB净化后的4种基质回收率范围53.15%~132.35%,明显改善了部分化合物较低和较高回收率的情况,故本文采用Oasis PRiME HLB净化柱进行净化。
2.2选择性试验
选取空白猪肉、鸡肉、鱼肉、鸡蛋空白样品、混合标准溶液、加标样品(向空白样品中加入混合标准溶液,加标量为20.0μg/kg),按1.3部分样品前处理方法处理后,以Unify数库中各目标化合物保留时间、母离子信息及子离子碎片信息进行定性分析。结果表明,空白猪肉、鸡肉、鱼肉、鸡蛋背景未见内源性物质干扰,加标样品与混合标准溶液中化合物的保留时间及离子对信息一致。
2.3残留试验
分别进样3针不同基质的高浓度水平(200 ng/mL)猪肉样品溶液后,在进3针空白溶剂,考察165种化合物在整个检测系统的残留情况,结果显示,进完样品溶液后的连续3针空白溶剂未见化合物残留,因此,在分析过程中仅需加1针空白溶剂即可。
2.4实际样品分析
应用建立的方法对省内范围内抽取的种植养殖基地、农民专业合作社、养殖户等农产品生产主体生产的31批猪肉、29批鸡肉、31批鸡蛋、32批鱼肉进行筛查分析,结果显示,共检出化合物有8种化合物。其中3批猪肉中主要检出的化合物有氧氟沙星、磺胺吡啶、磺胺间甲氧嘧啶、甲氧苄定、磺胺甲噁唑。鸡肉在本次抽检中未发现化合物检出,1批鸡蛋中主要检出恩诺沙星。7批鱼肉中主要检出环丙沙星、恩诺沙星、地西泮。
由实际样品分析结果可知,在猪肉、鸡肉、鸡蛋、鱼肉4种基质中鱼肉的兽药残留检出率最高,其次是猪肉。在种植养殖基地、农民专业合作社、养殖户中均存在不合格样品,因此,在动物的养殖过程中,要根据相关要求科学合理应用临床药物,对于未经批准的或假冒伪劣兽药严禁使用。选择使用兽药时,应采取恰当的给药途径,充分掌握不同种类药物对不同动物所规定的休药期。
3结论
本试验采用超高效液相色谱—飞行时间质谱仪,结合165种兽药的高分辨质谱信息,构建了165种兽药数据库,并用于123批动物性食品中兽药残留的筛查。该方法前处理方式简单,可在短时间内实现大批量的样品前处理和筛查定性,筛查结果准确,且筛查数据库能够用于持续监测动物性食品中中的兽药残留情况,本试验基本覆盖了农业农村部公告第197号-9-2019、国家食品安全监督抽检实施细则和食品安全评价性抽检实施细则中规定检测的兽药化合物,在一定程度上实现对畜禽肉和水产品类食用农产品的全面监测,可作为动物性食品中新风险物质发现识别的有力技术工具,为动物性食品中的安全监管提供技术支撑。
参考文献:
[1]Wang B,Xie K Z,Lee K.Veterinary drug residues in animal-derived foods:sample preparation and analytical methods[J].Foods,2021,10(3):555.
[2]Pratiwi R,Ramadhanti S P,Amatulloh A,et al.Recent advances in the determination of veterinary drug residues in food[J].Foods,2023,12(18):3 422.
[3]Wang W S,Liu H H,Zhang Y W,et al.Antihyperlipidemic and hepatoprotective properties of alkali-and enzyme-extractable polysaccharides by dictyophora indusiata[J].Sci Rep,2019,9(1):14 266.
[4]郑耀林,林秋凤,杨乐,等.液相色谱—高分辨质谱技术在兽药残留检测中的研究进展[J].食品科学,2023,44(3):359-365.
[5]陈秋华,张天闻,傅红,等.超高效液相色谱—四极杆飞行时间质谱法快速筛查水产品中16种激素残留[J].食品科学,2018,39(20):337-343.










