高效液相色谱法测定乙型肝炎病毒表面抗体纯度分析论文
2026-01-29 17:49:10 来源: 作者:xuling
摘要:研究旨在运用高效液相分子排阻色谱(SEC-HPLC),建立一种用于测定乙型肝炎病毒表面抗体纯度及生物活性的方法。
摘要:研究旨在运用高效液相分子排阻色谱(SEC-HPLC),建立一种用于测定乙型肝炎病毒表面抗体纯度及生物活性的方法。方法:主要采用Agilent Advance Bio SEC 30 nm色谱柱(4.6 mm×300 mm,2.7μm),以50 mmol/L磷酸盐缓冲液为流动相,流速0.35 mL/min,检测波长280 nm,柱温30℃。结果:本方法显示乙型肝炎病毒表面抗体具有良好线性关系,线性相关系数(R2)为0.999 9;精密度良好,峰面积RSD=0.12%;重复性良好,峰面积RSD=0.07%;稳定性良好,在2~8℃条件下保持96 h内含量稳定,RSD<1.5%;耐用性满足要求,pH值在6.5~7.5范围内,主峰分离度好,回收率高(98.66%)。结论:该方法可作为乙型肝炎病毒表面抗体纯度测定方法。
关键词:乙型肝炎病毒表面抗体;高效液相分子排阻色谱;化学发光免疫分析法
0引言
乙型肝炎病毒(Hepatitis B virus,HBV)是导致乙型肝炎的病原体,属于嗜肝DNA病毒科。HBV感染已经成为一个全球性的公共卫生问题,可引发肝纤维化、肝硬化甚至肝癌[1-2]。乙型肝炎病毒表面抗原(hepatitis B surface antigen,HBsAg)作为HBV包膜蛋白的主要成分,是HBV感染后最早出现的血清学标志物[3]。临床上常用乙型肝炎病毒表面抗原测定试剂盒检测血清标志物,确认是否感染HBV[4]。因此控制试剂盒中的乙型肝炎病毒表面抗体(hepatitis B surface antibody,HBsAb)质量,是控制检测准确性的关键。目前业内普遍采用聚丙烯酰胺凝胶电泳(polyacrylamide gel electrophoresis,PAGE)的方法控制抗体纯度,但方法灵敏度、特异性和准确性相对较差[5]。因此,本研究尝试运用灵敏度高、专属性好的高效液相分子排阻色谱(size exclusion chromatography-high performance liquid chromatography,SEC-HPLC)技术来分析和控制HBsAb的纯度,为体外诊断试剂厂家控制HBsAb的质量提供依据和指导。
1材料与方法
1.1测定材料及仪器
仪器Agilent 1260液相色谱仪(Agilent,型号:1260)。
试药HBsAb供试品(深圳市雅为世纪科技有限公司,批号:20230108);HBsAb对照品(深圳市雅为世纪科技有限公司,批号:20210722)[6]。
1.2使用方法
色谱柱:Agilent AdvanceBio SEC 30 nm(4.6 mm×300 mm,2.7μm);流速:0.35 mL/min;柱温:30℃;检测波长:280 nm;进样量:10μL;进样器温度:4℃:柱温:25℃。
1.3溶液制备
对照品/供试品溶液的制备:分别移取HBsAb对照品或供试品,加流动相A配制成每1 mL含1 mg的溶液,涡旋混匀。
阴性对照制备:以流动相作为阴性对照溶液。
2测定结果
2.1系统适用性测定
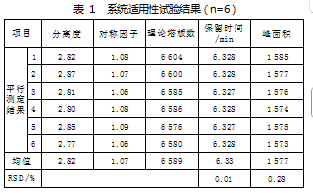
取20μL阴性对照品注入色谱柱进行测定,确认系统状态正常后,取100μL的供试品溶液,重复进样6次,如表1特征峰的分离度为2.82,保留时间6.33 min,拖尾因子1.07,理论塔板数6 588,峰面积RSD=0.28%,保留时间RSD=0.01%。
2.2专属性测定
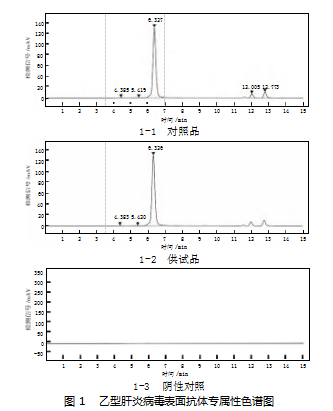
取20μL的对照品、供试品及阴性对照溶液,分别注入色谱柱,结果见图1,对照品与供试品溶液色谱图中HBsAb色谱峰的理论塔板数均大于3 000,阴性对照品在HBsAb的色谱峰保留时间处无吸收峰,表明该方法专属性好。
2.3精密度测定
取100μL的对照品溶液,重复进样6次,结果显示对照品溶液的峰面积RSD=0.12%,保留时间RSD=0.01%,表明精密度良好。
2.4重复性测定
取100μL供试品溶液,重复进样6次,结果显示供试品溶液的峰面积RSD=0.07%,保留时间RSD=0.01%,表明具有较好的重复性。
2.5线性关系测定
移取对照品批次的乙型肝炎病毒表面抗体适量,用流动相A稀释成质量浓度为0,0.125、0.25、0.5、1.0、2.0 mg/mL的标准溶液。分别取20μL进样,每个浓度点重复3次。以质量浓度为横坐标,峰面积为纵坐标绘制标准曲线,得线性回归方程Y=1 711.9X-27.384(R2=0.999 9),表明HBsAb在0~2.0 mg/mL范围内呈良好的线性关系。将每个质量浓度点的峰面积带入回归方程,得到每个质量浓度点实测浓度,计算回收率的RSD(n=3)均不大于1.0%,平均回收率在90.0%~101.0%,表明该方法准确度良好。
2.6稳定性测定
取供试品溶液适量放置于2~8℃冰箱中保存,分别于放置0、12、24、48、96 h时5个不同时间点取20μL进样测定,将峰面积代入上述回归方程计算质量浓度。结果显示峰面积及质量浓度相对标准偏差分别为1.18%、1.16%,均不大于2.0%,表明供试品在2~8℃条件下保存96 h内较为稳定。
2.7耐用性
使用pH为6.5、7.0、7.5三种不同pH的流动相分别对系统平衡2h,每种pH条件平衡后取对照品溶液适量重复进样3次。经考察,pH值在6.5~7.5范围内变化,色谱峰峰形对称、尖锐,主峰分离度较好,且理论塔板数不低于6 000,说明该方法具有较好的耐用性。
3结论
HBV感染作为全球性的公共卫生问题,可引发多种肝脏疾病甚至肝癌。因此加强乙型肝炎病毒的检测准确性,提前干预病毒传播,降低乙型肝炎病毒感染风险至关重要。SEC-HPLC是基于蛋白质相对分子质量大小在凝胶色谱柱内不同的分配行为实现分离,该方法分离能力强、重现性好,广泛应用于蛋白类药物纯度控制,但体外诊断试剂质量控制运用鲜见报道。本研究将其运用于乙型肝炎病毒表面抗原测定试剂盒的核心成分HBsAb纯度质量控制研究,为此技术应用于体外诊断试剂领域提供依据。基于此,从以下方面阐述方法建立考量:
1)检测波长的选择。蛋白质在280 nm波长处具有最大吸收度,经全波长图谱分析确认HBsAb在280 nm附近有最大吸收,故选择280 nm作为检测波长。
2)流动相条件选择。蛋白质及多肽采用高效液相色谱-分子排阻色谱法测试,使用的流动相通常为水溶液或缓冲溶液pH值在2~8范围。因此选择MES溶液、PBS溶液、Tris溶液三种,经验证发现由磷酸二氢钠与磷酸氢二钠组成的PBS缓冲溶液(pH值调至7.00)为流动相,色谱峰的对称性及理论塔板数均良好,并且可以保证色谱峰与杂质峰能有效分离,不干扰两者定量测定。
3)方法学验证。本研究为证明SEC-HPLC方法能准确检测HBsAb的纯度,达到控制产品质量的目的,参照国际ICH方法学验证原则进行方法学验证,内容覆盖系统适用性、线性、专属性、精密度、重复性、稳定性、耐用性,结果表明,建立的SEC-HPLC分析方法专属性强,检验灵敏度高,线性范围广,重复性与耐用性好,可用于体外诊断试剂乙型肝炎病毒表面抗原试剂盒核心原料的质量控制。
综上所述,SEC-HPLC方法可快速对HBsAb进行纯度分析,方法专属性强、灵敏度高,适合体外诊断试剂厂家对HBsAb的质量控制,进而有效控制临床使用的乙型肝炎病毒表面抗原试剂盒的质量。
参考文献
[1]郑志境.乙肝表面抗原和表面抗体同时阳性对乙肝性肝癌的预测价值[J].中国现代药物应用,2023,17(9):79-82.
[2]万千,陈诹,张鸿等.上海浦东新区15~65岁人群乙肝感染状况及危险因素分析[J].公共卫生与预防医学,2024,35(5):33-36.
[3]龚敏莉,罗微,毕月等.血清低水平乙肝病毒表面抗原的临床意义分析[J].巴楚医学,2024,7(2):86-91.
[4]龚敏莉,罗微,毕月等.血清低水平乙肝病毒表面抗原的临床意义分析[J].巴楚医学,2024,7(2):86-91.
[5]毛秀荣,李雷,朱俊,等.浅析聚丙烯酰氨凝胶电泳实验中常见问题及解决方法[J].工作研究,2022,34(7):95-102.
[6]邓琳琳,甄乾娜,高洁莹,等.高效液相色谱法同时测定妊娠合并乙型肝炎患者血浆中的吲哚与3-甲基吲哚[J].色谱,2017,35(7):735-740.










