Ni/Al2O3催化葡萄糖超临界水气化制氢性能强化机制研究论文
2024-12-27 14:10:12 来源: 作者:dingchenxi
摘要:超临界水气化湿生物质转化为清洁氢能,具有广阔的应用前景。本工作研究纤维素水解产物-葡萄糖超临界水气化制氢Ni/Al2O 3催化剂的影响。
摘要:超临界水气化湿生物质转化为清洁氢能,具有广阔的应用前景。本工作研究纤维素水解产物-葡萄糖超临界水气化制氢Ni/Al2O 3催化剂的影响。实验结果表明,Ni/Al2O 3催化剂可以有效促进葡萄糖气化生产氢气,在Ni/Al2O 3作用下,葡萄糖的碳气化率可达90.8%,氢选择性达87.1%,总产气量和H2产量分别为82.12 mol/kg和48.73 mol/kg,是K2CO 3催化剂的3.0倍和3.2倍。气化机理研究表明Ni/Al2O 3能促进葡萄糖形成更多小分子有机物,有利于生物质的热解反应和蒸汽重整反应生成更多的H2和CO 2。该研究为后续进一步研究Ni/Al2O 3催化纤维素类原生生物质气化制氢提供一定的参考意义。
关键词:生物质;超临界水气化;葡萄糖制氢;产物分布;Ni/Al2O 3催化剂
0引言
可再生的生物质资源可作为未来清洁能源的主要来源,具有广阔的开发前景。随着氢能的推广应用,如何高效利用生物质资源制取富氢能源成为当前上游制氢领域的研究热点。超临界水催化气化已经被证实是处理生物质资源如秸秆、稻壳、藻类等含水过量的生物质并转化为富氢气体的有效技术,催化剂的加入可以进一步加速气化效率和提高氢气产量,同时还可降低反应条件,从而提高技术效益[1-3]。此前研究发现,碱金属催化剂可以增强有机底物气化效率和产氢量,但均相催化剂存在催化剂难以回收再利用以及腐蚀设备等问题[4]。金属镍被证明对C-C、C-H键有很好的催化活性[5]。进一步的,使用水热稳定的氧化物(如氧化铝)负载活性金属Ni制备负载型催化剂可以进一步提高Ni的分散度,提高镍催化剂的催化活性和催化剂稳定性[6]。本工作采用纤维素的水解单体葡萄糖作为生物质原料,探究Ni/Al2O3对葡萄糖催化气化特性的影响,本研究采用浸渍法制取Ni/Al2O3负载型催化剂,并通过对比其与非催化和碱金属催化剂K2CO3的催化性能,验证了该Ni/Al2O3是一种高效催化超临界水气化葡萄糖产氢的催化剂。该研究对进一步研究Ni基负载型催化剂促进超临界水气化纤维素类生物质制氢提供了一定的参考意义。
1实验部分
1.1实验材料
D-(+)-葡萄糖(C6H12O6,AR级)购自上海阿拉丁生化科技股份有限公司;六水合硝酸镍(Ni(NO3)2·6H2O,AR级)、碳酸钾(K2CO3,纯度>99.0%)、氧化铝(Al2O3,99.99%metals basis)购自上海迈瑞尔。
1.2催化剂制备
Ni/Al2O3催化剂采用调pH值等体积浸渍法制备。首先称取一定质量的六水合硝酸镍(由Ni负载量确定)溶解于对应质量的氨水溶液中(NH3的质量浓度为5 mol/L),浸渍液的pH值大于11并确保配置的浸渍溶液的体积与Al2O3的孔隙体积相等。随后使用胶头滴管将上述溶液逐滴均匀浸入Al2O3载体并手动搅拌。将浸渍后材料放置于通风橱室温陈化2 h后放入100℃烘箱中过夜烘干。随后放入马弗炉中,以5℃/min程序升温升至600℃并保持该温度煅烧2 h。冷却后,将煅烧后的固体粉末送入还原炉中,在H2氛围下,10%H2/Ar混合气流速为40 mL/min,5℃/min程序升温至550℃,保持该温度还原2 h。待冷却结束,将固体粉末取出,并尽可能研磨成细小粉末后,样品管收集并标记为Ni/Al2O3催化剂。
1.3催化剂性能评价
本实验采用间歇釜式超临界水气化反应装置,主要包括Inconel 625反应釜(有效容积为100 mL)、可加热范围为0~900℃的电加热炉、控温范围为0~750℃的温度控制器、压力传感器、热电偶。反应装置最高承受压力为32.5 MPa,最高温度为750℃。实验分为三组:非催化组(空白对照组)、Ni/Al2O3催化组和K2CO3催化组。以一次Ni/Al2O3催化组实验为例,主要实验流程如下:称量一定质量的Ni/Al2O3和葡萄糖(催化剂与葡萄糖质量比为1∶1)先后加入反应釜中,随后加入一定质量的去离子水,摇晃反应釜使其尽可能均匀混合。通过法兰和纯石墨垫片密封,密封后通入一定压力的氩气吹扫反应釜2~3次,排除釜内空气同时验证装置的气密性良好。完成以上准备工作后,调控反应压力位于22.5~25 MPa,通入一定压力的氩气作为初始压力。反应通过电加热炉加热至预定温度,保持反应温度一段时间后,移除电加热炉。等待反应釜自然冷却至室温,使用气袋收集气体产物送入气相色谱进行检测,并采用针式注射器测量气体产物总体积。
本实验气体检测采用Agilent公司的8860GC气相色谱仪(GC)对气体产物进行检测,该仪器配备火焰电离检测器(FID)和热导检测器(TCD)可以检测H2、CO2、CO、CH4和C2烃类。气体产物通过碳气化率、氢选择性、总产气量和气体组成进行评价,见式(1)—式(4)。

2实验结果与讨论
本实验操作参数的选择基于超临界水气化反应中相对温和的条件而确定。在反应温度为500℃,葡萄糖浓度(质量分数)为2%和反应压力范围为22.5~25 MPa条件下,以葡萄糖作为生物质原料探究Ni/Al2O3催化剂对生物质超临界水气化的影响。碱金属催化剂被认为是气化纤维素类生物优秀的催化剂选择,因此选择K2CO3作为碱金属催化剂进行对比[1]。图1展示了葡萄糖在催化/非催化条件下超临界水气化的性能比较。在Ni/Al2O3催化下,葡萄糖碳气化率达到了90.8%,为同等条件下非催化(28.1%)的3.2倍。此外,Ni/Al2O3具有优异的氢选择性,气体产物中87.1%的氢集中在H2中,较非催化条件下(42.3%)提高了2.1倍,证实了其具备不俗的催化葡萄糖超临界水气化制取H2的潜在前景。对比公认生物质催化气化效果较好的碱金属催化剂K2CO3,其碳气化率仅为Ni/Al2O3的46.1%,氢选择性为Ni/Al2O3的76.3%。更高的碳气化率和氢选择性可能是由于Ni/Al2O3有利于葡萄糖上C-C、C-H和O-H键的断裂,促进有机物大分子向小分子气体转化[6]。证明了Ni/Al2O3是促进葡萄糖催化气化制氢行之有效的良好催化剂。
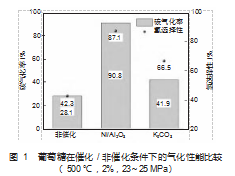
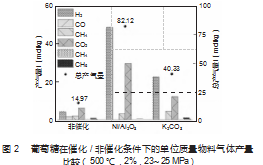
图2直观展示了在催化/非催化条件下,单位质量物料各气体产量的具体数值。Ni/Al2O3显著增加了气体的产量,单位质量物料总产气量达82.12 mol/kg。而K2CO3催化气化的总产气量仅为Ni/Al2O3的49.1%(40.33 mol/kg),从产量变化看,Ni/Al2O3的催化效果与K2CO3类似,主要促进了葡萄糖向H2和CO2的产生转变,引起了总产气量上的显著提高。同时在Ni/Al2O3的加入下,H2的产量提高至48.73 mol/kg。相对于K2CO3催化剂,Ni/Al2O3对葡萄糖的转化更彻底,几乎未观察到C2气体的生成。这可能是由于Ni/Al2O3抑制了有机大分子断裂后产生的小分子重新脱水缩合成大分子焦油的发生。
研究表明当催化剂加入后,会降低部分反应所需的活化能,促进某些反应的进行[6]。图3展示了催化/非催化条件下,葡萄糖催化气化气体产物的组成分布。图3清晰反映出催化剂加入显著改善气体组成分布。对比Ni/Al2O3和K2CO3催化剂对产氢影响,同样发现二者对产氢有着相似催化效果(59.3%和55.9%),明显区别非催化条件。这可能是由于催化剂的存在促进了葡萄糖分子断键产生更多小分子有机物,有利于蒸汽重整和热解反应等产气反应的进行,从而产生更多的H2。另一方面,Ni/Al2O3催化剂似乎对逆向甲烷化反应和水气变换反应有影响。CO作为反应的中间产物,虽然在体系中存在的含量较低,但对整个气体组成分布起到不可忽略的作用。Ni/Al2O3催化下,更多的CO参与逆水气变换反应而不是甲烷化反应,这一点对比Ni/Al2O3较K2CO3更多的H2/CO2占比(59.3%/36.3%和55.9%/30.7%)和更少的CH4占比(4.1%和11.4%)可以得到验证。此外,Ni/Al2O3催化下,葡萄糖气体产物以清洁的H2和CO2为主(总占比95.6%),利于后续气体的分离和提纯。
3结论
本实验通过间歇釜式超临界水气化反应装置对葡萄糖进行了催化/非催化条件下气化特性研究,探究了Ni/Al2O3对比K2CO3产生的气化特性影响,主要结论如下:
1)本实验中,Ni/Al2O3催化葡萄糖超临界水气化在500℃、2%、22.5~25MPa条件下,葡萄糖的碳气化率可达到90.8%,氢选择性达到87.1%,同时总产气量达到82.12 mol/kg。实验结果证明,Ni/Al2O3催化剂不仅可以实现葡萄糖生物质的有效气化,并且具备良好的制氢潜力。
2)K2CO3催化剂已被证实为生物质催化气化良好的催化剂,而Ni/Al2O3催化剂总产气量和H2产量较之分别提高了2.0倍和2.2倍,同时碳气化率和氢选择性也提高了2.2倍和1.3倍。此外Ni/Al2O3作为负载型催化剂,具有便于回收、对反应釜腐蚀性低等优点,证实了Ni/Al2O3催化葡萄糖气化具有良好前景,对纤维素类生物质催化气化及Ni/Al2O3催化剂工业推广应用具有一定的参考意义。
参考文献
[1]GHODKE Praveen Kumar,SHARMA Amit Kumar,JAYASEELAN Arun,et al.Hydrogen-rich syngas production from the lignocellulosic biomass by catalytic gasification:A state of art review on advance technologies,economic challenges,and future prospectus[J].Fuel,2023,342:127800.
[2]WEI Ning,XU Donghai,HAO Botian,et al.Chemical reactions of organic compounds in supercritical water gasification and oxidation[J].Water Research,2021,190:116634.
[3]KHANDELWAL Kapil,NANDA Sonil,BOAHENE Philip,et al.Conversion of biomass into hydrogen by supercritical water gasification:a review[J].Environmental Chemistry Letters,2023,21(5):2619-2638.
[4]GONG Weijin,HUANG Lei,GUO Lina,et al.Catalytic gasification of textile wastewater treatment sludge for hydrogen production in supercritical water with K2CO3/H2O2:Reaction variables,mechanism and kinetics[J].International Journal of Hydrogen Energy,2023,48(78):30310-30322.
[5]SıNAĜAli,KRUSE Andrea,RATHERT Jens.Influence of the Heating Rate and the Type of Catalyst on the Formation of Key Intermediates and on the Generation of Gases During Hydropyrolysis of Glucose in Supercritical Water in a Batch Reactor[J].Industrial&Engineering Chemistry Research,2004,43(2):502-508.
[6]XU Gong-xun,NANDA Sonil,GUO Jing-jing,et al.Red mud supported Ni-Cu bimetallic material for hydrothermal production of hydrogen from biomass[J].Industrial Crops and Products,2024,212:118370.










