EDTA系列金属螯合物与氮化碳复合材料的氧还原性能调控研究论文
2024-06-25 11:15:56 来源: 作者:xujingjing
摘要:本文研究了EDTA系列材料的氧还原性能,探究了将三聚氰胺、尿素、二氰二胺等不同氮源与EDTA系列复合形成的碳负载过渡金属材料的氧还原性能变化。CV和LSV曲线显示,该系列前驱物和氮化碳复合后的材料比直接煅烧的材料表现出更优异的氧还原性能,其中二氰二胺对其性能提升影响最大。
摘要:本文研究了EDTA系列材料的氧还原性能,探究了将三聚氰胺、尿素、二氰二胺等不同氮源与EDTA系列复合形成的碳负载过渡金属材料的氧还原性能变化。CV和LSV曲线显示,该系列前驱物和氮化碳复合后的材料比直接煅烧的材料表现出更优异的氧还原性能,其中二氰二胺对其性能提升影响最大。
关键词:EDTA;氧还原;氮化物
0引言
能源是人类社会赖以发展的基础支柱,随着能源的日益短缺,开发一种可再生能源具有重要意义。其中,燃料电池由于能量密度高、利用效率高等的优势而备受研究人员青睐[1]。然而,燃料电池迄今无法大规模使用的原因在于其阴极的氧还原反应存在动力学迟滞问题以及存在成本瓶颈[2]。近年来,氧还原催化剂的发展从商用的Pt基贵金属催化剂到非贵金属催化剂再到单原子催化剂等。研究人员致力于寻求一种高效率、低成本、可应用的氧还原阴极催化剂。在这样的大背景下,一些具有丰富官能团和特殊结构的前驱物体系如乙二胺四乙酸(EDTA)[3]、柠檬酸[4]、酞菁大环[5]等引起了一波研究热潮。其中,EDTA作为一种具有优秀螯合能力的前驱物备受青睐,它是一种常见的络合剂,具有非常强的配位能力,可以和Fe2+,Co2+,Cu2+等二价金属离子络合形成稳定的金属盐[3],且具备丰富的如羟基、羧基和氨基等官能团[6],是一种较为理想的碳源,而该系列金属盐是较为理想的过渡金属源。在过渡金属-氮-碳材料中,当前的主流观点认为氧还原的活性位是碳载体上被N原子修饰的边缘缺陷,而形成该种缺陷的氮源种类繁多,选择范围较广[7]。氮化碳由于具有和石墨烯类似的六元环结构,在热处理过程中,能确保催化活性更高的如吡啶氮被掺杂到多孔结构中,增加电子捕获及传送的效率,此外,形成的孔状结构有利于暴露更多的活性位点,用于结合游离的过渡金属离子,加快氧还原进程,因此氮化碳是一种较为理想的氮源[8]。
Liu等[9]首次报道以EDTA为碳源,三聚氰胺为氮源等一步法合成钴掺杂的多孔碳材料,表现出优异的活性及远超商用催化剂的稳定性和耐用性。Zhang[7]探究了不同氮源和金属源用量对氧还原催化活性的影响。Qiu[10]采用软模板法包覆二氰二胺,得到稳定性好的氧还原催化剂。Wang等[11]以不同比例的四水合乙酸钴和三聚氰胺混合作为前驱体,热解制得具有优异电化学性能的Co-N-C催化剂。然而,以EDTA体系作为前驱物制备得到的材料的氧还原性能调控仍未作出系统的比较结果,而过渡金属掺杂碳材料作为重要组成部分,对特定前驱物的调控研究仍具有一定意义。
基于EDTA系列物质的特定结构和固有性质,本文将该系列金属盐作为过渡金属源,将三聚氰胺、尿素、二氰二胺等作为富氮源,探究该系列过渡金属材料与氮化碳材料有机结合策略的可行性。氮源与金属源在热处理过程中可原位形成具有金属-Nx配位形式的活性位点,氮化碳包裹的过渡金属活性材料能够有效保护活性位点不受电解的侵蚀并且加速电荷转移,从而提高催化位点的利用率。对热处理得到的材料进行酸洗可以除去大部分未被碳层包覆的颗粒,留下的大多是金属原子位点,对EDTA系列金属螯合物与氮化碳复合材料的氧还原性能调控的研究在一定程度上能对该系列前驱物做单原子催化提供借鉴意义。
1实验部分
1.1实验步骤
1.1.1碳材料直接煅烧法的制备
分别称取乙二胺四乙酸、乙二胺四乙酸铁单钠盐、乙二胺四乙酸二钠钴盐水合物、乙二胺四乙酸二钠铜四水合物、乙二胺四乙酸二钠锰盐水合物和乙二胺四乙酸二钠锌盐水合物各2 g,研磨后移至管式炉中,N2气氛下,升温速率为5℃/min加热至550℃,保温4 h,继续升温至700℃保温2 h。自然冷却后,用1 mol/LHCl酸浸洗涤,水洗、醇洗过滤后烘干备用。
1.1.2氮化碳复合材料的制备
分别以尿素、三聚氰胺和二氰二胺为氮源、EDTA系列金属盐(Fe、Co、Cu、Mn、Zn)为过渡金属源,对前驱体的比例等进行调控研究。一般情况下,尿素、三聚氰胺和二氰二胺经550℃、4 h会聚合形成浅黄色的氮化碳,因此称取1 g金属盐和1 g氮化物前驱物于玛瑙研钵中,研磨均匀后同2.1.1实验步骤得到过渡金属基氮掺杂碳材料。
1.2氧还原性能测试
1.2.1氧还原测试系统
本文采用上海辰华的CHI760e型电化学工作站进行氧还原测试。使用典型的三电极测试系统,催化剂涂覆的玻碳电极作为工作电极,石墨棒和Ag/AgCl分别作为对电极和参比电极。此外,文中所有的电位表示已转换为可逆氢电极(RHE)。
1.2.2工作电极的制备
本文使用Pine旋转环盘电极进行表征。采用的电极为直径为5 mm的盘电极。
催化剂墨水制备过程:称取催化剂5 mg,加入700μLDI水、250μL异丙醇和50μL 5%质量分数Nafion的混合溶剂,室温下超声处理1 h,形成均匀的墨水。随后,取10μL制得的墨水均匀涂覆在已打磨的玻碳电极上,室温下干燥待测。
1.2.3循环伏安测试
循环伏安法(CV)是一种常用的电化学研究方法。根据曲线中峰的形状、位置等可判断电极材料在所在压力区间内的电化学氧还还原性能的好坏,对于一个新的电化学体系,首选的测试方法为循环伏安法。
1.2.4线性扫描伏安法
线性扫描伏安法(LSV)实际上是循环伏安曲线中氧还原的一部分,称为极化曲线。一般对于非贵金属催化剂,扫描方向为负扫。测试电压为1.2 V~0 V。在进行调控探究时,控制旋转圆盘电极的转速统一为1 600 r/min。该转速下能较为直观地展现出材料的氧还原性能。主要参照的3个指标分别为起始电势、半波电势和极限扩散电流密度。
2结果与讨论
2.1 EDTA体系煅烧材料的氧还原性能
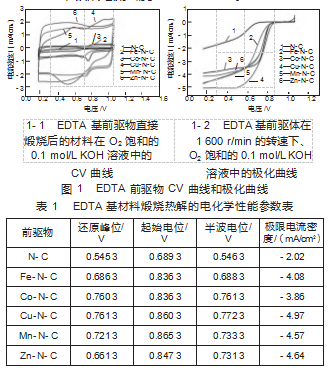
直接煅烧前驱物是一种简单且高效的合成杂原子或过渡金属掺杂的碳纳米材料的重要方法。为了探究EDTA体系前驱物的氧还原性质,将其进行直接煅烧,结果如图1所示,详细性能参数可见表1。从CV图和LSV图中可以看出,纯N-C材料表现出最弱的氧还原性质,随着过渡金属Fe、Co、Cu、Mn、Zn等的掺杂,表现出更正的电位和更大的极限电流密度,分散的金属原子能促进氧还原性能[12]。其中,在EDTA体系里,直接煅烧形成的Cu-N-C材料表现出最优异的氧还原性能,起始电位可达0.860 3 V,半波峰位0.772 3 V,极限电流密度-4.97 mA/cm2。
2.2不同氮源对EDTA体系氧还原性能的影响
对EDTA过渡金属体系和不同氮源的复合煅烧材料氧还原性能进行了测试。结果如图2所示,不同的氮源对EDTA体系氧还原性能影响程度因前驱物不同而异。如图2-1所示,氮源为尿素时,Co的还原峰位为0.738 3 V,其他金属表现出较弱的性能,于是根据1 600 r/min下的LSV(图2-2),Co、Cu、Fe、Mn、Zn的起始电位分别为0.819 3、1.023 3、0.986 3、0.684 3、0.991 3、1.022 3 V,半波电位为0.679 3、0.735 3、0.689 3、0.684 3、0.669 3 V,极限电流密度为-4.25、-4.64、-3.87、-4.06、-2.20 mA/cm2,与直接煅烧相比,起始电位分别提升-2.03%、18.95%、17.94%、14.56%、20.65%。氮源为三聚氰胺时,如图2-3和2-4所示,Co、Cu、Fe、Mn、Zn的还原峰位分别为0.761 3、0.516 3、0.712 3、0.545 3、0.541 3 V,起始电位为0.859 3、0.729 3、0.875 3、0.682 3、0.677 3 V,半波电位为0.773 3、0.518 3、0.714 3、0.699 3、0.594 3 V,极限电流密度为-4.13、-2.33、-4.46、-1.42、-1.35 mA/cm2,与直接煅烧相比,起始电位分别提升20.65%、-15.23%、4.66%、-21.15%、-20.06%。氮源为二氰二胺时,如图2-5和2-6所示,Co、Cu、Fe、Mn、Zn的还原峰位分别为0.772 3、0.533 3、0.864 3、0.495 3、0.603 3 V,起始电位为0.911 3、0.688 3、0.906 3、0.668 3、0.751 3 V,半波电位为0.772 3、0.551 3、0.772 3、0.569 3、0.666 3 V,极限电流密度为-4.73、-2.45、-4.69、-1.54、-2.12 mA/cm2,与直接煅烧相比,起始电位分别提升8.97%、-19.99%、8.37%、-22.77%、-11.33%。
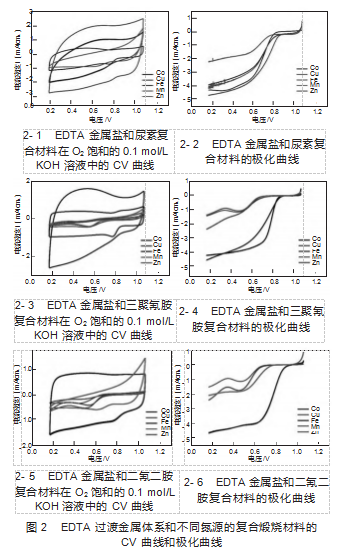
所以,在EDTA金属盐体系中,二氰二胺对氧还原的性能提升得最为明显,其次是三聚氰胺,最后是尿素。然而相较于直接煅烧得到的过渡金属催化剂,通过煅烧复合前体性能提升变化并不明显,未达到理想状态,无法替代商用Pt/C。可能原因在于原有的缺陷位点由于氮化碳的存在,使得N原子占据了过渡金属的位置[7],故氧还原性能有所提升但不明显。
3结论
本文以EDTA体系作为碳氮前驱体来合成氮掺杂的碳材料,考察了该体系的氧还原性能。CV和LSV曲线表明,该体系与不同氮源复合后能提升一定的性能,二氰二胺对EDTA-Fe、EDTA-Co性能提升促进最为明显。
参考文献
[1]Dong,Y,Wu,Y,Liu,M,et al.Electrocatalysis on shape-controlled ti-tanium nitride nanocrystals for the Oxygen reduction reaction[J].Chemsus Chem,2013,6(10):2016-2021.
[2]韩国康.碳基Cu单原子电催化剂的制备与氧还原性能研究[D].哈尔滨:哈尔滨工业大学,2021.
[3]Lo Vecchio C,Arico A S,Monforte G,et al.EDTA-derived Co-N-C and Fe-N-C electro-catalysts for the oxygen reduction reaction in acid environment[J].Renewable Energy,2018,120:342-349.
[4]Niu H J,Zhang L,Feng J J,et al.Graphene-encapsulated cobalt nanoparticles embedded in porous nitrogen-doped graphitic carbon nanosheets as efficient electrocatalysts for oxygen reduction reaction[J].Journal of Colloid and Interface Science,2019,552:744-51.
[5]Ki Hwan Koh,Sung Hyun Noh,Tae-Hyun Kim,et al.A graphene quantum dot/phthalocyanine conjugate:a synergistic catalyst for the oxygen reduction reaction[J].RSC Advances,2017(7):26113-26119.
[6]樊祥博.改性生物质炭复合天然高分子水凝胶的制备及其吸附性能研究[D].镇江:江苏大学,2022.
[7]张晶.非贵金属/氮共掺杂碳催化剂的制备及其电催化氧还原性能与机理研究[D].太原:太原理工大学,2014.
[8]孙启锋,欧昌锐,廖亚林,等.氮掺杂三维多孔石墨烯的孔隙结构与锌-空气电池氧还原电催化性能的关系(英文)[J].Journal of Central South University,2023,30(5):1490-1511.
[9]Liu Z,Zhang G,Lu Z,et al One-step scalable preparation of N-doped nanoporous carbon as a high-performance electrocatalyst for the oxy-gen reduction reaction[J].Nano Research,2013,6(4):293-301.
[10]邱庆超.氮、硫掺杂Fe C基氧还原催化剂的制备及电催化性能研究[D].泉州:华侨大学,2016.
[11]王展昊,王杰,吴爱民,等.Co-N-C碱性氧还原催化剂的合成与性能研究[J].电源技术,2023,47(4):489-492.
[12]冷雷鹏.钴基氮掺杂碳电催化剂制备及氧还原性能研究[D].大庆:东北石油大学,2022.










