基于基团贡献法的生物柴油比定压热容的理论研究论文
2024-05-25 14:59:44 来源: 作者:zhoudanni
摘要:生物柴油是将植物油、废弃的餐饮油(地沟油)和动植物脂肪等原料中的脂肪酸甘油三酯,与低链醇(主要是甲醇及乙醇)通过酯交换反应制取以脂肪酸甲酯和脂肪酸乙酯为主要成分的绿色燃料[1]。具有十六烷值高、无毒、可降解、无芳烃等特点,可直接替代或与化石柴油调和使用,能够改善尾气颗粒物、一氧化碳、碳氢化合物、硫化物等污染物的排放[2-3]。发展生物柴油产业可有效提高绿色清洁燃料的应用比重,是改善大气质量及生态环境的有效途径。目前生物柴油主要应用于交通燃料,以及应用于生物基材料,例如表面活性剂,生物酯增塑剂,天然脂肪醇,
摘要:生物柴油是一种可再生的清洁能源,主要原材料是植物油、废弃的餐饮油(地沟油)和动植物脂肪等,主要应用于表面活性剂、天然脂肪醇、工业溶剂、工业润滑剂、生物酯增塑剂、醇酸树脂等。比定压热容是流体的热工性能关键参数,是计算热工设备中工质焓变的基础数据,同时也是流体流动和传热计算的必要数据。采用基团贡献法研究在生物柴油中各基团随压力及温度的变化规律,提出了生物柴油主要组分脂肪酸酯类物质的比定压热容计算模型。与实验数据相比,模型计算值的最大偏差为2.7%,绝对平均偏差为0.79%,具有较高的计算精度,适用于温度333~433 K,及压力0.1~10 MPa范围内脂肪酸酯类物质的比定压热容计算。该模型的提出能够为生物柴油的推广应用提供基础热物性数据。
关键词:生物柴油,基团贡献法,比定压热容,理论计算
0引言
生物柴油是将植物油、废弃的餐饮油(地沟油)和动植物脂肪等原料中的脂肪酸甘油三酯,与低链醇(主要是甲醇及乙醇)通过酯交换反应制取以脂肪酸甲酯和脂肪酸乙酯为主要成分的绿色燃料[1]。具有十六烷值高、无毒、可降解、无芳烃等特点,可直接替代或与化石柴油调和使用,能够改善尾气颗粒物、一氧化碳、碳氢化合物、硫化物等污染物的排放[2-3]。发展生物柴油产业可有效提高绿色清洁燃料的应用比重,是改善大气质量及生态环境的有效途径。目前生物柴油主要应用于交通燃料,以及应用于生物基材料,例如表面活性剂,生物酯增塑剂,天然脂肪醇,工业溶剂,工业润滑剂,醇酸树脂等。相比起传统的化工材料,生物柴油的使用能有效减少二氧化碳,二氧化硫等温室气体及污染物排放。
如今,生物柴油的生产技术已经相当完善,并且,生物柴油的在诸多方面要优于石油基柴油:
(1)生物柴油具有可再生性,可以解决如今面临的资源的短缺问题以及未来要考虑的石油资源枯竭问题;
(2)生物柴油比起石油基柴油更清洁,硫元素,氟元素含量更低,燃烧产物以二氧化碳和水为主,有毒物质排放不到石油基柴油的十分之一,对大气的污染更小;
(3)生物柴油不具有毒性,对于生产人员的伤害更小;
(4)生物柴油的闪点高于一般的柴油,在制备,运输,储存过程中危险性更低;
(5)生物柴油的氧元素含量高,十六烷值更高,燃烧性能更好;
(6)生物柴油的可降解性很好,即使出现泄露情况对于环境的污染更小;
生物柴油生产已经可以满足日常需求,但要推广生物柴油的使用则需要对其物性进行研究,其中就包括了比定压热容数据。
比定压热容是流体关键的热工性能参数,是计算热工设备中工质焓变的基础数据,同时是流体流动和传热计算的必要数据。常用于如强化传热,绝热材料设计,工质热循环等领域。脂肪酸酯甲纯质的比定压热容是生物柴油比定压热容研究的基础,因此近些年国内外关于脂肪酸甲酯比定压热容的研究较多。Bogatishcheva[4]采用DSC方法测量了碳原子数为12、13、14、16及18脂肪酸酯类的比定压热容,测量温度范围为305~400 K;Pauly[5]同样采用DSC方法测量了12种脂肪酸酯类的比定压热容;He[6-7]采用流动型量热法测量了癸酸甲酯(C11:0)、月桂酸甲酯(C13:0)、乙醇及其混合物温度为314~334 K,压力为0.1~25 MPa时的比定压热容。通过总结发现:脂肪酸甲酯比热容的测量主要集中在少数几种物质(碳原子数集中在12~18之间),仅癸酸甲酯(C11:0)、月桂酸甲酯(C13:0)等少数物质有不同压力下的比定压热容,但温度测量范围较窄。由于实验数据较少,关于脂肪酸甲酯比定压热容的理论预测基本没有进行,仅仅采用多项式对实验数据进行关联。因此,有必要开展脂肪酸甲酯比定压热容的实验测量,并基于实验数据建立理论预测模型。考虑到脂肪酸酯类物质的化学结构相似,物性相似,因此采用基团贡献法计算生物柴油比定压热容。
基团贡献法最早由Langmuir于1925年提出,原理是把各种纯质或混合物的物性看作是它们的各种基团对物性贡献值的加和,主要以功能团划分基团,每种功能团会表现出独特的物理性质,常见的化合物都可以此方法进行基团划分,然后利用热力学原理,建立各基团的贡献值与物质物性之间的关联式,形成物性估算模型。该方法广泛应用于物质熔点、沸点、临界性质、蒸发焓、逸度系数、黏度及比热等热物性的计算UNIFAC模型较为常用,可用于相平衡及黏度等性质的计算[8-10]。基团贡献法同样可用于比定压热容的理论预测[11-12],传统的基团贡献法计算比热容的一般表达式为:

式中:c为待求物质的比热容;i为第i种基团;Δci为第i种基团对比热的贡献值;ni为分子中第i种基团的数量;a为关联常数。
1973年Chueh[13]提出的模型仅能计算20℃时液体的比定压热容;1977年Benson[14]提出的模型可计算不同温度碳氢化合物的比定压热容;Gani等[15-16]根据分子的复杂程度将基团分为第一、二、三级,实现了复杂化合物性质的计算。在此基础上Kolska等[17]于2008年将基团贡献法应用于复杂化合物比热容的计算,建立了与温度相关的计算模型。
目前基团贡献法主要应用于常压下流体比定压热容的计算,本文基于脂肪酸酯类物质比定压热容实验数据,研究了各基团贡献值随压力的变化规律,从而构建与温度和压力相关的流体比定压热容计算模型。
1基团贡献法计算模型
本文使用的计算模型由Kolska[18]等提出,适用于常温常压下脂肪酸酯类物质比定压热容计算,具体表述如下。
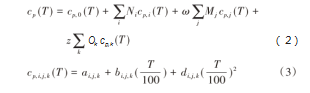
式中:cp,i(T)cp1-i(T)为一级基团i的贡献值;cp,j(T)cp2-j(T)为二级基团j的贡献值;cp,k(T)cp3-k(T)为三级基团k的贡献值;Ni、Mj和Ok分别为各级基团在化合物中出现的次数;ω和z为权重因子,取值0或1,指代二级或三级基团是否被使用;cp,0(T)为附加的可调参数(可视为0级基团);cp,i,j,k(T)为各基团关于温度的计算式;a、b、d为cp,i,j,k(T)计算式的系数。
式(2)被广泛应用于计算有机物常压下的比定压热容,但是其不能变现流体比定压热容随温度的变化规律,因此本文在原有基础上研究了各基团随压力的变化规律,提出一个新的计算模型。
本文选取了7种脂肪酸酯类物质,6条等温线(333.15 K-433.15 K)不同压力的比定压热容实验数据回归模型参数。脂肪酸甲酯和乙酯的化学式分别为CnH2n-1O2CH3及CnH2n-1O2CH2CH3,均由CH3、CH2、COOCH3及COOCH2CH3构成,其中COOCH2CH3为二级基团,其权重取1,其余为一级基团。根据化学式的不同,生物柴油的比定压热容基团贡献法计算模型可写作:
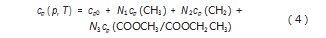
式中:cp(CH3)、cp(CH2)及cp(COOCH3/COOCH2CH3)分别为压力p,温度T时各基团的贡献值;N1、N2及N3分别为该物质中各基团的数量,其中N1和N3均为1。
压力为p0,温度为T0时,取7种物质的比定压热容实验数据代入式(4)中,则可构建方程组,该方程组有5个未知量,7个方程,采用最小二乘法可获得唯一解。
固定压力p0,改变温度,再次构建方程组,可获得该温度和压力下不同基团的贡献值;将6个温度下的基团贡献值代入式(3)回归可到该基团的系数a0,b0及d0。
改变压力为p1,计算该压力下不同温度时各基团的贡献值,再次代入式(3)可获得该压力下各基团的系数a1,b1及d1。最终,可获得不同压力时的系数a,b及d,构建各系数关于压力p的计算式如下:

将式(8)代入式(4)可获得生物柴油关于温度和压力的比定压热容基团贡献法计算模型。
2计算结果及分析
2.1实验数据
在此之前已经计算过脂肪酸酯(C6~C22)0.1 MPa下,温度范围为333~433 K之间的比定压热容数据(图1),实验值与预测值的绝对平均偏差为0.12%,最大绝对偏差为1.77%[19]。
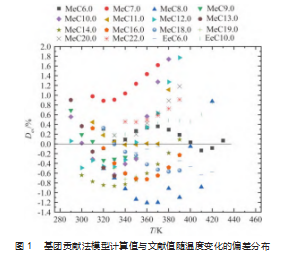
可靠的实验数据是构建计算模型的基础,本文收集了7种脂肪酸酯类物质(己酸甲酯C7H14O2,己酸乙酯C8H16O2,肉豆蔻酸甲酯C15H30O2,肉豆蔻酸乙酯C16H32O2,癸酸乙酯C12H24O2,辛酸甲酯C9H18O2,辛酸乙酯C10H20O2)的比定压热容实验数据[4,20-29],实验测量的温度范围为333~433 K,压力为0.1~10 MPa。通过比对不同研究人员发表的同类物质的实验结果,去除与偏差较大等异常数据;根据实验数据确定6条等温线(每条间隔20 K)、6条等压线(每条间隔2 MPa),采用线性插值法将将不同的实验数据处理至临近的等温线温度及等压线压力。
2.2计算结果及分析
基团贡献法改进过程中的整体计算部分借助软件MATLAB实现,鉴于脂肪酸酯类物质的分子结构,为避免出现|A|=0的奇异矩阵,决定使用Kolska模型中的cp0和cp(CH3)的贡献值,如表1所示。
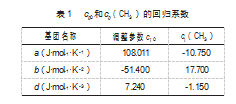
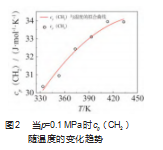
由式(4)求得各基团相同压力不同温度下的贡献值,代入式(3)进行拟合,可获得参数a、b、d。以cp(CH2)为例,p=0.1 MPa时其贡献值随温度的变化趋势如图2所示,通过拟合可获得此时a、b、d分别为-19.008,22.960,-2.547。同理,可获得各基团不同压力下的回归系数,列于表2中。
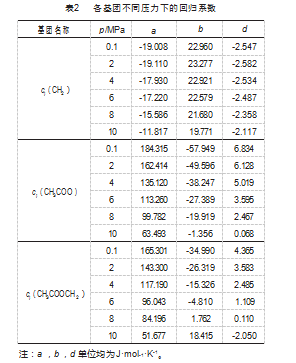
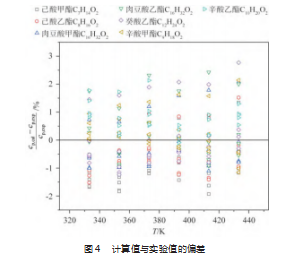
同一温度下,各基团的回归系数a、b、d均随压力p变化,以基团cp(CH3COO)的回归系数a为例分析回归系数随压力的变化趋势,如图3所示,回归可得到式(6)中的e值。同理可获得各基团式(5)~(7)的e、f、g值,列于表3中。将表3中的回归系数代入式(8)可获得各基团的贡献值,将所得的基团贡献值代入式(2)中,可获得生物柴油关于温度及压力的比定压热容基团贡献法计算模型。模型计算值与实验值相比,其最大偏差为2.7%,绝对平均偏差为0.79%,偏差分布如图4所示。由此可以看出,该模型具有较高的精度,能够满足生物柴油比定压热容的计算。
3结束语
本文基于基团贡献法,研究在脂肪酸酯类生物柴油中各基团比定压热容贡献值随温度及压力的变化规律,构建了生物柴油的比定压热容计算模型,形成以下结论:
(1)基于基团贡献法流体比定压热容计算模型,分析基团贡献值随压力的变化规律,提出了流体关于温度及压力的比定压热容基团贡献法计算模型;
(2)基于脂肪酸酯类比定压热容实验数据构建了生物柴油比定压热容关于温度及压力的基团贡献法计算模型,模型计算值与实验值的最大偏差为2.7%,绝对平均偏差为0.79%,表明模型具有较高的计算精度,可用于计算一定范围内的脂肪酸酯类物质的比定压热容,有助于生物柴油的推广应用。
参考文献:
[1]GOHAIN M,BARDHAN P,LASKAR K,et al.Rhodotorula muci‐laginosa:a source of heterogeneous catalyst for biodiesel produc‐tion from yeast single cell oil and waste cooking oil[J].Renew‐able Energy,2020,160:220-230.
[2]张雁玲,孟凡飞,王家兴,等.国内外生物柴油发展现状[J].现代化工,2019,39;396(10):15-20.
[3]BASHA S A,GOPAL K R,JEBARAJ S.A review on biodiesel production,combustion,emissions and performance[J].Renew‐able and Sustainable Energy Reviews,2009,13(6):1628-1634.
[4]BOGATISHCHEVA N S,FAIZULLIN M Z,NIKITIN E D.Heat capacities and thermal diffusivities of n-alkane acid ethyl esters—biodiesel fuel components[J].Russian Journal of Physical Chemistry A,2017,91(9):1647-1653.
[5]PAULY J,KOUAKOU A C,HABRIOUX M,et al.Heat capacity measurements of pure fatty acid methyl esters and biodiesels from 250 to 390 K[J].Fuel,2014,137:21-27.
[6]LIU X,ZHU C,SU C,et al.Isobaric molar heat capacities of bina‐ry mixtures containing methyl caprate and methyl laurateat pres‐suresup to 16.2 MPa[J].Thermochim Acta,2017,651:43-46.
[7]ZHU C,YANG F,LIU X,et al.Isobaric molar heat capacities measurement of binary mixtures containing ethyl laurate and eth‐anol at high pressures[J].Journal of Molecular Liquids,2019,280:301-306.
[8]DING H,KE W,ZHAO D,et al.Isobaric vapor-liquid equilibri‐um for binary system of methyl caprate+methyl laurate at 2,4 and 6 kPa[J].The Journal of Chemical Thermodynamics,2018,116:241-247.
[9]REZAKAZEMI M,MARJANI A,SHIRAZIAN S.Development of a group contribution method based on UNIFAC groups for the es‐timation of vapor pressures of pure hydrocarbon compounds[J].Chemical Engineering&Technology,2013,36(3):483-491.
[10]ZHAO N,JACQUEMIN J,OOZEERALLY R,et al.New meth‐od for the estimation of viscosity of pure and mixtures of ionic liquids based on the UNIFAC–VISCO model[J].Journal of Chemical&Engineering Data:the ACS Journal for Data,2016,61(6):2160-2169.
[11]NAEF R.Calculation of the isobaric heat capacities of the liq‐uid and solid phase of organic compounds at 298.15 K by means of the group-additivity method[J].Molecules,2020,25(5):1147.
[12]TRONCOSO J,SALGADO J,TEIJEIRA T,et al.Isobaric heat capacity of nanostructured liquids with potential use as lubri‐cants[J].The Journal of Chemical Thermodynamics,2018,123:107-116.
[13]CHUEH C F,SWANSON A C.Estimation of liquid heat capaci‐ty[J].Canadian Journal of Chemical Engineering,1973,51(5):596-600.
[14]LURIA M,BENSON S W.Heat capacity of liquid hydrocar‐bons.estimation of heat capacities at constant pressure as a tem‐perature function,using additivity rules[J].Journal of Chemical&Engineering Data,1977,22(1):90-100.
[15]MARREROJ,GANI R.Group contribution based estimation of pure component properties[J].Fluid Phase Equilib,2001,183(1):183-208.










