PD-1抑制剂联合安罗替尼治疗广泛期小细胞肺癌的效果研究论文
2024-06-24 13:44:33 来源: 作者:xieshijia
摘要:目的探讨广泛期小细胞肺癌(Small Cell Lung Cancer,SCLC)患者采用程序性死亡受体1(Programmed Death Receptor 1,PD-1)抑制剂联合安罗替尼的治疗效果。方法选取2021年1月—2023年12月桂林市人民医院收治的40例广泛期SCLC患者为研究对象,经随机数表法分为对照组和观察组,每组20例。对照组单纯给予PD-1抑制剂(替雷丽珠单抗)治疗,观察组在对照组基础上加用安罗替尼,比较两组客观缓解率、肿瘤标志物指标[神经元特异性烯醇化酶(Neuron-speci
[摘要]目的探讨广泛期小细胞肺癌(Small Cell Lung Cancer,SCLC)患者采用程序性死亡受体1(Programmed Death Receptor 1,PD-1)抑制剂联合安罗替尼的治疗效果。方法选取2021年1月—2023年12月桂林市人民医院收治的40例广泛期SCLC患者为研究对象,经随机数表法分为对照组和观察组,每组20例。对照组单纯给予PD-1抑制剂(替雷丽珠单抗)治疗,观察组在对照组基础上加用安罗替尼,比较两组客观缓解率、肿瘤标志物指标[神经元特异性烯醇化酶(Neuron-specific Enolase,NSE)、癌胚抗原(Carcinoembryonic Antigen,CEA)]、血清指标[内皮抑素(Endostatin,ES)、循环内皮细胞(Circulating Endothelial Cells,CEC)]、不良反应发生情况。结果治疗后,观察组的客观缓解率(75.00%)高于对照组(40.00%),差异有统计学意义(χ2=5.012,P<0.05)。观察组的NSE、CEA、CEC水平均低于对照组,ES水平高于对照组,差异有统计学意义(P均<0.05)。两组的不良反应发生率比较,差异无统计学意义(P>0.05)。结论针对广泛期SCLC患者,采取PD-1抑制剂+安罗替尼的方案治疗,效果好,能有效抑制肿瘤细胞生长,提高血清ES水平,降低CEC水平。
[关键词]小细胞肺癌;广泛期;细胞程序性死亡-配体1抑制剂;安罗替尼
Effect of PD-1 Inhibitor Combined with Anlotinib in the Treatment of Ex⁃tensive Stage Small Cell Lung Cancer
LILiying,YANG Fang
Department of Respiratory and Critical Care Medicine,Guilin People's Hospital,Guilin,Guangxi Zhuang Autonomous Region,541002 China
[Abstract]Objective To explore the effect of programmed death receptor 1(PD-1)inhibitors and anlotinib in pa‐tients with extensive small cell lung cancer(SCLC).Methods A total of 40 patients with extensive SCLC admitted to Guilin People's Hospital from January 2021 to December 2023 were selected as study objects,and divide into the con‐trol group and the observation group by random number table method,with 20 cases in each group.The control group was treated with PD-1 inhibitor(tirizumab)alone,while the observation group was treated with anlotinib based on the control group.Comparing the objective response rates,tumor marker indicators[neuron specific enolase(NSE)and car‐cinoembryonic antigen(CEA)],serum indicators[endostatin(ES)and circulating endothelial cells(CEC)],and the inci‐dence of adverse reactions between two groups.Results After treatment,the objective remission rate of observation group(75.00%)was higher than that of control group(40.00%),and the difference was statistically significant(χ2=5.012,P<0.05).The levels of NSE,CEA and CEC in the observation group were lower than those in the control group,and the level of ES was higher than that in the control group,and the differences were statistically significance(all P<0.05).There was no significant difference in the incidence of adverse reactions between the two groups(P>0.05).Con⁃clusion For patients with extensive stage SCLC,the regimen of PD-1 inhibitor plus anlotinib is effective,which can ef‐fectively inhibit tumor cell growth,increase serum ES level,and reduce CEC level.
[Key words]Small cell lung cancer;Extensive period;Programmed cell death-ligand 1 inhibitor;Anlotinib
在全球各种恶性肿瘤中,肺癌的发病率、病死率均居于首位[1]。依据组织病理学的差异,可将肺癌划分为非小细胞肺癌(Non-small-cell Carci‐noma,NSCLC)和小细胞肺癌(Small Cell Lung Can‐cer,SCLC)。尽管SCLC在肺癌中的占比仅为15%左右,但其属于典型的神经内分泌肿瘤,侵袭性和死亡率都较NSCLC高[2]。依据受累程度可将SCLC划分为广泛期和局限期,其中最常见的是广泛期,在初诊时,约有70%的SCLC患者被明确为广泛期[3]。对于广泛期SCLC患者,临床多将化疗作为其一线治疗方案,但预后差,复发率高,故亟需找寻一种有效且实用的新治疗手段。程序性死亡蛋白-1(Programmed Death Protein-1,PD-1)抑制剂是一种典型的免疫哨点单抗药物,可有效改善机体的免疫功能[4]。安罗替尼为一种新型的小分子酪氨酸激酶抑制剂,不仅能够有效抑制血管内皮生长因子受体的活性,还能有效阻止肿瘤血管的生长与扩散,进而加快肿瘤凋亡速度[5]。本研究选取桂林市人民医院在2021年1月—2023年12月收治的40例广泛期SCLC患者为研究对象,分析PD-1抑制剂+安罗替尼应用于广泛期SCLC的临床疗效,现报道如下。
1资料与方法
1.1一般资料
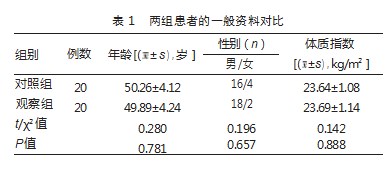
选取本院收治的40例广泛期SCLC患者作为研究对象,经随机数表法分成对照组与观察组,每组20例。两组一般资料对比,差异无统计学意义(P>0.05),具有可比性。见表1。本研究经医院医学伦理委员会批准(2020-103kY),患者对本研究均知情同意。
1.2纳入与排除标准
纳入标准:①符合疾病诊断标准[6],且经组织病理学等检查予以证实;②年龄>18岁;③临床资料完整;④疾病分型属于广泛期;⑤有较好的治疗依从性;⑥为化疗(常规依托泊苷联合卡铂或顺铂化疗)后病情进展或复发,不愿继续接受其他化疗方案,或者一、二线化疗后疾病进展,体力状况(Perfor‐mance Status,PS)评分>2分,对化疗难以耐受。排除标准:①凝血功能、血常规异常者;②对本研究所用药存在过敏情况者;③预计生存时间<3个月者;④其他脏器功能严重异常者;⑤合并其他恶性肿瘤者;⑥患有精神疾病者。
1.3方法
对照组单纯给予PD-1抑制剂,即静注200 mg替雷利珠单抗注射液(国药准字S20190045,规格:10 mL:100 mg),3周/次。观察组在对照组基础上,口服安罗替尼胶囊(国药准字H20180004,规格:12 mg×7粒),1粒/次,1次/d,口服2周后暂停1周。
3周为1个疗程,两组均持续治疗4疗程。
1.4观察指标
客观缓解率:参照相关标准[7],制订本文的疗效判定依据:患者的靶病灶已经消退,且持续时间≥4周,肿瘤标志物均恢复正常,即完全缓解(Complete Response,CR);治疗后,病灶体积较治疗前缩小≥30%,且持续4周,即部分缓解(Partial Response,PR);若病灶体积相比治疗前增大>20%,即疾病进展(Progressive Disease,PD);若在PR与PD间,即疾病稳定(Stable Disease,SD)。客观缓解率=(CR例数+PR例数)/总例数×100%。
治疗前后的肿瘤标志物指标:清晨采集5 mL空腹静脉血,3 000 r/min离心处理15 min以获得上清液,测定血清肿瘤标志物,用电化学发光法对神经元特异性烯醇化酶(Neuron-specific Enolase,NSE)、癌胚抗原(Carcinoembryonic Antigen,CEA)进行测定,所用仪器为免疫发光仪器(Uni Cel Dx I 800型,贝克曼库尔特)。
治疗前后的血清指标:采集5 mL空腹静脉血(操作方法同上),应用PercoⅡ密度梯度离心法测定循环内皮细胞(Circulating Endothelial Cells,CEC),用免疫发光仪(同上)检测内皮抑素(End‐ostatin,ES)。
不良反应:包括血小板减少、贫血、便秘、静脉血栓等。
1.5统计方法
用SPSS 27.0统计学软件处理数据,计数资料(客观缓解率、不良反应发生率)用例数(n)和率(%)表示,行χ2检验;计量资料(肿瘤标志物指标、血清指标)符合正态分布,用(±s)表示,行t检验。P<0.05为差异有统计学意义。
2结果
2.1两组客观缓解率比较
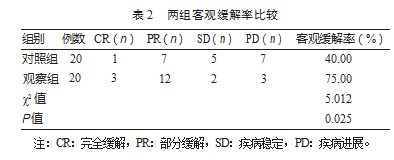
观察组的客观缓解率高于对照组,差异有统计学意义(P<0.05)。见表2。
2.2两组肿瘤标志物指标比较
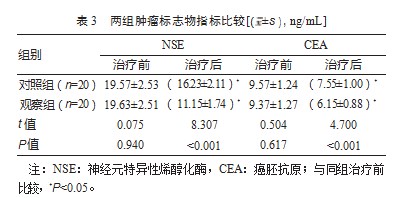
治疗前,两组NSE、CEA比较,差异无统计学意义(P均>0.05);治疗后,两组NSE、CEA均较治疗前下降,且观察组低于对照组,差异有统计学意义(P均<0.05)。见表3。
2.3两组血清指标比较
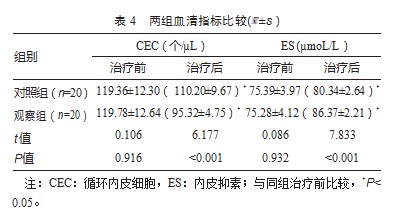
治疗前,两组CEC、ES比较,差异无统计学意义(P均>0.05);治疗后,观察组CEC水平低于对照组,ES水平高于对照组,差异有统计学意义(P均<0.05)。见表4。
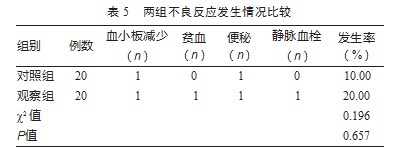
2.4两组不良反应发生情况比较
两组不良反应发生率比较,差异无统计学意义(P>0.05)。见表5。
3讨论
PD-1抑制剂属于典型的免疫哨点单抗药物,能够提升患者的抗肿瘤免疫应答能力,以间接方式杀伤肿瘤细胞。PD-1抑制剂有助于提高晚期NSCLC患者的生存率,延长其生存周期,故属一线用药[8]。细胞程序性死亡-配体1(Programmed Cell Death Protein1,PD-L1)又被称之为表面抗原分化簇274(Cluster of Differentiation 274,CD274),是机体当中的第一型跨膜蛋白,由此制成的PD-L1抑制剂,能够有效改善患者的免疫系统,抑制癌细胞扩散。广泛期小细胞肺癌首选化疗联合PD-L1抑制剂治疗,虽然有较好效果,但PD-L1抑制剂价格昂贵,限制了其临床应用。故本文选用PD-1抑制剂(替雷利珠单抗)联合安罗替尼这一方案来治疗。安罗替尼属抗血管生成药物范畴,能够同时对多靶点起作用。郑文滔等[9]以SCLC患者为对象,采用PD-1抑制剂+安罗替尼(研究组)进行治疗,且与单纯PD-1抑制剂(对照组)作对比,结果发现,研究组客观缓解率为66.27%,高于对照组的41.39%(P<0.05)。本研究的观察组客观缓解率高于对照组,与上述结论相近。提示此种联合方案可获得单用PD-1抑制剂的治疗效果。
广泛期SCLC的发病与血清肿瘤标志物水平存在直接关联,标志物水平的高低可反映病情程度[10]。NSE实为一种典型的肿瘤标志物,其具有促进肿瘤细胞因子扩散的作用,同时还能加速血管的生成。CEA属于一个广谱性肿瘤标志物,在正常机体中水平较低,但当机体被病毒、肿瘤细胞侵袭时,其水平会快速升高。文璐等[11]以SCLC患者为研究对象,观察组采用PD-1抑制剂+安罗替尼治疗,对照组给予PD-1抑制剂,观察组的NSE、CEA水平均低于对照组(P均<0.05)。在本研究中观察组的NSE(11.15±1.74)ng/mL、CEA(6.15±0.88)ng/mL低于对照组(P均>0.05),与上述结论一致。表明联合治疗方案在抑制肿瘤细胞生长方面,有着更理想的效果。
血管生成有着较复杂的病理过程,且通常会受到各种因子的调控。ES是一种血清指标,具有抑制血管生成的作用。CEC多在外周血管处分布,能够对血管内皮损伤情况实施判定。刘雨晴等[12]报道指出,观察组采用PD-1抑制剂+安罗替尼治疗后,CEC水平低于对照组,ES水平高于对照组(P均<0.05),与本文结果一致。提示PD-1抑制剂+安罗替尼能够显著降低血清CEC水平,并能使ES水平得到明显提高。由本研究结果可知,联合疗法不会增加不良反应发生率,用药安全性好。
综上所述,将PD-1抑制剂+安罗替尼用于广泛期SCLC的治疗,不仅能有效抑制肿瘤细胞的生长,还能升高血清ES水平,降低CEC水平,安全性较高。
[参考文献]
[1]李亚辉,李婷,穆林.广泛期小细胞肺癌的免疫治疗研究进展[J].2022,36(4):312-316.
[2]李姝蒙,陈芋屹,吴桐桐,等.西医一线、中医药联合西医一线治疗广泛期小细胞肺癌的研究进展[J].2023,20(30):43-46.
[3]武阳,陆翰杰,水会锋.既往免疫经治的晚期非小细胞肺癌患者接受安罗替尼联合PD-1单抗的疗效及安全性[J].2023,39(5):572-578.
[4]潘晓葶,戴安伟.安罗替尼联合PD-1单抗三线及以上治疗晚期非小细胞肺癌的疗效和安全性[J].2023,31(16):3024-3027.
[5]丁娇娇,高天慧,赵孟阳,等.安罗替尼联合多西他赛二线治疗晚期非小细胞肺癌疗效观察[J].2021,35(1):83-86.
[6]中国肺癌防治联盟,中华医学会呼吸病学分会肺癌学组,中国医师协会呼吸医师分会肺癌工作委员会.肺癌筛查与管理中国专家共识[J].国际呼吸杂志,2019,39(21):1604-1615.
[7]杨学宁,吴一龙.实体瘤治疗疗效评价标准——RECIST[J].循证医学,2004,4(2):85-90.
[8]武春秋,张允清.安罗替尼口服与多西他赛化疗和调强放疗在一线治疗失败广泛期小细胞肺癌治疗中的联合应用[J].2023,63(6):51-54.
[9]郑文滔,吴爱兵,蔡永广,等.PD-1抑制剂联合安罗替尼一线治疗老年晚期驱动基因阴性非鳞非小细胞肺癌患者的疗效及安全性分析[J].2023,22(2):127-130.
[10]王静怡,董量,付浩宇,等.安罗替尼二三线治疗的广泛期小细胞肺癌患者预后分析[J].2021,49(1):38-41.
[11]文璐,刘元明.盐酸安罗替尼治疗非小细胞肺癌的临床研究[J].2021,18(1),71-74.
[12]刘雨晴,袁淑敏,祁晓星,等.安罗替尼联合免疫检查点抑制剂治疗晚期非小细胞肺癌的疗效及安全性[J].2023,51(4):447-450.










