基于分子生物学与免疫学的大肠杆菌快速检测技术论文
2026-04-10 15:08:03 来源: 作者:xuling
摘要:深入探讨了通过级联信号放大、微流控芯片集成、人工智能辅助判读等跨学科策略,实现检测灵敏度与特异性协同提升的路径,以期突破检测多靶标联检、现场快速检测等方面的技术瓶颈。
摘要:大肠杆菌(Escherichia coli)作为全球公共卫生安全的重要威胁源,引发的感染性疾病谱系广泛,从自限性腹泻到致死性溶血性尿毒综合征,构成了显著的临床负担,是多个国际组织(如WHO、FDA、欧盟)及食品卫生标准的重要检测指标。发展实时、快速且高灵敏度的检测技术,已成为实现感染早期诊断和精准化治疗的核心需求。文章综述近年来大肠杆菌分子学和免疫学检测方法的最新进展,并讨论相关信号转导机制、生物识别元件优化及纳米材料增效策略。在此基础上,深入探讨了通过级联信号放大、微流控芯片集成、人工智能辅助判读等跨学科策略,实现检测灵敏度与特异性协同提升的路径,以期突破检测多靶标联检、现场快速检测等方面的技术瓶颈。
关键词:食源性致病菌;大肠杆菌;即时检测
大肠杆菌(E.coli)是常见的食源性病原体,主要包括肠侵袭性大肠杆菌(EIEC)、肠聚集性大肠杆菌(EAEC)、肠出血性大肠杆菌(EHEC)、肠致病性大肠杆菌(EPEC),以及产肠毒素大肠杆菌(ETEC)。食品领域,大肠杆菌污染来源多样,包括食品原料污染、加工过程污染、储存与运输污染等[1]。随着抗生素滥用,部分大肠杆菌已对抗生素产生耐药性,增加了大肠杆菌感染的治疗难度[2]。目前,多个国际组织(如WHO、FDA、欧盟)将大肠杆菌作为食品卫生标准的重要检测指标,在评估粪便污染、监控加工卫生、预测病原体风险、制订安全标准和保护消费者健康等方面具有重要意义[3]。通过科学检测及监控,可有效降低食品安全风险,保障公共健康。本文综述了大肠杆菌的传统及新兴检测技术,以期为E.coli O157:H7的快速检测提供参考。
1国家食品检测标准中大肠杆菌的检测方法及传统检测方法
生化培养鉴定法作为检测大肠杆菌的金标准,检测原理为通过检测微生物在特定培养基或试剂中的代谢反应(如酶活性、底物利用、产物生成等),区分和鉴定微生物种类。国家食品检测标准中大肠杆菌的检测方法如表1所示。其中,生物培养鉴定主要包括预增菌、选择性增菌、分离培养、生化鉴定4个步骤。该方法虽直观、准确,但费时、操作烦琐,无法满足现场及时检测的需求。

2分子生物学检测方法
2.1聚合酶链式反应(PCR)
利用PCR法实现大肠杆菌检测的国家食品相关标准为SN/T 3994-2014。PCR通过DNA聚合酶在体外特异性扩增目标DNA片段,利用引物和温度循环(变性、退火、延伸)实现DNA的指数级复制,包括常规PCR、实时荧光定量PCR(qPCR)、多重PCR等。Patcharapong等[11]开发了一种新型磁性纳米粒子PCR酶联基因测定(MELGA)和溶剂敏感纳米颗粒(SSNP)增强PCR测定技术,用于检测大肠杆菌(见图1A)。结果显示,与传统PCR相比,SSNP增强PCR检测的灵敏度提高10倍,而MELGA的灵敏度更是SSNP增强PCR检测的100倍。Sun等[12]开发了一种qPCR检测方法,用于同时识别5种主要致泻性大肠杆菌(DEC)的病理类型:产肠毒素型、肠出血型、肠致病型、肠聚集型和肠侵袭性大肠杆菌。该方法可同时检测13个DEC毒力基因,包括stp、sth、lt、stx1、stx2、eae、escV、bfpB、aggR、astA、pic、invE和ipaH。
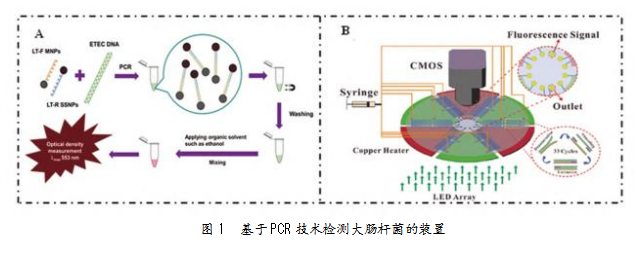
近年来,微流控PCR和数字PCR(dPCR)在检测大肠杆菌方面取得了显著进展。该类技术凭借高灵敏度、快速检测和自动化潜力,在食品安全、环境监测和临床诊断等领域展现出了广阔的应用前景。Moinet等[13]建立了一种新型微滴式dPCR平台,能同时检测和定量水样中的大肠杆菌、红叶球菌和土拨鼠球菌。此外,Yang等[14]创新性设计了一款微流控蛇形通道作为聚合酶链式反应(CF-PCR)的反应系统(见图1B)。在1 mL/h流速下,最快的PCR反应检测时间仅为5.38±0.2 min,对大肠杆菌的最低检测限度可达2.5×10-3 ng/μL。
传统PCR只能检测DNA,无法判断细菌是否存活,会出现假阳检测结果,同时需要昂贵的设备和试剂支持,在资源有限地区应用受限。未来需开发基于RNA或代谢活性的检测方法,区分活菌和死菌,并通过与其他技术结合突破固有限制。
2.2等温扩增技术(isothermal amplification technology,IAT)
利用IAT实现大肠杆菌检测的国家食品相关标准包括SN/T 3567.3-2015和SN/T 2754.2-2011。IAT通过特定的酶和引物设计,在恒定温度(60~65℃)下实现核酸的高效扩增。IAT种类很多,包括环介导等温扩增(LAMP)、滚环扩增(RCA)、交叉引物扩增(CPA)、重组酶介导的等温扩增(recombinaseaid amplification,RAA)、重组酶聚合酶扩增(recombinase polymerase amplification,RPA)等。Wang等[15]开发了基于实时荧光LAMP(RT-LAMP)和以钙黄绿素为指示剂的2种视觉LAMP试剂盒,性能优异,富集3 h后检测到接种至牛奶中的2.26 CFU/mL的E.coli O157:H7。近年来,等温扩增技术与其他技术(如CRISPR、微流控、纳米材料、电化学传感器等)结合也成为研究热点,灵敏度、特异性和便捷性显著。Wang等[16]将LAMP与CRISPR/Cas12a系统创新性结合,3 h就检测到了初始污染为7.4 CFU/mL的大肠杆菌(见图2A),有效避免了假阳性结果。为进一步提升传感器性能,Li等[17]在微流控通道安装原位捕获RCA(cRCA)适配体装置(见图2B),通过优化反应时间和圆形模板的初始浓度等条件,使装置在检测大肠杆菌方面表现出了优异性能。Jiang等[18]改良使用多聚适配体修饰微流控通道,使捕获的靶细胞增加3倍,同时将cRCA和sRCA集成于一个RCA检测系统(见图2C),相较使用单个荧光探针,检测信号显著增强250倍。在实际检测中,大肠杆菌进入可存活但不可培养(VBNC)状态,无法用金标准培养方法识别。Zhou等[19]为解决该问题开发了单叠氮化丙啶(PMA)的CPA测定法,专门设计了5种引物(2a/1s、2a、3a、4s和5a)用于识别rfbE、stx1和stx2 3个靶标。结果显示,该方法可有效识别VBNC状态的大肠杆菌O157:H7,有力推动对E.coli O157:H7的检测进展。
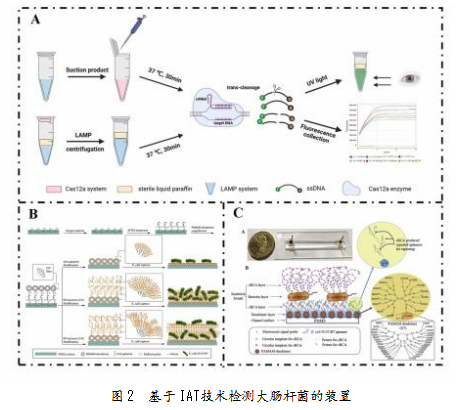
等温扩增技术虽可弥补PCR技术限制,但仍面临特异性、灵敏度、多重检测和定量能力等方面的挑战。未来,通过结合CRISPR、微流控、纳米材料、人工智能等新兴技术,等温扩增技术有望在灵敏度、特异性、便携性和应用范围上取得突破,成为现场快速检测的重要工具。
2.3 CRISPR-Cas检测技术
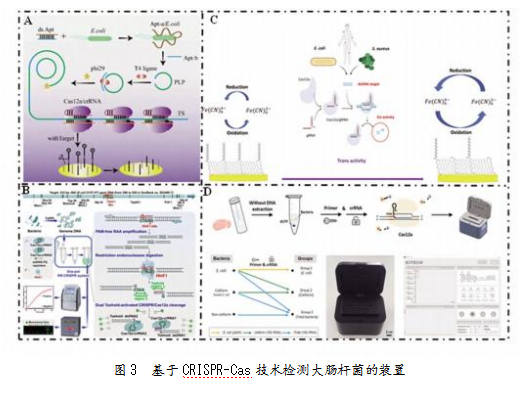
CRISPR-Cas检测技术的原理是利用Cas蛋白(如Cas12、Cas13)识别特定核酸序列后,激活其非特异性切割活性,输出荧光信号、电化学信号或比色法,实现对目标核酸的检测,其基本组成是CRISPR序列和Cas蛋白。常用的Cas蛋白包括Cas9(用于基因编辑,切割双链DNA)、Cas12(识别双链DNA后,切割单链DNA)、Cas13(识别单链RNA后,切割单链RNA)。Li等[20]将RCA与CRISPR/Cas12a结合,通过电信号变化实现大肠杆菌检测(见图3A)。
其原理为大肠杆菌与双链核酸适配体(ds Apt)特异性结合产生环状DNA,使APT与T4连接酶分离,激活RCA反应与CRISPR/Cas12a的辅助切割活性,进而切割加载到电极上的DNA序列、改变电化学信号。在最佳条件下,该方法的线性范围为1×102~1×107 CFU/mL,LOD为5.28 CFU/mL。Cas12a的PAM依赖性是其识别和切割目标DNA的关键机制,但也限制了其实际应用范围。为解决这一问题,Huang等[21]开发了一种无需PAM序列的检测方法,通过重组酶辅助扩增(RAA)联合限制性核酸内切酶介导的CRISPR/Cas12a(RR-CRISPR)技术,检测大肠杆菌O157:H7(见图3B)。该方法利用具有黏性末端的双链DNA(Toehold-dsDNA)独立于PAM序列激活CRISPR/Cas12a的反式切割活性,将检测限降至2 CFU/mL。
近年来,CRISPR/Cas12a技术与其他技术结合的策略在大肠杆菌检测方面显示出了优异性能。Andrea等[22]首次将CRISPR/Cas12a系统与电化学阻抗谱(EIS)测量结合,实现了对大肠杆菌和金黄色葡萄球菌的检测(见图3C),将LOD降至3 nM。Jiye等[23]利用增强型CRISPR/Cas系统、便携式荧光检测器共同搭建起一个检测大肠杆菌、大肠菌群和总细菌的即时护理平台(见图3D)。将ybbW基因用于大肠杆菌特异性检测,最终实现10-1个/μL(1个细胞/反应)的检测灵敏度和高特异性。
CRISPR/Cas12a技术与等温扩增技术(如LAMP、RPA等)的结合,已在分子诊断领域取得显著进展,同时与侧流层析试纸条(Lateral Flow Strip,LFS)、微流控芯片技术、电化学传感器等新技术结合的策略也在不断开发,使检测结果以荧光可视化、比色法、智能手机辅助等形式便捷显示。未来,随着新材料和新技术的引入,CRISPR/Cas12a系统的可视化检测方法将更加多样化、智能化和便携化,为即时诊断和精准医疗提供强有力的技术支持。
3免疫学检测方法
3.1侧向流动免疫层析试纸条(lateral flow immunochromatographic strip,LFIS)
LFIS的应用原理是通过毛细作用使样品在试纸条上流动,利用抗原-抗体的特异性结合在检测线处形成可见条带,实现对大肠杆菌的快速检测。基于这一原理,相关学者开展了一系列创新性研究。2016年,Song等[24]采用胶体金免疫层析条(ICS)双抗夹心法(见图4A),将检测限进一步降至4 CFU/mL。
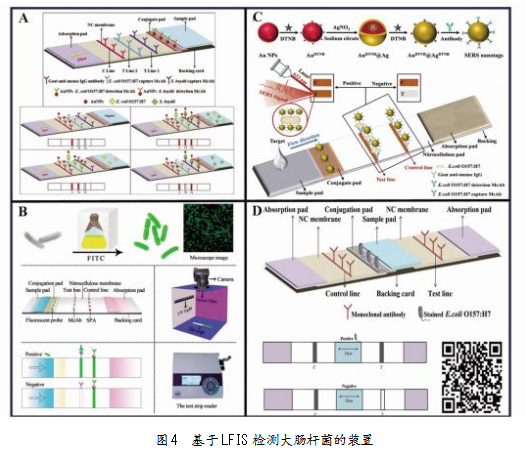
同年,发现一种“非定向活体标记”策略,即在增菌培养基中添加FITC,使致病菌在增菌1 h后自发呈现强烈荧光,形成“荧光细菌”。这一发现摒弃了传统纳米金标记抗体的需求,助力研发出了仅需一株抗体的新型“抗原有色化免疫层析试纸条”(见图4B),对E.coli O157:H7的检测灵敏度高达105~107 CFU/mL[25]。
Yan等[26]将表面增强拉曼散射(SERS)与侧向流动分析(SERS-LFA)结合(见图4C),实现了10 CFU/mL的超低检测限,为即时检测(POCT)提供了新思路。此外,Liu等[27]首次发现紫胶染料对细菌的染色能力,并据此开发出一种双向流动免疫分析条(BLFIS)(见图4D),用于检测E.coli O157:H7。刘坤等[28]引入聚集诱导发光(AIE)材料作为探针,利用其在细菌表面或内部聚集产生强荧光信号的特性,显著提升检测灵敏度,较传统胶体金试纸条提高10倍。在此基础上,设计出一种新型靶标有色化免疫层析试纸条,采用紫胶红素和十二水合硫酸铝钾媒染剂,通过“先媒后染”法,实现了免疫层析试纸条
“可视化”。该试纸条对E.coli O157:H7和沙门氏菌的检测限均达106 CFU/mL。这些研究不仅推动了LFIS技术的发展,也为食品安全和临床诊断提供了高效、灵敏的检测工具。
LFIS因快速、简便和低成本特性,在POCT检测中具有重要地位。未来,引入新型标记(如量子点、荧光纳米颗粒)替代传统胶体金,结合信号放大技术(如纳米酶、链式反应),集成智能手机或专用仪器进行定量分析,有望在灵敏度、定量能力、多目标检测和智能化等方面实现进一步提升,扩大技术应用范围。
3.2微流控芯片技术
微流控芯片检测细菌的核心原理是利用微米尺度上的特异性识别元件(如抗体、适配体)捕获目标细菌,通过电流或荧光等信号变化实现检测。微流控技术与拉曼光谱、化学发光、生物发光等先进方法结合,可充分发挥其高效、集成化优势,显著提升细菌检测的准确性、灵敏度和效率。Jayan等[29]设计了Y形分叉蛇形微流控通道(见图5A),通过原位合成银
图4基于LFIS检测大肠杆菌的装置
纳米粒子(AgNPs)增强表面增强拉曼光谱(SERS)信号强度,实现了优于其他传感器的低灵敏度,检测限为1.1 CFU/mL。为解决SERS重复性差的问题,Wang等[30]再在785 nm激发下,将NaYF4:Yb、Er SiO2 Au上转换微晶体复合材料(UC Au/Ag)嵌入了微流控芯片的基板(见图5B)。该传感器在检测大肠杆菌方面重复性优异。Sun等[31]开发了上游蛇形混合通道和下游船形微腔,以及微柱阵列组成的微流控装置(见图5C),通过催化发夹组装(CHA)和HRP-Au NPs催化化学发光实现了信号放大,仅需10μL样品就可在1.5 h完成检测工作。Zhu等[32]将噬菌体的功能化磁珠植入微流控装置中充当捕获探针,同时适配体连接共价有机框架(COF)材料作为检测探针,构建了“三明治”电化学和视觉荧光双信号传感器(见图5D)。该方法对大肠杆菌的检测范围为10~107 CFU/mL,检测限为4 CFU/mL。除上述高效策略,还存在其他一系列优异的方案。Quan等[33]创新性运用数字微流控技术,开发出一种基于时间序列图像分析的深度学习模型——TLENTNet(EfficientNet-Transformer网络)。该模型通过捕捉细菌生长过程中的时空特征,实现了对微流控芯片中大肠杆菌数量的精确计数(见图5E)。这一开创性工作标志着TLENTNet模型在细菌检测领域的首次成功应用。Rodoplu等[34]利用抗体结合的磁性颗粒捕获目标细菌,结合亚甲蓝存活试剂培养,通过微流控装置(μ瞳孔)实现视觉成像和比色信号监测(见图5F)。检测限(LOD)为2 CFU/100 mL(自来水样本)。该方法适用于资源有限地区的即时检测(POCT),资源消耗低、便携性高。
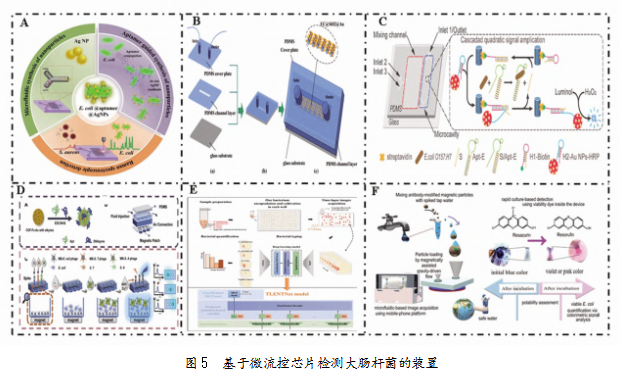
目前绝大多数微流控芯片检测法都是基于单信号或单感应电极输出实现对目标物质的检测,可能出现假阳结果。为解决这一问题,Xu等[35]等构建了一种双模式水凝胶阵列生物传感器,利用噬菌体-DNA序列特异性识别大肠杆菌,触发RCA反应形成长链DNA骨架(phage RCA-DNA)与互补DNA(cDNA)杂交形成双链DNA片段(phage RCA-dsDNA),并借助SYBR Green染料染色发射可见绿色荧光(FL),由智能手机测定实现快速筛选。同时,基于微流控芯片电泳(MCE)信号衰减与细菌浓度成正比的原理,实现定量检测,LOD为50 CFU/mL(FL信号)和6 CFU/mL(MCE信号)。2个结果相互矫正,减少了假阳结果的产生。
微流控芯片能够将增菌、检测一体化,为便携化和快速现场检测(POCT)提供可能。但目前仍存在易堵塞、污染、成本高、信号读取限制等问题。未来希望推进高通量制造工艺(如3D打印、纳米制造)的智能化发展和跨学科融合,使微流控芯片在更多领域实现突破性应用。
3.3电化学传感器
电化学传感器通过结合生物识别元件(如抗体、适配体、酶)和信号转换器(如光学、电化学)来检测目标细菌,包括光电化学(PEC)传感器、化学发光(ECL)传感器等。Zheng等[36]基于NCDs CuO/ZnO三元异质结构建检测大肠杆菌毒素DNA的PEC传感器(见图6A)。NCDs不仅能提高电极界面的电子转移速率,还能成功敏化CuO/ZnO复合物,实现光子到电子的高转换效率。在最佳条件下,制备的DNA生物传感器显示出了1.0×10-6~7.5×10-1 nM的宽线性范围和1.81×10-7 nM的低检测限(LOD)。He等[37]等新合成一系列TPE衍生物(命名为C3、C5和C6)。其自发形成的纳米聚集体表现出了显著增强的电化学发光(ECL)强度,相较原始的4-[4-(1,2,2-三苯基乙烯基)苯基]吡啶(TPP)分子提高17.0倍。基于这一发现,成功开发出一种高灵敏度ECL传感器(见图6B),用于检测大肠杆菌。该传感器的检测范围宽达10~107 CFU/mL,LOD低至1.99 CFU/mL,展现出了优异的分析性能。
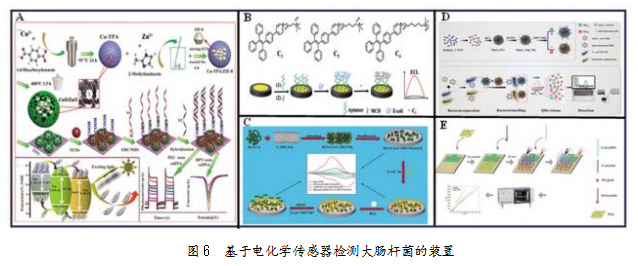
近年来,纳米材料凭借高比表面积以及优异的电学、光学和催化性能,在电化学传感器领域展现出了巨大的应用潜力。常用的纳米材料有金纳米颗粒(AuNPs)、量子点(Quantum Dots,QDs)、碳纳米管
(Carbon Nanotubes,CNTs)、金属有机框架(MOFs)等。Wang等[38]合成吲哚-5-羧酸聚合为聚-5-羧基吲哚纳米材料(PI-5-CA),引进羧基化的单壁碳纳米管(C-SWCNTs),进一步提高PI-5-CA的比表面积和电导率,通过电流信号变化实现了30 min内对E.coli O157:H7的灵敏检测(见图6C)。Nguyen等[39]首次将MoS2纳米片应用于阻抗传感器,实现了对大肠杆菌DNA的超低检测限检测(见图6D)。Li等[40]使用抗体偶联QDs MnO2纳米复合材料与免疫磁性纳米微珠(MNBs)将细菌夹心捕获(见图6E),同时谷胱甘肽将MnO2还原为Mn2+,快速释放复合物中的QDs,使其荧光强度发生改变,实现检测。该免疫测定法可在2 h内同时定量检测1.5×101~1.5×106 CFU/mL的大肠杆菌,检测限为15CFU/mL。
尽管纳米材料传感器在大肠杆菌检测中取得了显著进展,但其目前开发的材料种类仍然有限,低毒、绿色环保的纳米材料亟待进一步开发。此外,现有材料合成过程复杂且成本较高,且传感器构建步骤烦琐,限制了其大规模应用和商业化推广。电化学传感器未来应聚焦新型纳米材料的开发、抗干扰增强策略的构建、多目标检测与智能化的发展,以满足日益增长的精准检测需求。随着新材料、新技术不断涌现,生物传感器将在医疗健康、环境监测和食品安全等领域发挥更加重要的作用。
4结论与展望
当前,生化鉴定仍是大肠杆菌检测方法的金标准。同时,免疫学(如ELISA)和分子学技术(如PCR、CRISPR)也在与新技术的融合中不断发展。然而,这些方法仍存在复杂样本干扰(如食品基质抑制信号)、高成本与设备依赖(如PCR仪、荧光检测设备)、操作专业性要求高等问题,限制了其在现场快速检测中的应用。新兴技术(如纳米材料、微流控芯片)在灵敏度和特异性上表现优异,为POCT提供了可能,但仍面临合成材料复杂(如纳米酶制备)、成本高(如CRISPR试剂)、稳定性不足(如纳米材料降解)、多目标检测能力有限、环境友好性差等挑战。未来仍要依靠多技术联用(如CRISPR与纳米材料结合,实现高灵敏度检测)、便携式设备开发(如智能手机荧光检测装置)、人工智能数据分析(如机器学习优化结果判读)、绿色环保技术研发(如可降解材料)突破固有技术限制。例如,CRISPR与微流控芯片结合已达到1 CFU/mL的检测限,为POCT技术提供了重要参考。
参考文献
[1]NASEEM A,SEHYEON S,MISOOK C,et al.Point-of-Care Diagnostic Devices for Detection of Escherichia coli O157:H7 Using Microfluidic Systems:A Focused Review[J].Biosensors,2023,13(7):741.
[2]谭超,伍中宝,沈舒楚,等.氮杂环卡宾银配合物SBC3靶向大肠杆菌TDRS杀菌的作用机制[J].微生物学报,2025,65(5):2128-2143.
[3]T DAS,S DAS,B.C.A,Fabrication of a Label-Free Immunosensor Using Surface-Engineered AuPt GQD Core Shell Nanocomposite for the Selective Detection of Trace Levels of Escherichia coli from Contaminated Food Samples[J].ACS Biomaterials Science&Engineering,2024,10(6):4018-4034.
[4]中华人民共和国商务部.肉与肉制品中肠出血性大肠杆菌O157:H7检验方法:SB/T 10462-2008[S].北京:中国标准出版社,2008.
[5]全国动物检疫标准化技术委员会.动物产品中大肠菌群、粪大肠菌群和大肠杆菌的检测方法:NY/T 555-2002[S].北京:中国标准出版社,2002.
[6]进出口食品中大肠菌群、粪大肠菌群和大肠杆菌检测方法:SN/T 0169-2010[S].2010.
[7]进出口肉、肉制品及其他食品中肠出血性大肠杆菌O157:H7检测方法:SN/T 0973-2010[S].2010.
[8]交叉引物恒温扩增检测方法第3部分:大肠杆菌O157:H7.
[9]出口食品中致病菌环介导恒温扩增(LAMP)检测方法.第2部分:大肠杆菌O157:SN/T 2754.2-2011[S].2011.
[10]SN/T 3994-2014动物产品中肠出血性大肠杆菌O104:H4检疫技术规范[S].
[11]PATCHARAPONG T,YODSATHORN W,TIENRAT T,et al.Solvent-sensitive nanoparticle-enhanced PCR assay for the detection of enterotoxigenic Escherichia coli[J].Scientific Reports,2022,12(1):20677.
[12]SUN J,SHI Y,DU Y,et al.Rapid Detection of Diarrheagenic Escherichia coli by a New Multiplex Real-Time Quantitative PCR Assay[J].Applied Biochemistry and Microbiology,2020,56(6):748-757.
[13]MOINET M,COLLIS M R,ROGERS L,et al.Development of a multiplex droplet digital PCR assay for simultaneous detection and quantification of Escherichia coli,E.marmotae,and E.Ruysiae in water samples[J].Journal of Microbiological Methods,2024,220:106909.
[14]YANG B,WANG P,LI Z Q,et al.Simultaneous amplification of DNA in a multiplex circular array shaped continuous flow PCR microfluidic chip for on-site detection of bacterial[J].Lab on A Chip,2023,23(11):2633-2639.
[15]WANG Z W,CUI X P,HU A T,et al.Establishment of real-time fluorescence and visual LAMP for rapid detection ofEscherichia coli O157:H7and kits construction[J].Letters in Applied Microbiology,2023,76(11):OVAD122.
[16]WANG Z,CHEN H,HU A,et al.Establishment of LAMP-CRISPR/Cas12a for rapid detection of Escherichia coli O157:H7 and one-pot detection[J].Food Microbiology,2024,124:104622.
[17]LI S Y,JIANG Y Q,YANG X Y,et al.In situ rolling circle amplification surface modifications to improve E.coli O157:H7 capturing performances for rapid and sensitive microfluidic detection applications[J].Analytica Chimica Acta,2021,1150:338229.
[18]JIANG Y,QIU Z,LE T,et al.Developing a dual-RCA microfluidic platform for sensitive E.coli O157:H7 whole-cell detections[J].Analytica Chimica Acta,2020,1127:79-88.
[19]ZHOU W Q,WANG K,HONG W,et al.Development and application of a simple"easy to operate"propidium monoazide-crossing priming amplification on detection of viable and viable but non-culturable cells of O157 Escherichia coli[J].Frontiers in Microbiology,2020,11:569105.
[20]LI C,LIANG Y,FENG Q.An electrochemical biosensor utilizing CRISPR/Cas12a amplification for the detection of E.coli[J].The Analyst,2025.
[21]HUANG M,ZHU Y,BING X,et al.Restriction endonuclease-mediated PAM-free CRISPR/Cas12a strategy for one-pot sensitive detection of Escherichia coli O157:H7[J].Chemical Engineering Journal,2025,506:160330.
[22]ANDREA B,NOEMI P,FEDERICO V,et al.A label-free impedance biosensing assay based on CRISPR/Cas12a collateral activity for bacterial DNA detection[J].Journal of Pharmaceutical and Biomedical Analysis,2021,204(prepublish):114268.
[23]JIYE S,TAEHWI Y,JUNGHUN P,et al.Sensitive and simultaneous detection of hygiene indicator bacteria using an enhanced CRISPR/Cas system in combination with a portable fluorescence detector[J].Sensors and Actuators:B.Chemical,2022,365:131871.
[24]SONG C,LIU C,WU S,et al.Development of a lateral flow colloidal gold immunoassay strip for the simultaneous detection of Shigella boydii and Escherichia coli O157:H7 in bread,milk and jelly samples[J].Food Control,2016,59:345-351.
[25]SONG C,LIU J,LI J,et al.Dual FITC lateral flow immunoassay for sensitive detection of Escherichia coli O157:H7in food samples[J].Biosensors and Bioelectronics,2016,85:734-739.
[26]YAN S S,LI C,FANG S Q,et al.SERS-based lateral flow assay combined with machine learning for highly sensitive quantitative analysis of Escherichia coli O157:H7[J].Analytical and Bioanalytical Chemistry,2020,412(28):1-10.
[27]LIU C,FANG S Q,TIAN Y C,et al.Rapid detection of Escherichia coli O157:H7 in milk,bread,and jelly by lac dye coloration based bidirectional lateral flow immunoassay strip[J].Journal of Food Safety,2020,41(1):12862.
[28]刘坤,王英林,黄志强,等.基于紫胶红素的靶标有色化免疫层析试纸条联检大肠杆菌O157:H7和沙门氏菌[J].工业微生物,2024,54(3):104-110.
[29]JAYAN H,ZHOU R,ZHENG Y,et al.Microfluidic-SERS platform with in-situ nanoparticle synthesis for rapid E.colidetection in food[J].Food Chemistry,2025,471:142800.
[30]WANG C,MU X,HUO J,et al.Highly-efficient SERS detection for E.coli using a microfluidic chip with integrated NaYF4:Yb,Er SiO2 Au under near-infrared laser excitation[J].Microsystem Technologies,2020,(prepublish):1-7.
[31]SUN D L,FAN T T,LIU F,et al.A microfluidic chemiluminescence biosensor based on multiple signal amplification for rapid and sensitive detection of E.coli O157:H7[J].Biosensors&Bioelectronics,2022,212:114390.
[32]ZHU S,WANG S,WANG Y,et al.Microfluidic dual-mode detection system for multiple foodborne pathogens using phage-aptamer-DNAzyme composite encoded probes[J].Microchemical Journal,2025,208:112471.
[33]QUAN H,WANG S Y,XI X G,et al.Deep learning enhanced multiplex detection of viable foodborne pathogens in digital microfluidic chip[J].Biosensors&Bioelectronics,2023,245115837.
[34]RODOPLU D,CHANG C S,KAO C Y,et al.A micro-pupil device for point-of-care testing of viable Escherichia coli in tap water[J].Microchemical Journal:Devoted to the Application of Microtechniques in all Branches of Science,2022,178:107390.
[35]XU J,YU J L,LIU W Y,et al.A universal dual-mode hydrogel array based on phage-DNA probe for simultaneous rapid screening and precisely quantitative detection of Escherichia coli O157:H7 in foods by the fluorescent/microfluidic chip electrophoresis methods[J].Analytica Chimica Acta,2024,1287:342053.
[36]ZHENG D L,YANG J Y,ZHENG Z Y,et al.Sensitive photoelectrochemical detection of colitoxin DNA based on NCDs CuO/ZnO heterostructured nanocomposites with efficient separation capacity of photo-induced carriers[J].Microchimica Acta,2022,189:166.
[37]HE L,WANG Y,ZHANG C,et al.Self-assembled tetraphenylethene-based nanoaggregates with tunable electrochemiluminescence for the ultrasensitive detection of E.coli[J].Analytical Chemistry,2024,96:4809-4816.
[38]WANG H,FAN Y M,YANG Q L,et al.Boosting the electrochemical performance of PI-5-CA/C-SWCNT nanohybrid for sensitive detection of E.coli O157:H7 From the Real Sample[J].Frontiers in Chemistry,2022,10:843859.
[39]NGUYEN P N T,NGUYEN H S,TRAN T M.Disposable impedance sensors based on novel hybrid MoS2 nanosheets and microparticles to detect Escherichia Coli DNA.[J].PloS One,2024,19(2):e0299272.
[40]LI X,Huang F,LI H,et al.A sensitive immunoassay for simultaneous detection of foodborne pathogens using MnO2 nanoflowers-assisted loading and release of quantum dots[J].Food Chemistry,2020,322:126719.










