供氧和谷氨酸钠对植物乳杆菌发酵的影响论文
2026-04-09 17:37:18 来源: 作者:xuling
摘要:植物乳杆菌在发酵培养基(如蛋白陈50 g/L、葡萄糖50 g/L)中厌氧培养27 h,乳酸积累至9.4 g/L、发酵液pH降至4.02。细胞14 h后停止生长,并维持在31×108 CFU/mL左右。
摘要:植物乳杆菌在发酵培养基(如蛋白陈50 g/L、葡萄糖50 g/L)中厌氧培养27 h,乳酸积累至9.4 g/L、发酵液pH降至4.02。细胞14 h后停止生长,并维持在31×108 CFU/mL左右。文章考察了谷氨酸钠在厌氧和供氧条件下对植物乳杆菌生长及代谢的影响。结果显示,厌氧条件下添加30 g/L谷氨酸钠提高了发酵中后期发酵液的pH(4.25~4.54),峰值生物量为38×108 CFU/mL,较对照(厌氧未添加组)提高22.6%;供氧条件下添加谷氨酸钠后,峰值生物量显著提高至45×108 CFU/mL,较供氧未添加谷氨酸钠组(38×108 CFU/mL)提高18.4%,且14~27 h乳酸得率系数(YP/S)和生物量得率系数(YX/S)分别提高25%和183.3%。研究表明,供氧与谷氨酸钠协同作用显著增强了植物乳杆菌的酸胁迫抗性和生长效率,为其高密度发酵提供了理论参考。
关键词:植物乳杆菌;供氧;谷氨酸钠;发酵;得率系数
植物乳杆菌(Lactobacillus plantarum)为G+细菌,菌体呈杆状,兼性厌氧,最适温度和pH分别为30~37℃和6.5左右[1],具有耐酸、耐胆盐、调节免疫、改善肠道菌群、降低胆固醇等多种益生特性[2]。植物乳杆菌因发酵能力良好[3]被广泛应用于酸奶、干酪、香肠、泡菜和发酵饮料[4]等食品发酵领域,通过将糖类转化为乳酸降低pH,抑制病原菌生长,同时赋予食品独特风味[5]。此外,植物乳杆菌代谢产生的抗菌肽、胞外多糖等产物还有利于延长食品保质期[6]。作为微生态制剂,植物乳杆菌能改善畜禽肠道健康、提高营养物质吸收效率[7],并增强畜禽免疫力[8]。在医疗保健领域,植物乳杆菌常以活菌制剂的形式辅助治疗多种疾病,如儿童腹泻、肠易激综合征[9]等。
为提高植物乳杆菌生长效率,黄秀敏等[10]优化蔗糖(30 g/L)和酵母浸膏(50 g/L)等原料的质量浓度,摇瓶发酵18 h的活菌数达7.1×109 CFU/mL。李娜等[11]通过单因素及响应面试验获得优化培养基(蔗糖43 g/L、玉米浆干粉60 g/L)、在初始pH 6.5、30℃、接种量4%的条件下静置培养24 h,活菌数达8.01×109 CFU/mL。王玉林等[12]在优化培养基(酵母浸粉FM803 45 g/L,葡萄糖135 g/L)和培养条件(恒pH 6.0、37℃)下发酵12 h,活菌数达6.2×1010 CFU/mL。熊涛等[13]应用响应面法优化培养基配方(葡萄糖54.3 g/L、蛋白胨9.8 g/L)及氨水控pH 6.5、指数流加碳氮源发酵24 h,活菌数达9.3×109 CFU/mL。陈百莹等[14]在优化培养基(葡萄糖27.1 g/L,酵母粉4.5 g/L,牛肉膏6 g/L)、初始pH 6、35℃、接种量4%和转速80 r/min条件下摇瓶培养18 h,细胞数达9.28×109 CFU/mL。
植物乳杆菌厌氧发酵产生大量乳酸,会对细胞产生酸胁迫效应,引起细胞活力下降[15]。白凤翎等[16]发现,供氧能提高乳酸乳球菌(L.lactis)发酵生长的酸胁迫抗性,提高其生长效率。植物乳杆菌在供氧培养条件下乳酸含量降低而乙酸含量提高,对细胞起到保护作用,同时表现出典型的二次生长特征[17]。乳酸菌缓解酸胁迫包括谷氨酸脱羧酶系统[18-19]、F1F0-ATP质子泵[20]和产生碱性物质中和作用[21],但通过添加谷氨酸钠提高植物乳杆菌生物量的方式未见报道。
为提高植物乳杆菌生长效率,本文考察了供氧和谷氨酸钠对植物乳杆菌生长和乳酸生成的调控作用,发现二者可显著促进细胞生长并提高乳酸生成效率。
1材料与方法
1.1菌株
植物乳杆菌分离于酸浆水,实验室保存。
1.2仪器与设备
SPX-150D型恒温生化培养箱,购自上海智城分析仪器制造有限公司;CJ-2D型无菌操作台,购自天津市泰斯特仪器有限公司;高压蒸汽灭菌锅,购自上海博讯实业有限公司医疗设备厂;S-10生物传感分析仪,购自上海惠诚生物科技有限公司;漩涡振荡器,购自艾卡生物科技有限公司;pH计,购自赛默飞世尔科技有限公司;V-1300型可见分光光度计,购自上海美析仪器有限公司。
1.3方法
1.3.1培养基配制
种子培养基(g/L):胰蛋白胨15、牛肉膏15、酵母浸粉15、葡萄糖10、乙酸钠10、磷酸氢二钾2、柠檬酸三铵2。
灭菌条件:115℃,灭菌20 min。
发酵培养基(g/L):蛋白胨50、酵母浸粉15、葡萄糖50、乙酸钠10、磷酸氢二钾3、MgSO4·7H2O1.5、MnSO4·H2O 0.05、柠檬酸三铵5。
灭菌条件:葡萄糖与培养基分开灭菌,121℃,灭菌20 min。
1.3.2植物乳杆菌培养
种子培养:植物乳杆菌从-80℃甘油管接200μL到西林瓶(5 mL MRS培养基/20 mL西林瓶)中,37℃、200 r/min培养12 h,制成种子液。
厌氧发酵:使用厌氧瓶(瓶口用橡胶塞加螺旋帽紧固),接5 mL种子液至新鲜发酵培养基(100 mL发酵培养基/250 mL厌氧瓶),37℃、200 r/min培养28 h。
供氧发酵:使用普通摇瓶(8层纱布包扎瓶口),接5 mL种子液至新鲜发酵培养基(100 mL发酵培养基/250 mL摇瓶),37℃、200 r/min培养28 h。
1.3.3得率系数计算方法

1.3.4细胞数测定
发酵液细胞数(CFU/mL)采用稀释涂布平板法[22]测定。
1.3.5葡萄糖、乳酸质量浓度检测
葡萄糖、乳酸质量浓度测定:采用生物传感仪测定,发酵样品(-20℃保存)经12 000 r/min离心5 min,适当稀释上清液,准确吸取25μL稀释液进样。
1.3.6 pH测定
采用梅特勒pH计在线测定。
1.4数据分析
每组进行3次平行试验,数据以平均值±标准差表示。采用Origin9.0作图和处理分析数据。
2结果与分析
2.1植物乳杆菌在厌氧环境下的生长发酵特征
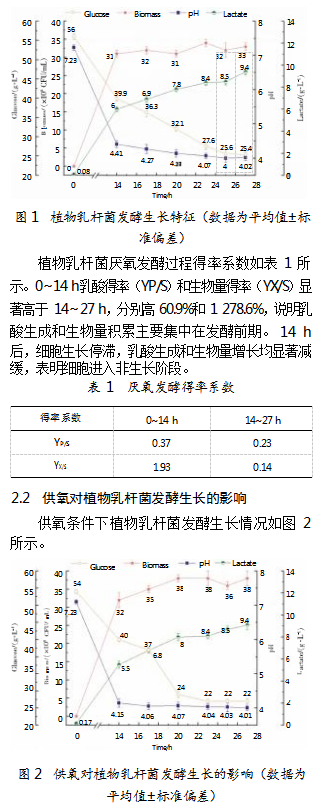
厌氧条件下植物乳杆菌发酵生长特征如图1所示。植物乳杆菌发酵呈现明显的阶段性特征:0~14 h,葡萄糖消耗迅速,糖耗速率为1.15 g/L/h,pH从7.23快速降至4.41,表明细胞代谢活跃,糖酵解代谢效率高,乳酸生成速率较快,达0.43 g/L/h,可促进细胞生长,生物量达31×108 CFU/mL;14~27 h,细胞生长进入稳定期,糖耗速率下降至1.12 g/L/h,乳酸生成速率显著降低,仅为0.26 g/L/h,较前期下降39.5%,同时pH从4.41缓慢降至4.02,说明稳定期糖酵解反应仍在进行,但产生的能量已不足以支持细胞快速生长。细胞能将能量用于维持质子泵运转以抵御低pH造成的酸胁迫。
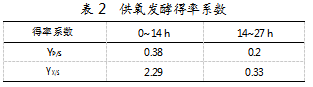
植物乳杆菌在供氧条件下,0~14 h葡萄糖消耗速率和乳酸生成率分别为1.0 g/L/h和0.38 g/L/h,pH从7.1迅速降至4.15;14~20 h葡萄糖消耗速率大幅提升至2.67 g/L/h,乳酸生成率也略有上升,达0.42 g/L/h,此时生物量显著增加,20 h达到峰值38×108 CFU/mL,此后葡萄糖消耗几乎停滞,生物量进入稳定期,pH也基本稳定在4.01;20~27 h细胞生长停止,葡萄糖消耗速率降至0.29 g/L/h,乳酸生成率降至0.16 g/L/h,表明发酵后期尽管仍有乳酸生成,但pH已接近4,酸性环境对细胞生长产生了一定的胁迫效应。供氧环境有利于植物乳杆菌生长,但并未有效缓解酸胁迫问题。
供氧条件下,0~14 h植物乳杆菌YP/S和生物量得率YX/S分别较厌氧条件提高2.7%和18.7%,表明供氧条件有利于乳酸的生成和生物量的积累;14~27 h,尽管供氧条件下的YP/S比对照(厌氧发酵)降低13.0%,但YX/S比厌氧条件提高135.7%,表明发酵后期供氧条件改善了细胞的呼吸作用,使细胞能够在乳酸生成减少的情况下仍维持一定的生长能力(见表2)。这为优化植物乳杆菌发酵工艺提供了依据。
2.3谷氨酸钠对植物乳杆菌厌氧发酵的影响
尽管供氧能显著提高生物量,但细胞在14 h后仍停止生长,说明供氧未能有效解决酸胁迫问题。为缓解低pH对植物乳杆菌生长的抑制作用,实验考察了谷氨酸钠对植物乳杆菌生长的影响,如图3所示。
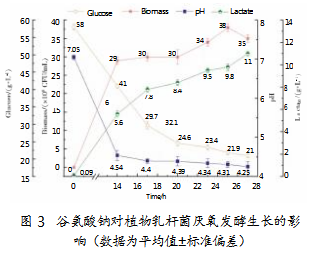
对照组14h进入稳定期(细胞数31×108 CFU/mL,见图1);实验组细胞数14 h达29×108 CFU/mL,与对照接近,但20 h出现二次生长并于25 h再次达到峰值(38×108 CFU/mL),较对照提高22.6%。相应地,0~14 h葡萄糖消耗速率1.21 g/L/h,乳酸生成速率0.39 g/L/h;14~27 h葡萄糖消耗速率1.54 g/L/h,乳酸生成速率0.42 g/L/h,分别提高27.3%和7.7%,表明谷氨酸钠不仅能促进植物乳杆菌生长,还能使其在消耗更多葡萄糖的同时产生更多乳酸。pH下降幅度更小:14 h后对照组pH维持在4.41~4.02,而实验组维持在4.54~4.25。14~27 h的YP/S与YX/S分别比对照提高17%和200%(见表3),表明谷氨酸钠显著促进了发酵后期乳酸生成和细胞生长。该现象与谷氨酸钠作为重要氮源和代谢调节剂在细胞内的作用密切相关。谷氨酸钠能激活细胞谷氨酸脱羧酶生成γ-氨基丁酸,通过消耗质子抵抗酸胁迫,且在pH 4.0~5.0时表现得尤为突出[19]。这与图3所示,14~27 h(发酵后期)pH维持在4.54~4.25,且葡萄糖消耗速率和乳酸生成速率分别较发酵前期(0~14 h)提高27.3%和7.7%的结果一致,说明谷氨酸钠不仅促进了发酵过程中植物乳杆菌的生长,还提高了其代谢效率,显著增强了细胞的酸胁迫耐受能力。
2.4谷氨酸钠对植物乳杆菌供氧发酵的影响
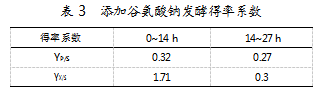
供氧和谷氨酸钠均对植物乳杆菌的乳酸生成和细胞生长具有显著影响。实验进一步考察了二者对植物乳杆菌生长代谢的协同作用(见图4)。
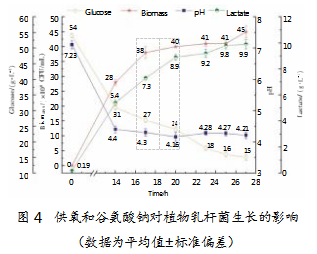
供氧条件下(对照组II),20 h达到生物量峰值(38×108 CFU/mL,见图2),添加谷氨酸钠(实验组IV)17 h达到峰值(38×108 CFU/mL),周期提前3 h。后实验组IV出现缓慢的二次生长,并于27 h再次达到峰值(45×108 CFU/mL),较对照II提高18.4%。27 h两组葡萄糖消耗量和pH基本无差异,但实验组IV的乳酸产量为9.9 g/L,较对照组II提高8.8%,表明供氧和谷氨酸钠更有利于植物乳杆菌生长代谢,显著提高了其生物量和乳酸产量。
厌氧生长添加谷氨酸钠(对照组III,见图3)14 h生物量为29×108 CFU/mL,而实验组IV(见图4)17 h生物量为38×108 CFU/mL,较对照III提高26.6%。对照组III和实验组IV均出现二次生长,但有氧条件下实验组IV生物量峰值较对照III提高18.4%,表明有氧代谢能促进植物乳杆菌生长。
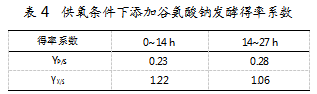
相比表2、表3,实验组IV在0~14 h的YP/S和YX/S有所降低,但14~27 h的YP/S和YX/S显著提高,较对照组II(有氧培养)分别提高25%和183.3%,较对照组III(厌氧培养添加谷氨酸钠)分别下降16.6%,提高88.8%(见表4),说明有氧和谷氨酸钠两者存在协同效应,更能有效促进植物乳杆菌生长和乳酸产量增加,并提高其耐酸性,减缓发酵过程中pH的下降速率,为植物乳杆菌发酵优化提供重要的参考依据。
3结论
本文研究了植物乳杆菌在厌氧和供氧条件下的生长与乳酸生成特性,并考察了谷氨酸钠对其生长代谢的影响。厌氧发酵并添加30 g/L谷氨酸钠虽能提高发酵中后期的pH(4.25~4.54),但细胞在14 h后仍停止生长,峰值生物量为38×108 CFU/mL,较厌氧发酵未添加谷氨酸钠组提高11.8%。供氧条件添加谷氨酸钠后,生物量显著提高至45×108 CFU/mL,较供氧未添加谷氨酸钠组提高18.4%,且14~27 h的乳酸得率系数(YP/S)和生物量得率系数(YX/S)分别提高25%和183.3%。研究表明,在厌氧和供氧条件下添加谷氨酸钠均能有效缓解低pH对植物乳杆菌生长的抑制作用,增强其酸胁迫抗性和生长效率、葡萄糖消耗量和乳酸产量,且供氧与谷氨酸钠还存在显著的协同作用。研究结果为植物乳杆菌高密度发酵提供了理论参考。
参考文献
[1]刘超楠,蔡熙姮,张新宇,等.植物乳杆菌基因组学研究进展[J].食品科技,2020,45(11):1-7.
[2]张国柱,宫俊峰,赵玉明,等.植物乳杆菌高密度发酵[J].食品工业,2022,43(10):144-147.
[3]赖长龙,曹余,杨玉,等.植物乳杆菌发酵动力学及高密度培养研究[J].食品与发酵工业,2022,48(20):137-144.
[4]李傲强,李正钰,田启全,等.植物乳植杆菌促进植物基生物活性物质释放机制及其在发酵食品中的应用研究进展[J].乳业科学与技术,2024,47(4):47-52.
[5]刘飞翔,董其惠,吴蓉,等.不同国家和地区传统发酵食品及其发酵微生物研究进展[J].食品科学,2020,41(21):338-350.
[6]兰冬雪,瞿茜楠,黄天,等.益生菌活性代谢产物的研究及应用进展[J].食品工业科技,2022,43(24):11-20.
[7]吕孝国,李佃场,李雪敏,等.植物乳杆菌P-8在家禽生产中的应用研究进展[J].中国家禽,2020,42(12):96-100.
[8]陈峰,马微微,于雷雷,等.植物乳杆菌CCFM8661增强小鼠免疫力的功能评价[J].食品与生物技术学报,2024,43(5):37-43.
[9]靳志强,王延样.植物乳杆菌在人体肠道的益生特性[J].中国乳品工业,2007(9):30-34.
[10]黄秀敏,张宜靖,李学优,等.植物乳杆菌发酵培养基的优化[J].安徽农业科学,2016,44(24):6-7,22.
[11]李娜,杨江华,韦宇拓.植物乳杆菌ZJ316高密度发酵条件优化[J].中国酿造,2021,40(5):43-48.
[12]王玉林,黄洁,崔树茂,等.植物乳杆菌最适生长底物解析及高密度培养工艺[J].食品与发酵工业,2020,46(4):19-27.
[13]熊涛,黄锦卿,宋苏华,等.植物乳杆菌发酵培养基的优化及其高密度培养技术[J].食品科学,2011,32(7):262-268.
[14]陈百莹,郑苗,邓泽元,等.植物乳杆菌ZJ316培养基优化和高密度培养的研究[J].中国食品学报,2020,20(7):65-74.
[15]武万强,王琳琳,赵建新,等.植物乳杆菌生理特性及益生功能研究进展[J].食品与发酵工业,2019,45(1):1-13.
[16]白凤翎,张柏林,蒋湘宁.乳酸菌有氧呼吸代谢研究进展[J].食品科学,2009,30(13):262-267.
[17]付龙云.乳酸菌抗氧胁迫及有氧生长的研究[D].济南:山东大学,2013.
[18]黄桂东,李超波,曹郁生,等.L-谷氨酸钠对酸胁迫下短乳杆菌NCL912蛋白表达的影响[J].食品科学,2011,32(11):181-186.
[19]GONG L,REN C,XU Y.Deciphering the crucial roles of transcriptional regulator GadR on gamma-aminobutyric acid production and acid resistance in Lactobacillus brevis[J].Microbial Cell Factories,2019,18:1-12.
[20]乌日娜,武俊瑞,孟和,等.乳酸菌酸胁迫反应机制研究进展[J].微生物学杂志,2007(2):62-66.
[21]金君华,张昊,郭慧媛,等.乳酸菌酸胁迫应答机制研究进展[J].中国乳业,2011(11):32-35.
[22]黄雪松,丁跃,宋昭,等.ccpN敲除对地衣芽孢杆菌DW2杆菌肽合成代谢的调控效应[J].食品与发酵工业,2022,48(19):23-29.










