大肠杆菌过表达cscA 基因对甜高粱汁发酵生产L- 乳酸的研究论文
2026-04-09 14:20:59 来源: 作者:xuling
摘要:甜高粱主要种植在我国西北地区,被广泛应用于酿酒工业。甜高粱茎秆压榨制得的甜高粱汁富含可溶性糖,蔗糖含量约60%,开发利用价值极高。
摘要:甜高粱主要种植在我国西北地区,被广泛应用于酿酒工业。甜高粱茎秆压榨制得的甜高粱汁富含可溶性糖,蔗糖含量约60%,开发利用价值极高。文章选取能高效转化蔗糖的大肠杆菌E-L206057作为研究对象,嵌入过表达cscA基因,进一步优化该菌株对蔗糖的利用效率,充分挖掘甜高粱的资源潜力。发酵实验结果表明,相较于未过表达cscA基因的对照菌株,工程菌E-L206057/pTrc99a-MI-93-cscA的蔗糖消耗速率显著提升19.64%,L-乳酸的平均生产强度提高15.6%。在7 L发酵罐中,以甜高粱汁为唯一碳源,菌株E-L206057/pTrc99a-MI-93-cscA完成发酵仅需14 h,最终L-乳酸产量达81.41 g/L,平均生产强度为5.82 g/L/h,相较对照菌株,提高14.34%。研究成果为利用非粮作物发酵生产L-乳酸提供了全新思路,有望为降低L-乳酸的生产成本开辟新的有效途径。
关键词:cscA过表达;甜高粱汁;L-乳酸;大肠杆菌;蔗糖
L-乳酸(L-Lactic acid)作为一种重要的有机化合物,微生物发酵为其工业生产的核心制备技术[1]。传统发酵方法主要以淀粉[2]、葡萄糖等粮食作物为发酵原料,加剧了发酵原料消耗与食物供给间的矛盾。因此,探寻利用廉价非粮生物质或农业加工副产物生产L-乳酸的有效方法,成为发酵领域的研究热点。例如,王康[3]采用无机碱CaO水溶液和NaOH水溶液对玉米秸秆进行高温预处理,利用凝结芽孢杆菌Bacillus coagulans 36D1进行批次补料发酵,最终获得67 g/L的L-乳酸;陈军晓[4]对甘薯渣进行酶解处理,使用植物乳杆菌(Lactiplantibacillus plantarum)进行发酵,发现在同等葡萄糖水平下,以水解液为碳源比以纯葡萄糖为碳源的L-乳酸产量提升31.08%;杨春柳等[5]优化酶解竹基纤维素的条件,利用凝结芽孢杆菌(Bacillus coagulans)发酵,得到6.28 g/L的L-乳酸。尽管上述研究成果为L-乳酸的低成本生产提供了有价值的参考,但其原料需要经过复杂的酸碱法及酶法预处理,无疑增加了发酵成本和工艺复杂性。
甜高粱汁作为一种极具潜力的发酵原料,由甜高粱(Sorghum bicolor)秸秆压榨而成[6]。甜高粱为一年生草本C4植物,具有突出的生物学特性:一方面,生物学产量颇为可观[7];另一方面,具有强大的抗逆能力,是我国西北盐碱地等边际土地种植作物的理想选择,彰显出了非粮属性与环境友好性。甜高粱汁作为非粮能源作物的衍生产品,完美融合可持续性与经济效益,主要成分涵盖蔗糖、葡萄糖、果糖及少量其他糖类[8]。这些可溶性糖在甜高粱汁中含量丰富,能够为L-乳酸发酵提供充足底物。与传统淀粉和木质纤维素作为发酵原料相比,甜高粱汁中的可发酵糖预处理流程相对简单,显著降低了生产成本和工艺复杂度,为L-乳酸的生产提供了更经济、高效的选择。
目前,甜高粱汁在L-乳酸发酵领域的应用已取得一定研究成果。例如,Liu等[9]运用唾液乳杆菌(Lactobacillus salivarius CGMCC 7.75),以甜高粱汁搭配昂贵氮源开展发酵实验,成功收获142.49 g/L的L-乳酸;Wang等[10]通过优化酸解甜高粱汁的蔗糖提取方式及中和剂添加策略,使L-乳酸质量浓度、收率和产酸率分别提升至102 g/L、0.942 g/g和2.9 g/L/h。然而,已有发酵工艺仍存在不容忽视的问题:第一,菌株发酵过程中需要添加酵母粉或蛋白胨等氮源,大幅增加了发酵成本;第二,部分L-乳酸生产菌株蔗糖利用效率欠佳,需先借助酸水解或酶解方法处理甜高粱汁中的蔗糖,增加生产工艺的复杂性和操作难度。
大肠杆菌(Escherichia coli)在发酵领域展现出了独特优势:培养成本低,能有效降低生产成本;生长速度极快,可在短时间内实现大量繁殖,提高生产效率;基因操作简便,便于遗传改造、优化发酵性能。大肠杆菌不仅能以硫酸铵等无机盐为氮源,而且特定株系如大肠杆菌W系具备直接代谢蔗糖的能力,无需经过烦琐的酸水解和酶解步骤,可直接利用甜高粱汁中的蔗糖、果糖及葡萄糖,为甜高粱汁发酵生产L-乳酸提供了便利。因此,利用大肠杆菌发酵甜高粱汁生产L-乳酸具有广阔的应用前景,是一种极具潜力的生产方式。
在前期研究工作中,通过实验室定向驯化技术,成功筛选出一株能高效利用蔗糖生产L-乳酸的大肠杆菌。该菌株在100 L发酵罐中利用蔗糖发酵时,产量可达97 g/L,在糖蜜和玉米浆混合液中也表现出了优异的发酵性能[11]。在此基础上,研究通过表达cscA基因强化大肠杆菌的蔗糖的利用能力,挖掘其在蔗糖代谢方面的潜力。同时,重点关注大肠杆菌在以甜高粱汁为唯一碳源的复杂环境下的代谢特性和发酵性能,深入剖析其代谢途径和调控机制,旨在为利用非粮作物降低L-乳酸的生产成本开辟新途径,推动L-乳酸发酵产业的可持续发展。
1材料与方法
1.1材料
1.1.1菌株、质粒与引物
产L-乳酸工程大肠杆菌E-L206057(E.coli W:ldhL△frdBC△adhE△pta△pflB△cscR△aldA△ldhA)、E-L206057/pTrc99a-MI-93-cscA、E-L206057/pTrc99a;质粒pTrc99a、G17043(含MI-93启动子)、pTrc99a-MI-93-cscA(MI-93-cscA),均由本实验构建保存。实验所用引物如表1所示。

1.1.2主要试剂
氨苄青霉素钠(分析纯),购自上海麦克林生化科技股份有限公司;Primer STAR DNA聚合酶、T5核酸外切酶,购自宝日医生物技术(北京)有限公司;甜高粱汁(蔗糖、果糖和葡萄糖的比例为蔗糖64.62%、葡萄糖17.79%、果糖17.60%),2024年7月采收压榨于湖南省长沙县北山镇荣合桥社区;其他试剂为国产分析纯。
1.1.3培养基
LB固体培养基:10 g/L蛋白胨,10 g/L酵母粉,5 g/L氯化钠,20 g/L琼脂粉。
LB液体培养基:10 g/L蛋白胨,10 g/L酵母粉,5 g/L氯化钠。
氨青苄霉素抗性平板:LB固体培养基,50 mg/L氨苄青霉素钠。
氨青苄霉素抗性液体培养基:LB液体培养基,50 mg/L氨苄青霉素钠。
NBS无机盐培养基:2 g/L酵母粉,3.5 g/L KH2PO4,5.0 g/L K2HPO4,3.5 g/L(NH4)2HPO4,0.25 g/L MgSO4·7H2O,15 mg/L CaCl2·2H2O,0.5 mg/L硫胺素,1 mL/L痕量盐培养基。其中,痕量盐培养基配方为:0.1 M HCl配置(1.6 g/L FeCl3,0.2 g/L CoCl2·6H2O,0.1 g/L CuCl2,0.2g/L ZnCl2·4H2O,0.2 g/L NaMoO4,0.05 g/L H3BO3);MgSO4·7H2O需用孔径0.22μm无菌滤器单独过滤灭菌,并121℃高温灭菌20 min。
NBS无机盐固体培养基:NBS无机盐培养基,20 g/L葡萄糖,20 g/L琼脂粉。
发酵罐培养基:NBS无机盐培养基,将甜高粱汁的总含糖量调至100 g/L,酵母粉2 g/L,聚醚消泡剂1 g/L。
1.2仪器与设备
Waters-e2695高效液相色谱仪,购自美国Waters公司;37070发酵罐,购自Sartorius Stedim Biotech GmbH;ZWY-2102C恒温摇床,购自上海智城分析仪器制造有限公司;DNP-9022电热恒温培养箱,购自上海精宏实验设备有限公司;SBA-40D型生物传感分析仪,购自山东省科学院生物研究所;SW-CJ-2FB超净工作台,购自苏州苏洁净化设备有限公司。
1.3实验方法
1.3.1甜高粱处理及甜高粱汁的压榨
将甜高粱清洗压榨得到的液体使用8层纱布过滤,去除大颗粒物质,加入6 mol/L NaOH溶液将pH调至6.8~7.0,6 000 r/min离心10 min,取上清测含糖量。在后续发酵过程中,通过添加适量水精确调控甜高粱汁的糖浓度。
1.3.2 pTrc99a-MI-93-cscA质粒构建
通过重叠延伸PCR连接启动子MI-93和cscA基因。以大肠杆菌E-L206057为模板,以cscA-1和cscA-2为引物,扩增cscA基因;以质粒G17043(含人工合成MI-93启动子[12])为模板,以m193-1、m193-2为引物,扩增启动子MI-93片段;以扩增的cscA基因片段和MI-93片段为模板,以mcsc-1、mcsc-2为引物,进行重叠延伸PCR获得带有启动子MI-93和cscA基因的重组片段MI-93-cscA。
pTrc99a载体线性化。以蛋白表达质粒pTrc99a为模板,以EYCDNA2-P1和EYCDNA2-P2为引物,线性化质粒pTrc99a,获得不带有Ptrc启动子的线性化质粒pTrc99a载体片段。
外切酶处理线性化载体及MI-93-cscA片段。将得到的带有MI-93启动子和cscA基因的重组片段MI-93-cscA与线性化不具有Ptrc启动子的pTrc99a载体片段进行T5外切酶处理,以CaCl2法转化至E.coli DH5α中[13]。得到的转化子以csc-yz-1和csc-yz-2为引物进行PCR验证,验证成功的转化子提取质粒测序。将测序正确的质粒命名为pTrc99a-MI-93-cscA。
将质粒pTrc99a-MI-93-cscA转入E-L206057。采用CaCl2法制备E-L206057感受态细胞,采用热激法将质粒pTrc99a-MI-93-cscA转入E-L206057感受态细胞。使用氨青苄霉素抗性平板进行筛选,将得到的阳性克隆命名为E-L206057/pTrc99a-MI-93-cscA菌株。
1.3.3摇瓶发酵验证过表达cscA基因对大肠杆菌利用蔗糖的能力的影响
分别挑取菌株E-L206057、E-L206057/pTrc99a-MI-93-cscA单菌落接种于葡萄糖含量20 g/L的NBS无机盐培养基中活化。取活化后的菌液以1%的接种量分别接种于以蔗糖、模拟甜高粱汁、甜高粱汁(总含糖量均为40 g/L)为碳源的NBS无机盐液体培养基中,以40 g/L CaCO3粉末为中和剂,37℃、200 r/min发酵24 h。每4 h取样,检测发酵液的L-乳酸、蔗糖、葡萄糖和果糖含量。
对于菌株E-L206057/pTrc99a-MI-93-cscA,培养发酵时需加入50 mg/L氨苄青霉素钠。模拟甜高粱汁中,蔗糖、果糖和葡萄糖占总糖的比例分别为64.62%、17.79%和17.60%。
1.3.4 7 L发酵罐中以甜高粱汁为唯一碳源对L-乳酸发酵的影响
在7 L发酵罐中使用甜高粱汁为唯一碳源对菌株E-L206057、E-L206057/pTrc99a-MI-93-cscA进行发酵处理。
分别挑取菌株E-L206057、E-L206057/pTrc99a-MI-93-cscA单菌落接种于葡萄糖含量20 g/L的NBS无机盐培养基中活化,37℃、200 r/min培养12 h,再按13%(V/V)的接种量,接种到以3 L甜高粱汁为唯一碳源的NBS培养基上,于7 L发酵罐中37℃、200 r/min发酵。发酵过程中流加3 mol/L的Ca(OH)2混悬液作为中和剂,控制发酵液pH为7.0。前8 h每4 h取样一次,8 h后每2 h取样一次,发酵液样品糖耗尽视为发酵结束。
对于携带质粒的菌株E-L206057/pTrc99a-MI-93-cscA,培养发酵时需加入50 mg/L氨苄青霉素钠。
1.4方法
1.4.1蔗糖水解酶活力测定
从平板上挑取菌株E-L206057和E-L206057/pTrc99a-MI-93-cscA单菌落接入50 mL LB培养基中,37℃、200 r/min培养12 h,得到种子液。以1%的接种量将种子液分别接入50 mL LB培养基中,37℃、200 r/min培养12 h,6 000 r/min离心5 min,收集菌体。参考文献[14]进行超声破胞处理获得粗酶液:加入20 mL pH 7.2的PBS缓冲液重悬并进行超声破碎,超声功率300 W,工作4 s,间隔5 s,破碎15 min。超声破胞后,10 000 r/min离心5 min,收集上清为粗酶液。粗酶液总蛋白含量以BSA为蛋白标准用Bradford法测定。
蔗糖水解酶酶活参考GB 5009.255-2016进行测定[15]。采用SBA-40D型生物传感分析仪测量酶解液中葡萄糖的质量浓度。取10 mL刻度试管,加入1.0 mol/L蔗糖溶液0.8 mL和粗酶液0.1 mL,37℃水浴保温30 min,取出后立即加入0.1 mL的1 mol/L NaOH溶液,终止酶促反应。相同条件下,沸水浴钝化酶液作为酶活空白对照。
酶活单位(U)定义为:在37℃、pH 7.0条件下,将每分钟还原1μmol葡萄糖所需酶量定义为1个单位。
1.4.2有机酸及糖含量的测定
有机酸含量测定:使用6%硫酸水溶液按体积比1:1中和发酵液,静置数分钟形成CaSO4沉淀,10 000 r/min离心10 min,取上清用孔径0.22μm水系滤膜过滤,备用;使用Waters e2695高效液相色谱仪测量发酵液的有机酸含量。
HPLC条件:色谱柱为Xtimate®Sugar-H;流动相为5 mmol/L H2SO4溶液;流速为0.5 mL/min;柱温为45℃;检测器为PDA检测器;检测波长为210 nm;进样量为10μL[16]。蔗糖、果糖测定方法与有机酸含量的测定方法一致,检测器为Waters RI检测器[17]。
葡萄糖含量测定:取适量发酵液,12 000 r/min离心5 min,取上清,用水稀释至合适倍数,使用SBA-40D型生物传感分析仪测量。
1.5数据处理与统计分析
糖酸转化率计算方法:糖酸转化率SA参考文献[18]的计算方法,如式(1)所示。

式中:ρ为物质量浓度,g/L;V为发酵液总体积,L;m为总耗糖量,g。
数据处理方法:用Excel 2010整理实验数据;使用SPSS 26进行方差分析;用Origin 2022作图。
2结果和讨论
2.1过表达cscA基因对大肠杆菌蔗糖水解酶酶活的影响
大肠杆菌主要采用2种蔗糖利用方式:一种是W系大肠杆菌自身携带的csc操纵子。该机制在大肠杆菌的蔗糖代谢过程中发挥核心作用[19]。大肠杆菌依赖cscA基因编码的蔗糖水解酶,将蔗糖催化分解为葡萄糖和果糖,纳入糖酵解途径进一步代谢和利用。另一种是在菌株内部外源引入蔗糖磷酸水解酶scrA基因。例如,Stephens等[20]表达scrA基因,使大肠杆菌E.coli K12 SURE获得蔗糖利用能力。但该途径下蔗糖需经磷酸化处理才能被大肠杆菌利用,面对复杂碳源环境可能会受碳源分解代谢物阻遏(CCR)效应限制。因此,利用基因工程手段过表达cscA基因,是增强菌株在复杂碳源环境下利用蔗糖进行L-乳酸发酵的有效选择[21]。
大肠杆菌E-L206057衍生于大肠杆菌W系,其染色体拥有cscA基因,但拷贝数较少。为强化蔗糖利用能力,实验用组成型的强启动子MI-93配合中拷贝的pTrc99A质粒骨架过表达cscA基因。
在酶活水平上比较菌株E-L206057、菌株E-L206057/pTrc99a-MI-93-cscA、菌株E-L206057/pTrc99a中cscA基因所编码的蔗糖水解酶的比酶活变化情况,如表2所示。过表达cscA基因的菌株表现出较高的蔗糖水解酶比酶活(2.82 U/mg),与作为对照的无载体质粒菌株E-L206057(0.26 U/mg)和空载体菌株E-L206057/pTrc99a(0.22 U/mg)相比,提高10倍以上。
2.2过表达cscA基因在摇瓶中对甜高粱汁发酵的影响
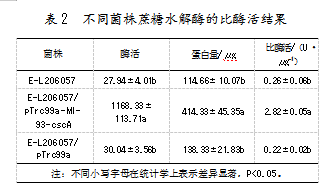
本研究以E-L206057与E-L206057/pTrc99a-MI-93-cscA为菌种,分别以40 g/L蔗糖、总含糖量40 g/L的模拟甜高粱汁、总含糖量40 g/L的甜高粱汁为唯一碳源进行L-乳酸发酵,比较过表达cscA基因对菌株利用甜高粱汁这种复杂碳源的影响。在以蔗糖为唯一碳源的发酵体系中(见图1),菌株E-L206057/pTrc99a-MI-93-cscA与菌株E-L206057的平均蔗糖消耗速率分别为2.01 g/L/h和1.68 g/L/h。过表达cscA基因的工程菌株E-L206057/pTrc99a-MI-93-cscA,相较于未改造的原始菌株E-L206057,平均蔗糖消耗速率提高19.64%,展现出优越的蔗糖代谢特性,与表2的酶活测定结果一致。在相同发酵时间(20 h)内,工程菌株E-L206057/pTrc99a-MI-93-cscA几乎完全消耗培养基中的蔗糖,而菌株E-L206057的发酵液内仍有蔗糖残留。同时,菌株E-L206057/pTrc99a-MI-93-cscA与菌株E-L206057的L-乳酸平均生产强度分别为1.60 g/L/h和1.85 g/L/h。过表达cscA后的E-L206057/pTrc99a-MI-93-cscA,相较出发菌株E-L206057,生产强度提高了15.6%。
在以模拟甜高粱汁(总含糖量40 g/L)为唯一碳源的发酵体系中(见图2),菌株E-L206057与菌株E-L206057/pTrc99a-MI-93-cscA面对复杂的碳源,表现出了类似的碳源利用顺序。发酵初期,两菌株均优先利用葡萄糖,且速率相似,分别为0.90 g/L/h和0.87 g/L/h,8 h时,葡萄糖被完全消耗,果糖、蔗糖的消耗速率逐渐增大。在2菌株利用果糖前期,果糖消耗速率相似;在发酵后期,菌株E-L206057/pTrc99a-MI-93-cscA的发酵液中出现果糖堆积现象。此外,菌株E-L206057与菌株E-L206057/pTrc99a-MI-93-cscA平均生产强度分别为1.76 g/L/h和1.91 g/L/h,增长8.52%,表明强化cscA基因表达对于提高大肠杆菌在混合碳源环境下的L-乳酸产量具有积极作用。
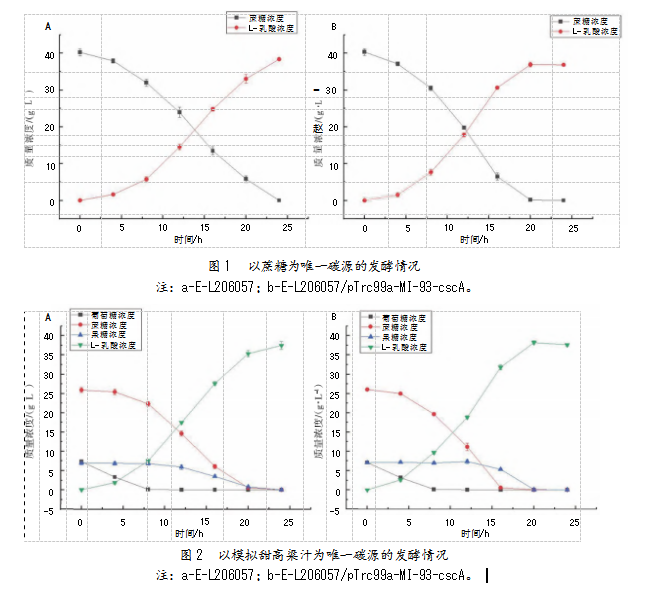
分析模拟甜高粱汁混合糖发酵发现,强化cscA基因的表达,并不改变大肠杆菌对不同碳源的优先利用顺序,即葡萄糖的优先地位仍保持不变[22]。这可能与csc蔗糖转运系统是一种非PTS(磷酸转移酶系统)有关——非PTS系统不受碳源分解代谢物阻遏(CCR)效应限制[23],也难以对其他糖的利用产生影响。另外,过表达cscA基因后的菌株E-L206057/pTrc99a-MI-93-cscA,相比菌株E-L206057,含有更多蔗糖水解酶,蔗糖消耗速率更快,但并不能保证果糖被快速利用。虽然蔗糖被迅速分解为大量葡萄糖和果糖,但胞内果糖磷酸酶的转化速率不足以匹配果糖的生成速度,致使果糖在细胞内积累[24],整个发酵过程中果糖利用较为平缓。菌株E-L206057/pTrc99a-MI-93-cscA的果糖消耗速率低于菌株E-L206057。
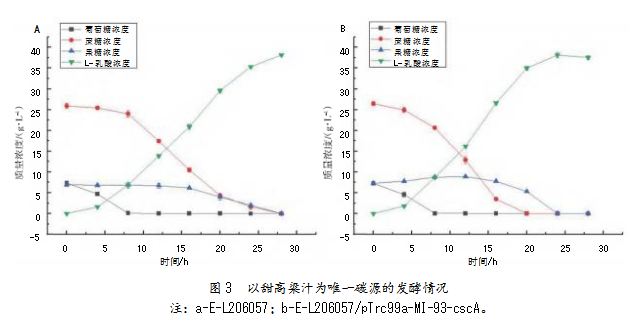
在以甜高粱汁为唯一碳源的发酵过程中(见图3),碳源的利用顺序与以模拟甜高粱汁为唯一碳源的发酵情况相似。菌株E-L206057/pTrc99a-MI-93-cscA和菌株E-L206057对葡萄糖、蔗糖和果糖的利用次序保持一致。但相较于以模拟甜高粱汁为唯一碳源发酵,以甜高粱汁为唯一碳源发酵的总时长有所增加。进一步分析发现,在以甜高粱汁为唯一碳源的发酵中,2株菌发酵的L-乳酸平均生产强度和最大生产强度分别1.36、2.17 g/L/h和1.59、2.63 g/L/h,低于以模拟甜高粱汁为碳源的发酵。
这是因为压榨出的甜高粱汁虽经处理,但仍是一种成分复杂的发酵原料,不仅含有可溶性碳源(如葡萄糖、蔗糖和果糖),还包含果胶、蛋白质、氨基酸、矿物质元素及纤维素等多种不溶性固形物[25]。这些额外成分可能对菌体生长和相关蛋白合成产生抑制作用,影响菌体对碳源的利用效率,延长发酵时间并降低生产强度[26]。
2.3 7 L发酵罐发酵时cscA基因表达对甜高粱汁发酵的影响
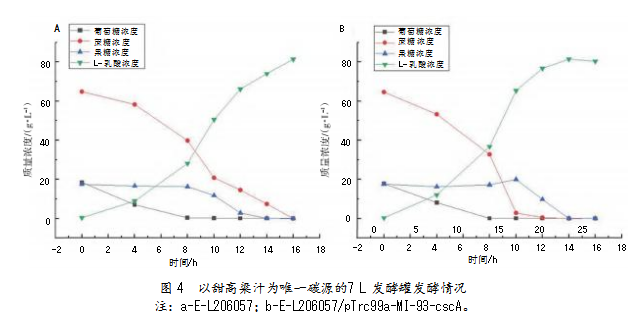
将菌株E-L206057及菌株E-L206057/pTrc99a-MI-93-cscA作为菌种,在7 L发酵罐中以甜高粱汁为唯一碳源进行发酵(见图4)。相较于摇瓶发酵,使用7 L发酵罐的L-乳酸发酵在碳源代谢速度上差异更显著。与对照菌株E-L206057底物的最大消耗速率11.83 g/L/h相比,工程菌株E-L206057/pTrc99a-MI-93-cscA底物的最大消耗速率提升15.05%,达13.61 g/L/h,加快了甜高粱汁中碳源的消耗速度,缩短了发酵周期。菌株E-L206057和菌株E-L206057/pTrc99a-MI-93-csc的L-乳酸产量分别为81.39 g/L、81.41 g/L,平均生产强度分别为5.09 g/L/h和5.82 g/L/h,糖酸转化率分别为80.34%和81.08%。菌株E-L206057/pTrc99a-MI-93-cscA的平均生产强度较菌株E-L206057提升14.34%,同时因在发酵过程中使用3 mol/L的Ca(OH)2混悬液作为中和剂,增加罐内发酵液总体积,降低了糖酸转化率。
相较摇瓶发酵,发酵罐中L-乳酸较高的生产强度和产量可能与发酵条件有关。在发酵罐系统中,温度、pH、搅拌速率及空气流量等关键参数均可实现精确调控,使发酵环境维持在有利于大肠杆菌生长与代谢的最适区间,增加环境中的菌体密度,促进底物转化,大幅提升L-乳酸的产量和生产强度。这与其他研究者的报道结果一致[27]。
3结论
本研究选取强启动子MI-93表达蔗糖水解酶cscA基因并得出以下结论。
过表达cscA基因的菌株E-L206057/pTrc99a-MI-93-cscA表现出较高的蔗糖水解酶比酶活(2.82 U/mg),与作为对照的无载体质粒菌株E-L206057(0.26 U/mg)和空载体菌株E-L206057/pTrc99a(0.22 U/mg)相比,提高10倍以上。
过表达cscA基因的工程菌株E-L206057/pTrc99a-MI-93-cscA,相较未改造的原始菌株E-L206057,蔗糖消耗速率提高19.64%,展现出优越的蔗糖代谢特性。
模拟甜高粱汁的混合糖发酵发现,强化cscA基因的表达并不改变大肠杆菌对不同碳源的优先利用顺序,即葡萄糖的优先地位仍保持不变。菌株E-L206057/pTrc99a-MI-93-cscA的果糖消耗速率低于菌株E-L206057。
在以甜高粱汁为唯一碳源的发酵中,碳源的利用顺序与采用模拟甜高粱汁为唯一碳源的发酵情况相似。菌株E-L206057/pTrc99a-MI-93-cscA和菌株E-L206057对发酵产L-乳酸的平均生产强度和最大生产强度分别为1.36、2.17 g/L/h和1.59、2.63 g/L/h,低于模拟甜高粱汁为碳源的发酵。
以甜高粱汁为唯一碳源,利用7 L发酵罐发酵,菌株E-L206057/pTrc99a-MI-93-cscA的L-乳酸平均生产强度较菌株E-L206057提高14.34%。
使用优化后的菌株E-L206057/pTrc99a-MI-93-cscA发酵生产L-乳酸,对比出发菌E-L206057,具有L-乳酸产量高、总生产强度提高的优势。并且使用甜高粱汁发酵生产L-乳酸,生产成本降低,为使用非粮作物大规模生产L-乳酸提供了新的可能。
参考文献
[1]唐柳映,王昌涛,曹晓蕊,等.乳酸菌发酵中L-乳酸的发酵工艺研究进展[J].中国食品,2024(2):114-117.
[2]李旺,李元晓,丁轲,等.罗伊乳杆菌优化培养及产乳酸效果研究[J].畜牧与兽医,2019,51(4):54-59.
[3]王康.木质纤维素生产L-乳酸新方法研究[D].北京:北京化工大学,2023.
[4]陈军晓.甘薯渣水解液乳酸发酵及分离的研究[D].济南:齐鲁工业大学,2024.
[5]杨春柳,管秀琼,刘春,等.利用竹基纤维素为碳源生物转化L-乳酸的潜力研究[J].食品与发酵工业,2024,50(6):177-183.
[6]田雪娇.重离子束辐照选育高产乳酸菌株及其发酵工艺技术研究[D].北京:中国科学院大学(中国科学院近代物理研究所),2022.
[7]李春宏,张培通,郭文琦,等.甜高粱青贮饲料研究与利用现状及展望[J].江苏农业科学,2014,42(3):150-152.
[8]周振祥,赵博,王唯先,等.不同前处理对测定甜高粱茎秆汁液3种糖含量的影响[J].草业科学,2022,39(5):940-948.
[9]LIU Q L,WANG S L,ZHI J F,et al.Efficient production of lactic acid from sweet sorghum juice by a newly isolated Lactobacillus salivarius CGMCC 7.75[J].Indian Journal of Microbiology,2013,53(3):332-336.
[10]WANG Y,TASHIRO Y,SONOMOTO K.Fermentative production of lactic acid from renewable materials:Recent achievements,prospects,and limits[J].Journal of Bioscience and Bioengineering,2015,119(1):10-18.
[11]WANG Y Z,LI K P,HUANG F,et al.Engineering and adaptive evolution of Escherichia coli W for l-lactic acid fermentation from molasses and corn steep liquor without additional nutrients[J].Bioresource Technology,2013,148:394-400.
[12]SUN W J,CHEN Y,LI M K,et al.Integration of(S)-2,3-oxidosqualene enables E.coli to become Iron Man E.coli with improved overall tolerance[J].Biotechnology for Biofuels and Bioproducts,2023,16(1):191.
[13]YU F,LI X,WANG F,et al.TLTC,a T5 exonuclease mediated low-temperature DNA cloning method[J].Frontiers in Bioengineering and Biotechnology,2023,11:1167534.
[14]洪解放.大肠杆菌xylA和xylB基因的克隆与表达[D].天津:天津大学,2006.
[15]张桦宇.重组大肠杆菌利用蔗糖生产L-乳酸[D].天津:天津科技大学,2023.
[16]谢莹莹,张悦,刘雁鸣,等.HPLC法同时测定乳酸中L-乳酸及6种有机酸杂质的含量[J].中南药学,2022,20(10):2390-2393.
[17]唐宗馨,杨硕,段勃帆,等.基于蔗糖代谢途径分析保加利亚乳杆菌的后酸化性能[J].现代食品科技,2023,39(12):142-150.
[18]张震,熊海波,徐庆阳.大肠杆菌高密度培养发酵L-色氨酸[J].食品与发酵工业,2019,45(23):15-20.
[19]SABRI S,NIELSEN L K,VICKERS C E.Molecular control of sucrose utilization inEscherichiacoli W,an efficient sucrose-utilizing strain[J].Applied and Environmental Microbiology,2013,79(2):478-487.
[20]STEPHENS C,MARTINEZ M,LEONARDI V,et al.The Scr and Csc pathways for sucrose utilization co-exist in E.coli,but only the Scr pathway is widespread in other Enterobacteriaceae[J].Frontiers in Microbiology,2024,15:1409295.
[21]CARRUTHERS D N,SALESKI T E,SCHOLZ SA,et al.Random chromosomal integration and screening yields E.coli K-12 derivatives capable of efficient sucrose utilization[J].ACS Synthetic Biology,2020,9(12):3311-3321.
[22]张克旭.分解代谢物阻遏[J].微生物学通报,1983(4):189-191.
[23]SABRI S,NIELSEN L K,VICKERS C E.Molecular control of sucrose utilization in Escherichia coli W,an efficient sucrose-utilizing strain[J].Applied and Environmental Microbiology,2013,79(2):478-487.
[24]KIM G Y,YANG J,HAN Y H,et al.Synthetic redesign of Escherichia coli W for faster metabolism of sugarcane molasses[J].Microbial Cell Factories,2024,23(1):242.
[25]叶勒生·托合达别克,涂振东,李斌斌,等.响应面优化甜高粱汁酶解工艺分析[J].新疆农业科学,2022,59(7):1632-1641.
[26]胡嘉欢,张谷涵,付永前,等.米根霉一步发酵法高效积累L-乳酸的策略[J].过程工程学报,2017,17(2):375-381.
[27]闫凯,郑维莎,连智雄,等.一株高产酸乳酸菌的分离、鉴定及高密度发酵研究[J].广东饲料,2017,26(6):24-27.










