注射用透明质酸钠溶液体外降解研究论文
2026-04-02 17:30:12 来源: 作者:xuling
摘要:注射用透明质酸钠溶液在适宜的体外环境下由透明质酸酶降解,在9 h内可完全降解为β-D-葡糖醛酸和N-乙酰β-D-葡糖胺,24 h后将会降解为CO2和H2O。
摘要:文章研究注射用透明质酸钠溶液的体外降解趋势。采用流变仪及乌氏毛细管黏计法,测定不同时间点经透明质酸酶(每克注射用透明质酸钠溶液中含透明质酸酶150 U)降解的注射用透明质酸钠溶液的剪切黏度、特性黏数,计算各降解时间点注射用透明质酸钠溶液的透明质酸降解率,以此评价本公司注射用透明质酸钠溶液的降解性能。注射用透明质酸钠溶液在适宜的体外环境下由透明质酸酶降解,在9 h内可完全降解为β-D-葡糖醛酸和N-乙酰β-D-葡糖胺,24 h后将会降解为CO2和H2O。
关键词:注射用;透明质酸钠;体外降解;流变仪
透明质酸(hyaluronic acid,HA)是一种由β-D-葡糖醛酸和N-乙酰β-D-葡糖胺交替通过β-1,4和β-1,3糖苷键连接在一起的非硫酸化线性阴离子多糖。非交联透明质酸在机体内的酶解作用主要通过透明质酸酶完成[1]。本公司的注射用透明质酸钠溶液是一种非交联注射用透明质酸钠溶液,随着降解反应发生,注射用透明质酸钠溶液黏性降低,最终降解为CO2和H2O[2]。通过对注射用透明质酸钠溶液进行剪切黏度或平均分子量测定,可以分析注射用透明质酸钠溶液在体外适宜环境下经透明质酸酶降解的降解情况。
查阅相关文献及临床研究资料,明确注射治疗过量、发生表浅或炎性反应时的推荐剂量为1.5~150 U,对于血管栓塞这类情况,起始推荐剂量为150~200 U,如果无效,则需重复注射,总用量可达1 500 U及以上[3]。总结搜集到的相关临床资料,本次试验中透明质酸酶的浓度控制在150 U/g左右。
1试验材料与方法
1.1试验材料
注射用透明质酸钠溶液(海南希睿达生物技术有限公司,230601-1)、透明质酸酶150U(SLCP2312)、0.2 mol/L氯化钠溶液。
1.2试验方法
1.2.1降解性能(剪切黏度)
流变仪参数设置:设备型号:MARS 40,转子型号:P35/Ti-01220868;ID 5:108 CSτ(应力)0.000 Pa;t<300.00 s T 25.00℃≤1.00℃;ID 6:Lift;ID 9:108 CSτ(应力)0.000 Pa;T 180.00 s T prev℃;ID 7:202(step)CRγ(应变)0.001 000 1/s-1 000.1/s log t 300.0 s#300 T prev℃;ID 11:interpolation Data:η(黏度)=f(γ),γ=1.000 1/s,(y=a+bx,d);ID 8:Lift Lift apart end of job。

流变仪测试剪切黏度:取27支注射用透明质酸钠溶液(规格:2 mL/支)内容物混匀,用流变仪设定以上参数,测定混匀后的注射用透明质酸钠溶液未经透明质酸酶降解的初始剪切黏度。称取约52 g上述已测定过初始黏度的注射用透明质酸钠溶液,加入约10 mg透明质酸酶(标识活性:791 U/mg)(注射用透明质酸钠溶液的透明质酸酶含量约为150 U/g),混匀于37℃恒温水浴降解。于设定时间取样,使用流变仪设定上述参数,测定其剪切黏度并加以记录。
时间点设置:设置0 h、0.5 h、1 h、2 h、3 h、6 h、9 h、12 h、24 h共9个时间点,得出降解趋势,以降解率达到99%以上的时间点为降解终点。
降解率计算:计算不同时间点注射用透明质酸钠溶液的剪切黏度与初始剪切黏度之比,记为该样品的降解率(剪切黏度),用式(1)计算。

1.2.2降解性能(特性黏数)
试验使用乌氏毛细管黏度计(内径0.5±0.05 mm,长140±5 mm,测定球容量3.5±0.5 mL)、秒表、磁力搅拌器、容量瓶、垂溶玻璃过滤器进行。
乌氏毛细管黏度计测试特性黏数:称取27支注射用透明质酸钠溶液(规格:2 mL/支)内容物混匀,用乌氏毛细管黏度计,测定混匀后注射用透明质酸钠溶液未经透明质酸酶降解的特性粘数。称取约52 g上述已测定过初始特性黏数的注射用透明质酸钠溶液,加入透明质酸酶(标识活性:791 U/mg)约10 mg(即每g注射用透明质酸钠溶液含透明质酸酶约150 U),混匀后于37℃恒温水浴降解。取各个降解时间点的样品,精密称定0.5 g,置于50 mL容量瓶中,加0.2 mol/L氯化钠溶液稀释至刻度,摇匀使其充分溶解,按《中国药典》2020年版四部0633黏度测定法第二法测定[4],依次测定0.2 mol/L氯化钠溶液的流出时间(T0)和供试品溶液(T)的流出时间,测定其特性黏数并记录。
时间点设置:设置0 h、0.5 h、1 h、2 h、3 h、6 h、9 h、12 h、24 h共9个时间点,得出降解趋势,以降解率达到99%以上的时间点为降解终点。
降解性能(特性黏数):计算不同时间点注射用透明质酸钠溶液的平均分子量与初始平均分子量之比,记为该样品的降解率(平均分子量),用式(2)计算。
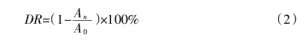
式中:DR表示降解率(平均分子量),%;A0表示初始注射用透明质酸钠溶液平均分子量;A n表示测试注射用透明质酸钠溶液平均分子量。

2试验结果
注射用透明质酸钠溶液在环境温度为37℃,透明质酸酶浓度为150 U/mL的体外降解实验中,经过0.5 h的降解,剪切黏度由10 390 mPa·s降至5 288 mPa·s,降解率达到49%;经过1 h的降解,剪切黏度由10 390 mPa·s降至3 305 mPa·s,降解率为68.20%,3 h内降解速度较快;经过3 h的降解,本产品的剪切黏度由10 390 mPa·s降至1 304 mPa·s,降解率达到87.40%。3 h~24 h降解速度减慢,降解9 h后,本品的剪切黏度降至150.5 mPa·s,降解率已达到99%,可视为本品的大分子透明质酸已被透明质酸酶完全降解。
注射用透明质酸钠溶液在37℃下,透明质酸酶浓度为150 U/mL的体外降解实验中,经过0.5 h的降解,平均分子质量由524 436.4降至503 602.0,降解率达3.97%;降解2 h内,降低速度最快,呈指数型分布,平均分子质量由524 436.4降至388 072.2,降解达26.00%,降解2~48 h基本呈线性趋势。随着时间增加,48 h后本品的平均分子质量降至698.6,降解率已达99.87%,可视为本品的大分子透明质酸已被透明质酸酶完全降解。
以上采用剪切黏度和特性黏数两种方法,对注射用透明质酸钠溶液于37℃,透明质酸酶浓度为150 U/mL的条件下,进行体外降解实验。同一时间内,剪切黏度测得的降解率高于通过特性黏数测得的降解率,但均在前3 h降解速率最快,9 h后基本降解完成,降解至24 h,两种测量方式的降解率均已超过99%。
3讨论
透明质酸是人体组织中广泛存在的一类天然多糖,透明质酸在体内的降解机制及其在体外环境下的降解行为始终是研究的焦点,本研究通过模拟体外环境,分析了注射用透明质酸钠溶液在透明质酸酶作用下的降解过程,并对其降解机制展开了深入探讨。
根据试验结果展开分析,注射用透明质酸钠溶液于适宜的体外环境下由透明质酸酶降解,在9 h内能完全降解为β-D-葡糖醛酸与N-乙酰β-D-葡糖胺。24 h后,透明质酸进一步降解为CO2和H2O。这一降解过程不但揭示了透明质酸在体外环境下的降解机制,还为了解透明质酸的体内代谢过程提供了重要的参考依据。此外,实验结果表明,透明质酸酶浓度增加、降解时间延长都显著加速了透明质酸的降解过程。温度对降解过程的影响表现出了相应的复杂性,在适宜的温度范围内,温度升高会加速降解过程,但温度过高会使透明质酸酶失活,从而抑制降解反应。
综上所述,注射用透明质酸钠溶液在透明质酸酶作用下的降解过程是一个复杂的多阶段过程,整个过程揭示了透明质酸在体外环境中的降解机制,还为透明质酸在体内的代谢过程提供了重要的参考依据。后续研究将进一步探讨透明质酸在不同环境条件下的降解行为,为其在医药与生物材料领域的应用提供更完善的理论支持。
参考文献
[1]陈筑昕,蒋承安,刘凯.透明质酸酶在透明质酸软组织填充并发症治疗中的应用[J].组织工程与重建外科杂志,2017,13(3):175-177.
[2]李佳琪,黄元礼,李妍,等.非交联透明质酸分子质量降解的机制及影响因素[J].中国组织工程研究,2024,28(5):747-752.
[3]刘兰婷,吴琳,曾戴琳,等.注射用透明质酸的应用进展[J].实用皮肤病学杂志,2020,13(6):352-355.
[4]国家药典委员会.中华人民共和国药典(四部)[M].北京:中国医药科技出版社,2020.










