盐对合成多肽螺旋结构的影响论文
2026-04-02 09:46:25 来源: 作者:xuling
摘要:合成多肽凭借其有序二级结构(α-螺旋、β-折叠)和良好的生物相容性,在生物医学与材料科学领域极具应用价值。其螺旋结构可随离子种类或浓度发生动态转变,进而影响材料性能。
摘要:合成多肽凭借其有序二级结构(α-螺旋、β-折叠)和良好的生物相容性,在生物医学与材料科学领域极具应用价值。其螺旋结构可随离子种类或浓度发生动态转变,进而影响材料性能。目前,基于温度、pH的调控策略已被深入研究,而盐通过静电屏蔽、配位等方式调控多肽螺旋结构的潜力仍待挖掘。文章系统梳理了合成多肽二级结构的调控策略,聚焦盐调控机制,总结其在组织工程、药物递送、生物传感中的应用实例。并针对离子协同机制不清、生理环境适配不足等问题,展望盐离子调控多肽功能化的设计方向,以期为合成多肽材料的结构设计与性能优化提供参考。
关键词:多肽;螺旋结构;盐效应
蛋白质功能高度依赖氢键主导的二级结构(α-螺旋、β-折叠)及其动态构象变化[1]。受天然蛋白多级结构启发,合成多肽作为具有相同肽键骨架的功能分子,兼具序列多样性与二级结构可控性,成为模拟天然蛋白功能及开发新型生物材料的理想平台,已在多种学科领域展现出应用潜力。合成多肽源于人体常见氨基酸的衍生物,其产量和分子量均易于控制,适合大规模制备。通过化学手段可对其序列进行精准设计,其能突破天然多肽的限制,赋予产物更高的稳定性、生物活性和靶向性等。
α-螺旋作为多肽最重要的二级结构之一,在自组装、生物医学性能等方面与无规结构的差异显著。本文研究多肽螺旋结构的性质、应用及盐离子对螺旋结构的影响,不仅深化了对生物大分子折叠的理解,更为生物医学材料设计提供了重要依据。
1α-螺旋结构
1.1螺旋多肽的表征
多肽的各种二级结构可通过肽键的氢键模式或多肽主链的二面角——φ角(Cα-N键的扭转角)和ψ角(Cα-C键的扭转角)来区分。圆二色光谱(CD)和傅里叶变换红外光谱(FTIR)是表征多肽二级结构最常用的技术。
CD基于手性分子对左右圆偏振光的吸收差异,通过远紫外区(180~250 nm)肽键的特征吸收峰解析结构[2],灵敏度高(微克级样品),适合实时监测水溶液中多肽的构象动态变化(如pH、温度变化),能定量估算二级结构含量,但无法区分β-转角与无规卷曲,且易受溶剂干扰。
FTIR则通过分析肽键的酰胺I带(1 600~1 700 cm-1)和酰胺Ⅱ带(1 500~1 600 cm-1)的振动特征来表征结构,适用于固态(如冻干样品)和液态样品的分析,可区分β-折叠的平行与反平行构象,且能通过差谱技术消除溶剂干扰,但需依赖专业软件拟合光谱,对低含量结构的灵敏度较低。酰胺Ⅰ和不同多肽构象的酰胺Ⅱ带的频率已被预测。α-螺旋、β-折叠和无规卷曲多肽的CD特征和FTIR特征见表1。
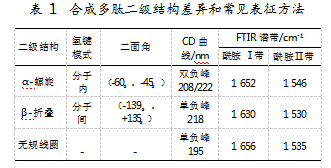
除此之外,核磁共振(NMR)、X射线晶体衍射、拉曼光谱、荧光光谱等常与CD、FTIR联用,以实现优势互补,全面解析多肽的二级结构特征。
1.2调节多肽螺旋的策略
侧链之间的疏水相互作用、氢键相互作用和电荷相互作用,稳定了α-螺旋的形成,去除或恢复这些侧链基团或氢键,已被广泛用于设计具有螺旋-无规卷曲转变特性的多肽材料。这一特性已被广泛应用于选择性药物释放、基因递送及疾病诊断等领域。
1.2.1调节侧链极性
在多肽结构调控中,侧链极性基团的偶极-偶极相互作用,会干扰多肽螺旋结构所需的氢键网络。同时,极性基团的亲水性会干扰主链肽键与水的相互作用,破坏螺旋结构的稳定性。Kramer和Deming报道了含硫醚基团的多肽在氧化环境下,其硫醚基团可被氧化为极性更强的亚砜或砜,能显著改变侧链极性与相互作用[3]。多肽构象转变受取代基、极性基团与主链距离、溶剂等因素调控。由此,研究人员设计出多种螺旋-卷曲构象转变型多肽。生物体内相关活性氧物种(ROS)可触发这种多肽构象转变,在生物医学领域极具应用前景。
1.2.2调节氢键
α-螺旋构象的稳定性依赖主链内的氢键网络。侧链二元氢键(BHB)配体可通过竞争性作用破坏螺旋结构。BHB配体兼具氢键供体与受体能力,与主链肽键发生相互作用,削弱链内氢键,干扰强度与配体距主链的距离相关。值得注意的是,基于氢键的螺旋破坏剂易受其他官能团影响,如长疏水链或羧酸基团的引入,可通过空间位阻或电子效应抵消三唑基团的破坏作用[4]。众所周知,温度变化也会影响多肽分子的氢键相互作用。温度升高,氢键被破坏,螺旋结构可能解旋转变为无规卷曲;温度降低,氢键恢复,有利于螺旋结构的形成和稳定。
1.2.3调节溶液pH
多肽的螺旋构象与侧链电荷密切相关,侧链电荷的屏蔽/暴露是调节合成多肽二级结构最常用的策略。在赖氨酸/精氨酸富集的多肽中,碱性条件下侧链氨基的去质子化降低正电荷密度,削弱静电排斥,促进螺旋形成;而酸性条件下,侧链氨基的质子化导致电荷排斥增强,诱导螺旋解离。谷氨酸/天冬氨酸富集的多肽在酸性环境中羧酸根发生质子化,减少负电荷排斥,稳定α-螺旋。pH响应多肽为选择性药物释放与基因递送等提供了新思路。聚乙二醇-聚组氨酸嵌段共聚物在肿瘤微酸性环境(pH=6.5)中发生质子化,触发无规-螺旋构象转变,可应用于实体肿瘤治疗[5]。
2盐调控多肽螺旋结构
多肽链的电荷分布是决定其构象的关键,侧链静电排斥因金属配位或盐筛选而被消除,从而可观察到α-螺旋构象的恢复。溶液中离子通过2种机制影响多肽构象:非特异性电荷屏蔽降低静电排斥;特异性离子结合改变局部电荷环境。
2.1盐离子在生物大分子结构调控中的重要性
盐离子对聚氨基酸二级结构的调控兼具科学意义与应用价值。在基础科学层面,其通过电荷屏蔽、特异性结合等方式影响α-螺旋、β-折叠等结构的形成与平衡,为解析蛋白质折叠、生物分子相变及Hofmeister效应提供了分子依据。在生物医学领域,精准调控盐离子浓度与种类可优化药物递送,辅助合成多肽设计。在材料科学领域,盐离子可作为环境响应“开关”,驱动多肽智能材料可控组装。此类研究不仅揭示了离子与生物分子的互作规律,还推动了跨学科创新,成为连接基础理论与生物技术、纳米医学的关键纽带。
2.2盐调控多肽螺旋结构策略
库仑相互作用主导蛋白质折叠与稳定性,通过调控氨基酸侧链电荷状态,可实现不同构象之间的切换。其中,离子强度和pH是关键环境参数。离子强度可通过增减盐的浓度与特性调节,决定其电荷筛选能力。多肽在不同pH及盐含量下,可呈现无规卷曲、α-螺旋和β-折叠,展现出多肽结构的多样性。此外,金属盐能与多肽主链及侧链氨基酸配体相互作用,可诱导多肽从无序到折叠,或在不同折叠状态间发生构象转变。
2.2.1金属离子配位
蛋白质中的金属离子在稳定结构、诱导构象转变等方面发挥关键作用,其对蛋白质结构的影响备受关注。研究人员借助肽模型探索金属离子功能的复制可能。如J等和Ramadan等发现,砷(Ⅲ)与半胱氨酸残基的结合位点不同,对多肽α-螺旋和β-折叠结构的稳定效果不同[6-7]。
在金属盐诱导多肽二级结构的研究中,金属离子可与多肽侧链作用,诱导无序到螺旋的构象转变。2016年,Bonduelle等筛选发现,中性pH下,Cu2+、Zn2+盐可显著诱导多肽螺旋形成,加入强配位外部配体(如NTA)可使多肽从螺旋转为卷曲[8]。后续又发现Cd2+配位能分别诱导聚谷氨酸形成α-螺旋,诱导聚羧甲基-L-半胱氨酸形成β-折叠;用EDTA等可去除配位实现结构可逆转变;同时PCMC侧链硫醚氧化可破坏Cd2+诱导的β-折叠,实现pH、金属配位和氧化还原多重响应调控[9]。
引导无规线圈向螺旋转变的另一种方式,是疏水核心内的金属离子配位。在含组氨酸多肽未折叠的pH条件下,添加Ag+可促使其形成纤维状α-螺旋聚集体。与外部结合位点不同,该肽-金属复合物的配位几何结构受疏水核心空间位阻限制显著。T等和Eleonora等分别将卷曲螺旋与锌诱导折叠元素融合,设计杂合序列,均实现了锌离子响应的构象转变[10-11]。此外,金属配位也可能破坏卷曲螺旋的稳定性[6]。
金属离子与带电多肽的配位可以中和电荷,并通过无规线团-螺旋转变进一步引发自组装。Ken-suke等报道,聚乙二醇-聚谷氨酸嵌段聚合物中,带负电的聚谷氨酸嵌段与(1,2-二氨基环己烷)铂(Ⅱ)(DACHPt)的结合,证实了聚谷氨酸嵌段的无规线圈-螺旋转变导致金属囊泡的自发形成[12]。
2.2.2反离子静电作用
反离子结合影响含有带电侧基多肽的溶液性质和构象。含磺酸根基团的多肽在水-醇体系中形成螺旋的过程具有反离子特异性。通过聚(α-甲基L-谷氨酸)与异硫氰酸酯交换反应制备含磺酸根基团的带电多肽,研究其在水-醇溶液中的构象转变,发现其螺旋形成具有显著的抗衡离子特异性,顺序为Li+<Na+<Cs+≤Rb+≤K+,与聚谷氨酸相反,符合Desnoyers规则[13]。
Steven等设计的TZ1H肽中,组氨酸残基位于核心,在纤维结构螺旋界面相邻处形成金属离子结合位点[14]。银(I)离子与组氨酸特异性结合,诱导TZ1H肽从随机卷曲转变为α-螺旋,其CD光谱随银(I)浓度变化显著。银(I)配位稳定α-螺旋,驱动多肽自组装为高纵横比纤维,并经透射电镜验证。基于此,提出合成响应性肽系统的通用设计策略,证实合理设计选择性客体结合位点是制备纳米自组装材料的有效途径。
2.2.3选择性结合与特异性调控
不同金属离子因其电子结构和配位偏好不同,对肽的构象影响具有选择性。实验表明,锌(Ⅱ)离子、铜(Ⅱ)离子和镍(Ⅱ)离子等因偏好其他配位几何构型,难以在TZ1H肽的三角平面配位位点有效结合,从而无法像银(Ⅰ)离子那样诱导肽链发生明显的构象转变和纤维组装[15],这体现了金属离子与肽结合的特异性,以及这种特异性对螺旋转变调控的重要意义。
Hoshino等设计了一个由37个氨基酸残基组成的同源二聚体卷曲线圈的肽,作为分析蛋白质中电荷排斥作用及其被溶剂屏蔽的模型[16]。这些肽在pH=4.7和20℃没有盐的情况下展开,但添加NaClO4协同稳定了α-螺旋构象,ClO4-与多肽上的正电荷结合,屏蔽了电荷排斥,使得α-螺旋结构得以稳定。在研究中,NaClO4诱导蛋白质构象转变的效果比NaCl强很多,这说明特定阴离子与蛋白质的直接结合,而非一般的离子强度效应,是引发蛋白质构象转变的关键。
3应用领域与前景展望
过去几十年,合成多肽领域在合成方法开发、二级结构调控和生物活性优化方面成果显著。合成技术的突破解决了关键难题并提升了制备效率,诱导二级结构转变推动了细胞渗透等生物应用的发展。但仍存在以下问题:开发兼具化学多样性与多功能基团的多肽存在挑战,亟须序列精确可控、可减少批次差异的合成方法;具有明确有序二级结构的合成多肽,在人工酶、免疫佐剂等新生物领域的应用有待进一步深入;现有多肽二级结构体外调控策略受限于敏感性和选择性,如磷酸酶、pH、紫外线、盐等调控方式存在局限性,需开发与生物环境兼容、可实现高选择性和高敏感控制的策略,并研究多肽二级结构可逆调控机制;α-螺旋多肽的细胞毒性问题突出,现有平衡毒性与膜活性的策略应用范围窄,需拓展至基因递送等更多领域。
参考文献
[1]HARPER E T,ROSE G D.Helix stop signals in proteins and peptides:The capping box[J].Biochemistry,1993,32(30):7605-7609.
[2]M B B,ALISON R,D J H.Circular and linear dichroism of proteins[J].Physical Chemistry Chemical Physics:PCCP,2007,9(17):2020-2035.
[3]KRAMER,JESSICA R.,DEMING,TIMOTHY J.Gly-copolypeptides with a Redox-Triggered Helix-to-Coil Transition[J].Journal of the American Chemical Society,2012,134(9):4112-4115.
[4]SONG Z,TAN Z,ZHENG X,et al.Manipulating the helix coil transition profile of synthetic polypeptides by leverag-ing side-chain molecular interactions[J].Polymer Chem-istry[J],2020,11(8):1445-1449.
[5]LEE S E,SHIN J H,NA K,et al.Poly(l-histidine)PEG block copolymer micelles and pH-induced destabilization[J].Journal of Controlled Release,2003,90(3):363-374.
[6]J.D C,COLIN T,P.J S.Effects of As(III)binding onα-helical structure[J].Journal of the American Chemical Society,2003,125(10):2923-2929.
[7]RAMADAN D,CLINE J D,BAI S,et al.Effects of As(III)binding onβ-hairpin structure[J].Journal of the Ameri-can Chemical Society,2007,129(10):2981-2988.
[8]BONDUELLE C,MAKNI F,SEVERAC L,et al.Smart metallopoly(L-glutamic acid)polymers:reversible he-lix-to-coil transition at neutral pH[J].RSC Advances,2016,6(88):84694-84697.
[9]KUROTU T.Polarographic behavior of Cd2+and Zn2+—PGA complexes.Polarographic and circular dichroism spectroscopic studies on the Cd2+and/or Zn2+—poly(α-L-glutamic acid)complex in aqueous solution[J].In-organica Chimica Acta,1992,191(1):141-147.
[10]T B F,P C M,E J P,et al.Arsenic(III)-cysteine interac-tions stabilize three-helix bundles in aqueous solution[J].Inorganic Chemistry,2000,39(24):5422-5423.
[11]ELEONORA C,K B S,N D W.ZiCo:a peptide de-signed to switch folded state upon binding zinc[J].Jour-nal of the American Chemical Society,2005,127(43):15008-15009.
[12]KENSUKE O,HORACIO C,YUKI M,et al.Bioactive polymeric metallosomes self-assembled through block copolymer-metal complexation[J].Journal of the Ameri-can Chemical Society,2012,134(32):13172-13175.
[13]ANDO A,SATOH M.Counter-ion-specific helix forma-tion of poly(#gamma#-methyl L-glutamate)derivatives containing sulfonate group in aqueous alcohols[J].Poly-mer International,2001,50(8):911-916.
[14]STEVEN D,YURI Z,P V C.Engineering responsive mechanisms to control the assembly of peptide-based nanostructures[J].Biochemical Society Transactions,2009,37(Pt 4):653-659.
[15]N S D,P V C.Design of a selective metal ion switch for self-assembly ofpeptide-based fibrils[J].Journal ofAmeri-can Chemical Society,2008,130(1),49-51.
[16]HOSHINO M,GOTO Y,YUMOTO N,et al.Design and characterization of the anion-sensitive coiled-coil peptide[J].Protein Science,1997,6(7):1396-1404.










