消毒时长及间隔对亲和层析填料(MabCapture 重组蛋白A)载量的影响研究论文
2025-04-29 14:45:32 来源: 作者:xuling
摘要:文章通过生产相同的柱高,使用缩小柱直径的方式,利用线性的缩小模型测试了碱液消毒时长及间隔对亲和层析填料(MabCapture重组蛋白A)载量的影响。
摘要:文章通过生产相同的柱高,使用缩小柱直径的方式,利用线性的缩小模型测试了碱液消毒时长及间隔对亲和层析填料(MabCapture重组蛋白A)载量的影响。结果表明,消毒25 h后载量(DBC)仍能达到95%以上;亲和层析消毒间隔为3个循环时,填料的动态结合载量下降5.2%,下降幅度较小,且回收率未出现下降。因此,可将消毒时间定为25 h,并将亲和层析最大消毒间隔定为3个循环。
关键词:亲和层析填料;消毒时长;消毒间隔
1实验目的
随着生物制药行业的快速发展,大规模工业化生产技术逐渐成熟。其中,抗体作为免疫系统的核心组成部分,可预防和控制病原体传播,同时为再次感染提供长期保护。抗体包含2个完全相同的抗原结合片段(Fab)和1个可结晶片段(Fc)。蛋白A能够与抗体的Fc片段结合,用于抗体纯化。
亲和层析填料(MabCapture重组蛋白A)的动态结合载量在理论上会受到亲和层析消毒液(0.1M NaOH+1M NaCl)的影响,且与碱液接触时间越长,填料的动态结合载量降低越明显[1]。因此,明确碱液接触时间及填料动态结合载量的降低值,对于了解填料的经济性能有一定参考意义。
2实验过程
2.1材料(层析设备、介质、主要试剂)
AKTA-avant150层析系统;博格隆BXK10/20层析柱;MabCapture重组蛋白A亲和层析介质;NaOH;无水磷酸氢二钠;磷酸二氢钠一水合物;氯化钠;磷酸。按生产工艺要求配制平衡液、再生液、消毒液。疏水层析洗脱峰为笔者所在公司CMAB807产品完成疏水层析的中间产品。
2.2方法
工业化生产时的层板柱内径为700 mm,柱高为600 mm。实际使用时,装柱高度为18~22 cm。
本实验采用与生产相同的柱高,通过缩小柱直径的方式,实现线性的缩小模型,以测试碱液消毒时长及间隔对亲和层析填料(MabCapture重组蛋白A亲和层析介质)载量的影响。计划按实际工艺流程,以博格隆BXK10/20层析柱开展实验,取新的亲和层析填料装填层析柱并测试柱效合格,即建立scale down model。在江苏泰州迈博太科药业有限公司应用AKTA-avant150层析系统开展试验。试验时间为2023年7—9月。
2.2.1消毒时长对亲和层析填料(MabCapture重组蛋白A)载量的影响
亲和层析柱工艺中装柱高度可接受范围为18-22 cm,线性流速可接受范围为120~160 cm/h。据此,可计算出保留时间范围为6.75~11 min。在亲和层析消毒步骤中,规定消毒液清洗时间不超过15 min,消毒柱体积不少于1.5 CV。假设消毒步骤保留时间为T,消毒柱体积为V,关系式表达如下。
V(CV)×T(min)≤15(min)
若消毒柱体积取最小值1.5 CV,则消毒保留时间T≤10 min;若以100循环的填料寿命计算,100循环内消毒液与填料接触总时间为100×15=1 500 min,即25 h。本实验将研究消毒液与填料接触0~25 h内填料动态结合载量的变化。
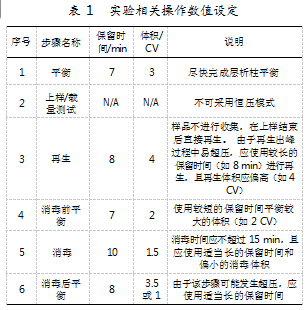
在亲和层析载量测试过程中,执行相应步骤的操作数值设置如表1所示。
在本项目中,疏水层析洗脱液成分为10 mM PB+200 mM硫酸铵,pH 6.8~7.2,电导率可接受标准为20~40 mS/cm。可见,疏水层析洗脱峰的pH和电导率与疏水层析洗脱液基本一致,且与深层过滤上清接近,适用于亲和层析填料载量的测试。因此,实验使用疏水层析洗脱峰进行亲和层析的动态载量测试。
本实验用于载量测试的疏水层析洗脱峰pH为6.75,电导率为38.37 mS/cm,蛋白质量质量浓度为6.3 g/L。
经过实验,得到填料动态结合载量下降百分比结果如表2所示。
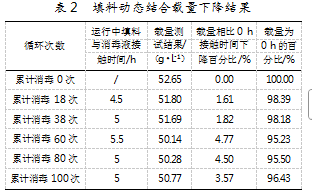
结果显示,随着填料与碱液接触时间的增加,DBC呈现下降趋势;在填料与碱液接触时间达到25 h后,DBC为初始值的96.43%,工艺固定生产用载量为DBC的80%。由此可知,累计消毒100次后,仍能满足生产的载量需求。
2.2.2消毒间隔对亲和层析填料(MabCapture重组蛋白A)载量的影响
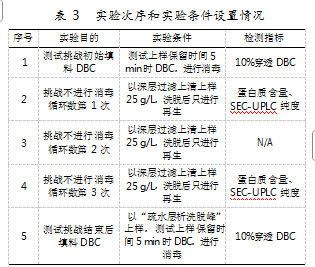
亲和层析消毒液中的碱液对亲和层析填料的动态结合载量有损害。若亲和层析在若干个循环后进行1次消毒,且确定若干个循环内不进行消毒以不影响收集液产品的质量,则可显著增加亲和层析填料的使用次数[2]。实验确定,亲和层析在3个循环内不消毒的情况下,对亲和层析的收集液产品质量、回收率和动态结合载量无影响。鉴于深层过滤上清中含有大量杂质,本实验决定采用工艺规程中最高上样载量25 g/L进行上样,并在所挑战的循环间隔数内(3个循环)只进行洗脱和再生,不执行消毒步骤,以比较所挑战的循环数前后填料动态结合载量、层析回收率和收集液产品质量的差别。若在执行挑战的循环后,动态结合载量和回收率未发生降低,且收集液产品质量未发生下降,则说明所挑战的循环间隔数成功[3]。实验次序和实验条件安排如表3所示。
本实验用于载量测试的疏水层析洗脱峰样品的pH为6.75,蛋白质质量浓度为6.3 g/L;用于上样的深层过滤上清样品的pH为7.19,蛋白质质量浓度为1.146 g/L。
实验过程参数及载量测试结果如表4所示。
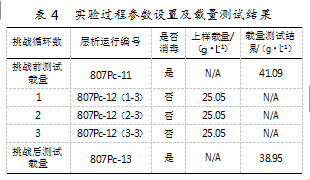
结果显示,挑战后的层析柱载量测试结果比层析前低5.2%,差距较小,可接受。
上样蛋白质质量浓度1.146 g/L,上样体积171 mL,上样蛋白总量196.65 mg。经过第一个循环后,亲和层析洗脱峰蛋白质质量浓度为16.3 g/L,SEC聚体为1.07%,SEC单体为98.76%,收集样品体积为10.36 mL,收集样品蛋白总量为168.87 mg,回收率达85.87%。最后一个循环后,亲和层析洗脱峰蛋白质质量浓度为17.6 g/L,SEC聚体为1.07%,SEC单体为98.74%,收集样品体积为10.32 mL,收集样品蛋白总量为186.91 mg,回收率为95.05%。
结果显示,挑战前后的多聚体含量相同,且均满足≤5%的可接受标准;挑战前后样品蛋白回收率未发生下降,且均满足80%~105%的可接受标准。
综上可知,在所挑战的3个循环不消毒前后,填料的动态结合载量仅下降5.2%,下降幅度较小,多聚体含量相同,且回收率在挑战后未发生下降,说明在亲和层析3个循环不消毒情况下,填料对目标蛋白的结合能力、填料的纯化能力和回收率未发生明显劣化,可将亲和层析最大消毒间隔定为3个循环。
3结论和建议
基于亲和层析填料与碱液接触时间对填料动态结合载量有影响,本实验挑战了亲和层析3个循环不消毒试验。结果显示,挑战前后其填料的动态结合载量、收集液的多聚体含量和回收率均未发生明显劣化。因此,可将亲和层析最大消毒循环间隔数定为3,结合循环消毒100次后,其DBC仍能满足生产的载量需求,可大幅提高填料使用次数。然而,在实际生产中,还需关注填料与消毒液的累计接触总时间,并结合载量变化或回收率变化情况定期监控填料动态。
参考文献
[1]郭子豪.高性能蛋白A亲和层析介质的制备、性能与应用研究[D].无锡:江南大学,2023.
[2]张玲,曹小丹,杨海旭,等.连续流层析技术在亲和层析中的应用及生产放大评估[J].中国生物工程杂志,2021,41(6):38-44.
[3]鲁伟,应国清,杨晓明,等.单克隆抗体工业生产中蛋白A亲和层析步骤的成本分析[J].高校化学工程学报,2023,37(2):276-284.










