超声波辅助低共熔溶剂提取胡萝卜中的番茄红素论文
2024-11-06 11:14:14 来源: 作者:dingchenxi
摘要:采用响应面分析法,利用超声辅助天然低共熔溶剂对胡萝卜中番茄红素的提取工艺进行优化。以番茄红素的提取率为评价指标,在单因素的基础上进行研究,选取pH、液料比和超声温度为因变量,进行Box-Behnken响应面实验设计和分析。
摘要:采用响应面分析法,利用超声辅助天然低共熔溶剂对胡萝卜中番茄红素的提取工艺进行优化。以番茄红素的提取率为评价指标,在单因素的基础上进行研究,选取pH、液料比和超声温度为因变量,进行Box-Behnken响应面实验设计和分析。结果表明,胡萝卜中番茄红素提取的最优组合为液料比5:1(g/mL),含水量10%的DES[n(氯化胆碱):n(乙酸)=1:2],超声温度40℃,提取时间20 min,调节pH值为3,在此条件下,番茄红素得率为18.41%。超声辅助天然低共熔溶剂对胡萝卜中番茄红素的提取有较好的效果,本研究为番茄红素的综合开发和利用提供依据。
关键词:番茄红素;低共熔溶剂;超声辅助提取;响应面法
胡萝卜[1]是伞形科胡萝卜属野胡萝卜的变种,含有丰富的类胡萝卜素[2],具有很高的食用和药用价值。番茄红素为类胡萝卜素中的一种化合物,由11个共轭碳-碳双键和2个非共轭碳-碳双键组成,在预防心血管疾病、保肝护眼、免疫调节、减慢人体老化速度以及在预防和对抗癌症方面发挥着重要作用[3-4],被认为是在自然界中消除自由基最强的物质之一。
传统的有机溶剂法提取番茄红素存在提取率较低、挥发性强、对人体和环境有害等问题,不符合绿色化学的概念[5-8]。低共熔溶剂[9](deep eutectic solvents,DES)是一种新型的绿色溶剂,由受氢体和供氢体组成的两组分或三组分低共熔混合物,具有绿色环保、制备简单、成本低、可生物降解等特点[10]。超声波辅助法是利用产生的空化作用,使细胞内可溶性物质快速释放、扩散并进入到提取剂中,具有省时、高效等特点[11-12]。因此,本实验利用超声波辅助低共熔溶剂提取胡萝卜中番茄红素,以单因素实验为基础,结合Box-Behnken响应面法,深入探究了胡萝卜中番茄红素的最佳提取工艺,以期为其综合开发利用提供一定的依据。
1材料与方法
1.1材料与仪器
胡萝卜为当日市售的新鲜胡萝卜,将新鲜成熟的胡萝卜洗净后削皮,切小块放入研钵中捣碎至糊状备用;氯化胆碱、二乙二醇、乙二醇,分析纯,上海易恩化学技术有限公司;乙酸乙酯、乙酸,分析纯,成都市科隆化学品有限公司;DL-乳酸、柠檬酸、1,3-丙二醇、丙三醇,分析纯,上海麦克林生化科技有限公司;尿素,分析纯,西陇科学股份有限公司。
电子分析天平:WTB2003,杭州万特衡器有限公司;超声波清洗器,AK-040,深圳钰洁清洗设备有限公司;高速离心机,LD-4,金坛区西城新瑞仪器厂;集热式恒温加热磁力搅拌器,DF-101S,上海力辰邦西仪器科技有限公司;紫外可见分光光度计,UV-5500,上海元析仪器有限公司。
1.2实验方法
1.2.1低共熔溶剂的制备
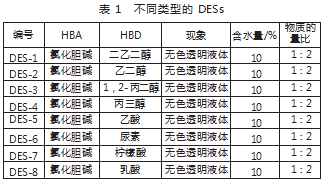
选择DES[13]氢键受体组与氢键供体组按照一定的摩尔比,在80℃下加热搅拌直至形成均匀、无色、透明液体为止,冷却至室温,密封保存。不同类型DES如表1所示。
1.2.2番茄红素的提取方法
精密称取研磨好的胡萝卜5 g,置于25 mL锥形瓶中,按照液料比(mL/g)5:1加入含水量10%的DES[n(氯化胆碱):n(乙酸)=1:2],振荡摇匀,温度40℃下超声提取20 min(240 W),将提取液在4 000 r/min下离心20 min,取上清液,调节pH值为3,待测。
1.2.3标准曲线的建立和番茄红素得率的计算
标准曲线的绘制:
根据李睿[14]的方法制作标准曲线,精确称取苏丹Ⅰ色素25 mg,以无水乙醇定容至25 mL。准确吸取0.06、0.12、0.18、0.24、0.30、0.36 mL溶液,置于编号为1~6的25 mL容量瓶中,用乙酸乙酯定容,在473 nm处测定吸光值,绘制标准曲线,得回归方程为y=0.284 6x+0.006,R2=0.999 9,在选定的浓度测量区间内,随着浓度的增大,吸光度值也随之增大。
番茄红素得率的计算:
向提取液中加入10 mL乙酸乙酯萃取,振荡摇匀,将上层液体取出0.5 mL用乙酸乙酯定容至25 mL,避光操作,以乙酸乙酯为空白,在473 nm处测定吸光值。
番茄红素得率计算见式(1):
Z=0.001ρBN/W.(1)
式中:Z为番茄红素含量,mg/g;ρ为回归方程计算得到番茄红素浓度,mg/L;B为乙酸乙酯萃取液体积,mL,取10 mL;N为稀释倍数,取50倍;W为胡萝卜质量,g,取5 g。
1.2.4单因素实验
精密称取研磨好的胡萝卜5 g,加入DES,在超声波辅助下提取番茄红素。以番茄红素的得率为指标,分别考察DES类型、DES的物持贩量比(2:1、1:1、1:2、1:3、1:4)、DES的含水量(0%、5%、10%、15%、20%)、pH值(1、2、3、4、5)、液料比(2:1、3:1、4:1、5:1、6:1)、超声时间(10、15、20、25、30 min)、超声温度(20、30、40、50℃)对得率的影响。
1.2.5 Box-Benhnken响应面实验
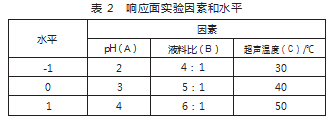
在单因素实验结果的基础上,选择对提取得率影响较大的三个因素即pH(A)、液料比(B)、超声温度(C)3个因素为自变量,以番茄红素提取得率(Y)为因变量,响应面因素水平见表2。
2结果与分析
2.1单因素实验结果
2.1.1 DES种类对番茄红素得率的影响
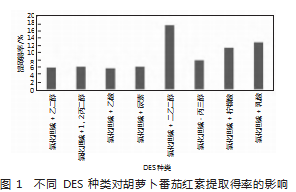
不同的DES具有不同的特性,其溶解性、黏度、密度、导电性等物理性质各不相同,这在很大程度上对番茄红素的提取效果产生影响[15]。本次实验将氯化胆碱作为了氢键受体,以醇基、酸基、碱基等作为氢键供体。由图1可知,DES-5(氯化胆碱+乙酸)对番茄红素的提取效果相对较好,原因可能是DES-5相对其他低共熔溶剂的黏度较小,故表面张力小,分散性好,使溶剂能更好地与目标分子接触,因此选择DES-5作为提取溶剂。
2.1.2摩尔比对番茄红素得率的影响
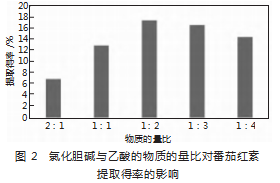
由图2可知,当n(氯化胆碱):n(乙酸)=1:2时番茄红素得率最高,这可能是因为不同的物质的量比会使DES的黏度和表面张力不同,物质的量比过低可能会使DES与待提取物的作用弱,难以将样品中的目标物提出,因此DES物质的量比确定为1:2。
2.1.3含水量对番茄红素得率的影响
由于DES本身具有较高的黏度、扩散能力比水差,因此较难进入到待提取样品内部,少量的水可以将DES的黏度降低到水的范围,并使某些DES的电导率提高100倍。由图3可知,随含水量的增加,番茄红素提取率先上升后下降,当其含水量为10%时,番茄红素得率达到了最大值。这可能是因为含水量达到一定值后,溶解出了更多杂质,与待提取物质竞争低共溶剂,从而减弱了低共熔溶剂与番茄红素成分间相互作用力,从而使目标成分得率下降[16]。因此DES含水量确定为10%。
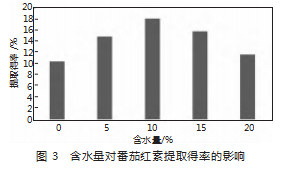
2.1.4 pH对提取番茄红素的影响
由图4可知,pH对番茄红素的提取得率影响较大,在酸性条件下随着pH的增加,番茄红素的提取率呈现出先升高后下降的现象,反映了番茄红素在酸性条件下化合物更加牢固,在近中性的条件下易被降解而失活。因此,选择pH为2、3、4作为响应面实验设计的三个水平。
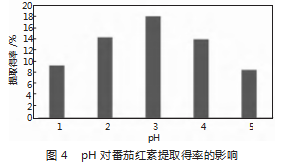
2.1.5液料比对番茄红素得率的影响
由图5可知,液料比对番茄红素的提取得率影响较大,在料液比1:5之前,番茄红素得率随料液比的增大而增大,料液比(g/mL)1:5之后番茄红素得率随料液比的增大而逐渐减小。其原因可能是在提取过程中,料液比增大可以增加进入细胞分子数,有利于提高传质的动力,从而番茄红素的得率提高。但当其比例增大到5:1时,继续加大料液比会使番茄红素重新吸附回待提取物中,不仅使提取率变低,还造成了溶剂的浪费。因此,选择液料比4:1、5:1、6:1作为响应面实验设计的三个水平。
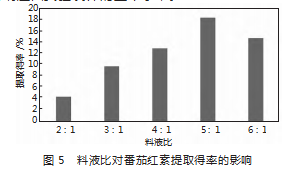
2.1.6超声时间对番茄红素得率的影响
由图6可知,随着超声时间的增加,其得率先升高后下滑,当超声时间为20 min时,番茄红素达最高得率,后随时间的变长得率反而下降,这可能是因为超声可以让胡萝卜中的目标成分与其他物质分离出来,但超声时间过长使部分番茄红素分解,因此超声时间确定为20 min。
2.1.7超声温度对番茄红素得率的影响
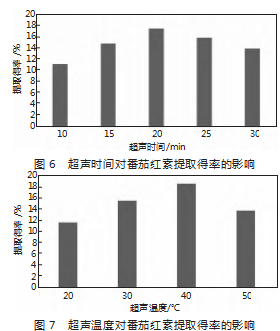
由图7可知,超声温度对番茄红素的提取得率影响较大,当提取温度达到为40℃时番茄红素的提取率最高,这也许是由于温度的提高有利于内部小分子的热运动,但温度过高使待提取中的热敏物质分解,杂质增多,同时,温度过高也会导致番茄红素的分解。因此,选择超声温度30、40、50℃作为响应面实验设计的三个水平。
2.2响应面实验结果与分析
利用Box-Behnken中心组合设计进行3因素3水平的响应面实验,方案及结果见表3。
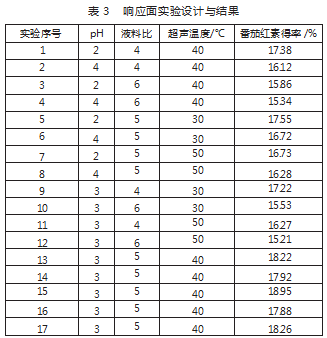
利用Design-Expert13软件对表3中的数据进行回归方程拟合,得到番茄红素得率的回归方程为:
Y=18.25-0.382 5A-0.631 3B-0.316 2C+0.185 0AB+0.095AC+0.157 5BC-0.654 2A2-1.42B2-0.771 8C2.
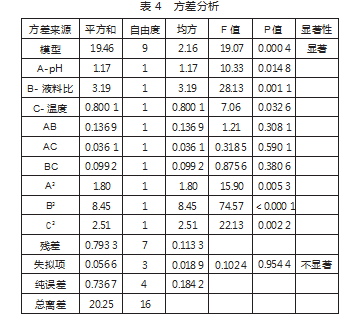
由回归模型方差分析结果可知,回归模型P值为0.000 4<0.01,表明回归模型极显著,失拟项P值为0.954 4>0.05,表明不显著,说明该模型与实验有良好的拟合性。模型的R2值为0.960 8,R2adj为0.910 5,
表明模型拟合度良好,两者均接近于1,表明该模型具有良好的准确度,实验误差相对较小,因此可用于分析和预测各种因素对胡萝卜中番茄红素提取得率的影响。此外,pH和液料比的P值小于0.01,表明了这两个因素对番茄红素的提取率影响极显著,超声温度的P值小于0.05,表明其对番茄红素的影响显著。根据F值的大小可以判断各因素影响程度为A(液料比)>C(pH)>B(超声温度)。方差分析结果见表4。
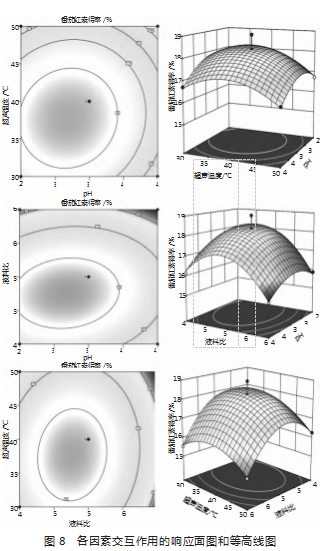
运用多元线性回归方程进行计算机模拟分析,可以揭示各因素之间相互影响的关系,等高线图越接近椭圆形,响应面图坡度越陡[18]。由图8可知,不同因素的对应值对响应值产生了明显的影响。
2.3工艺验证
根据Box-Behnken响应面法建立的模型,以最大得率为目标,预测番茄红素的最佳提取工艺为:pH为2.653,液料比为4.741,超声温度为37.474℃,在此条件下胡萝卜中番茄红素的提取得率为18.434%。考虑到实际操作,将最佳工艺参数调整为:pH=3,液料比为5:1,超声温度为40℃,在此条件下,胡萝卜中番茄红素的提取得率为18.41%,与理论值相近,参数可靠,可用于实际提取。
3结论
本研究利用超声波辅助低共熔溶剂提取胡萝卜中番茄红素,通过单因素实验结合Box-Behnken响应面法确定最优提取工艺为:液料比5:1,含水量10%的DES[n(氯化胆碱):n(乙酸)=1:2],超声温度40℃,提取时间20 min,调节pH值为3,在此条件下胡萝卜中番茄红素的提取得率为18.41%,本研究为胡萝卜中番茄红素的综合开发利用提供一定的依据。
参考文献
[1]颜文富.胡萝卜品种选择与种植技术[J].农业技术与装备,2022(9):174-176.
[2]李洪安,彭小强,刘思悦,等.紫甘薯和胡萝卜加工前后抗氧化协同作用变化[J].天然产物研究与开发,2023,35(1):118-130.
[3]Liang X,Ma C,Yan X,et al.Advances in research on bioactivity,metabolism,stability and delivery systems of lycopene[J].Trends in Food Science&Technology,2019,93:185-196.
[4]Mcclements D J.Nano-enabled personalized nutrition:Developing multicomponent-bioactive colloidal delivery systems[J].Advances in Colloid and Interface Science,2020,282:102211.
[5]张卫佳,陈家树.番茄红素有效成分的提取工艺及其解酒机制的研究[J].酿酒科技,2016(4):120-121.
[6]Ettorre A,Frosali S,Andreassim,et al.Lycopene PHytocomplex,but not pure lycopene,is able to trigger apoptosis and improve the efficacy of PHotodynamictherapy in HL60 human leukemia cells[J].Experi-mental Biology&Medicine(Maywood),2010,235(9):1114-1125.
[7]余越,黄先静,贺旭,等.4种贵州红酸汤中全反式番茄红素的提取及含量测定[J].中国调味品,2017(4):129-133.
[8]刘钰华,李佳,闫唯,等.超声波辅助提取圣女果番茄红素及其抗氧化活性研究[J].保鲜与加工,2017,17(2):73-77.
[9]秦淑淼,李秀萍,赵荣祥.CH3COOH/ZnCl2低共熔溶剂脱除模拟油中氮化物[J].石油炼制与化工,2020,51(4):37-42.
[10]Izadi R M,Haghbakhsh R,Raeissi S.Thermodynamic screening of various group contribution methods for estimation of the critical properties and acentric factors of deep eutectic solvents[J].Journal of Molecular Liquids,2024,399:124345.
[11]Eldin Elhag Abugabr Elhag H,Naila A,Ajit Aeldin Elhag Abugabr Elhag H,Naila A,Ajit A,et al.Sequential extraction of saponins from Eurycoma longifolia roots by water extraction and ultrasound-assisted extraction[J].Materials Today:Proceedings,2018,5(10):21672-21681.
[12]黄武,李亚杰,亢帅,等.超声辅助提取花生红衣中原花青素[J].食品研究与开发,2021,42(10):112-117.
[13]许光治,张有做.菜籽油低共熔溶剂萃取物DPPH自由基清除能力研究[J].中国粮油学报,2018,33(2):50-55.
[14]李睿.番茄中番茄红素提取工艺的比较研究[J].应用化工,2020,49(12):2994-2997.
[15]孙平,董萍萍,董丹华,等.超声波辅助低共熔溶剂提取野菊花总黄酮的工艺研究[J].食品工业科技,2020,41(20):147-152.
[16]Bi W T,Tian M L,Row K H.Evaluation of alcohol-based deep eu-tectic solvent in extraction and determination of flavonoids with re-sponse surface methodology optimization[J].Journal of Chromatog-raPHy A,2013,1285:22-30.
[17]赵文红,严婷婷,尹文婷,等.溶液pH对番茄红素稳定性及其降解动力学研究[J].现代食品科技,2020,36(1):178-183.
[18]A Gutiérrez,Atilhan M,Aparicio S.Molecular dynamics study on water confinement in deep eutectic solvents[J].Journal of Molecular Liquids,2021,339:116758.










