气相色谱 - 质谱联用技术检测水质中哌嗪含量论文
2024-06-28 10:38:48 来源: 作者:caixiaona
摘要:建立了一种气相色谱-质谱联用技术检测水质哌嗪含量的方法,在pH=9.5、60℃条件下,使用五氟苯甲酰氯成功衍生水中哌嗪,衍生物用乙酸乙酯萃取进GC-MS检测,方法回收率93.5%~106%,在质量浓度20~2 560 ng/mL范围内,哌嗪衍生产物有良好的线性,相关系数为0.999,检测限为6μg/L(信噪比为3),定量限为20μg/L(信噪比为10)。
摘要:建立了一种气相色谱-质谱联用技术检测水质哌嗪含量的方法,在pH=9.5、60℃条件下,使用五氟苯甲酰氯成功衍生水中哌嗪,衍生物用乙酸乙酯萃取进GC-MS检测,方法回收率93.5%~106%,在质量浓度20~2 560 ng/mL范围内,哌嗪衍生产物有良好的线性,相关系数为0.999,检测限为6μg/L(信噪比为3),定量限为20μg/L(信噪比为10)。
关键词:水质;哌嗪;五氟苯甲酰氯;衍生;气相色谱-质谱联用
0引言
哌嗪是一种医药中间体和精细化工原料,用途较为广泛,哌嗪及其衍生物主要用来制备喹诺酮类抗菌药、哌嗪利福霉素类抗生素、人用和兽用驱肠虫药,还用来制备精神类药物、心血管药物及抗肿瘤药物等。哌嗪毒性较低,但大量接触本品(口服、吸入、皮肤接触),能引起人体虚弱、视力模糊、共济失调、震颤、癫痫样抽搐。此外,哌嗪能引起高铁血红蛋白血症,影响血液携氧能力,出现头痛、头晕、恶心、紫绀。眼接触引起严重刺激和灼伤,对皮肤有刺激性。
![]()
哌嗪检测方法,有比色法[1-4],该方法适合分析质量浓度范围大于1μg/mL以上的样品;黄川徽、徐铜文[5]建立了紫外分光光度法,在244~275 nm波长下对0.001~0.50 mol/L哌嗪水溶液进行了检测,线性相关系数0.993以上;朱岩等[6]建立了阳离子色谱法检测哌嗪的方法,淋洗液为2 mmol/L盐酸溶液+2 mmol/L间苯二胺溶液,检出限为0.1μg/mL;甘冬彦、杨建玲、杨晓芸等[7]建立了高哌嗪中杂质乙二胺和哌嗪的气相色谱法(FID检测器)检测方法,方法考察了CPsil8 CB(30 m×0.25 mm×0.50μm)柱、HP-5(30 m×0.32 mm×0.25μm)柱、DB-624UI(30 m×0.32 mm×1.8μm)三种色谱柱,发现使用HP-5毛细管色谱柱分析乙二胺和哌嗪严重拖尾,当使用DB-624UI毛细管色谱分析时候基线不平并且杂峰干扰较多,而CPsil8 CB毛细管分析乙二胺和哌嗪时候峰形较为理想,哌嗪在20.4~163.6μg/mL质量浓度范围内线性关系良好,线性相关系数0.999以上,检出限为3μg/mL。李俊、王英瑛[8]建立了气相色谱法测定氧氟沙星和诺氟沙星中N-甲基哌嗪和哌嗪的残留量的方法,色谱柱考察了HP-FFAP、DB-624、HP-5三种不同的毛细管柱,结果发现N-甲基哌嗪和哌嗪在这3根色谱柱中均严重拖尾,而使用胺类专用色谱柱Agilent CAM毛细管柱(30.0 m×0.25 mm×0.25μm),程序升温方式分析,则可以得到较好的峰形,哌嗪在10.08~201.60μg/mL质量浓度范围内线性关系良好,线性相关系数0.999 5,检出限0.73μg/mL。气相色谱-质谱法有王雅娟、王波、张杨杨等[9],建立了乙酸酐法衍生哌嗪,气相色谱-串联质谱(GC-MS/MS)检测鸭子组织体内的哌嗪残留量的方法,EI离子源,扫描方式为SIM离子,哌嗪在4.5~2500μg/kg含量范围内线性关系良好,回收率高于84%,哌嗪在鸭组织的检出限为1.4~1.5μg/kg(S/N≥3)。赵霞、王波、崔璐璐等[10],也是采用乙酸酐衍生哌嗪,串联气质法检测鹅体内的哌嗪残留量。高效液相色谱法有张杨杨[11],建立了鸡组织、鸡蛋及猪肉中哌嗪残留量,样品经过提取/净化/浓缩后用丹磺酰氯作为衍生试剂,三乙胺做催化试剂,丹磺酰氯和哌嗪生成单取代衍生产物,再用高效液相-荧光检测器检测,在激发波长330 nm,发射波长531 nm条件下检测,最低检出限为0.5μg/kg。李欣、沈敏雅、杨倩等[12]建立了水中哌嗪的检测方法,方法使用对甲苯磺酰氯在碱性条件下衍生水中哌嗪,衍生产物经过液相质谱确认同时产生哌嗪-对甲苯磺酰氯的单取代和双取代两种产物,该方法定量采用了液相色谱-紫外检测器检测,波长为240 nm,哌嗪的衍生化产物与过量衍生化试剂分离良好,在10~100 mg/L的范围内,哌嗪的浓度与其衍生产物峰面积呈现良好的线性关系,相关系数r>0.999,方法的检出限为0.09 mg/L,定量限为0.30 mg/L。高效液相-串联质谱法有孙礼瑞[13],他在研究中发现丹磺酰氯和哌嗪衍生过程会产生单取代物和双取代物两种,单取物很少,主要为双取代物,这个与研究结果与张杨杨[11]不同,并且他认为丹磺酰氯-哌嗪双取代物极其不够稳定,容易发生降解,因此他采用高效液相-串联质谱法直接分析哌嗪含量,哌嗪在添加含量50.0~200.0μg/kg范围内,平均回收率在82.22%~88.63%,方法检出限为0.3μg/kg,文章中提及液质分析哌嗪含量可以省去衍生步骤,但要克服哌嗪在液相C18色谱柱上的保留时间过短、峰展宽、峰形拖尾等问题。食品国家标准[14]检测动物源食品中哌嗪也是采用此法,用1%氨水乙腈提取,过硅藻土柱净化,用高效液相-串联质谱测定,外标法定量哌嗪,测定低限为10μg/kg。
上述各类分析哌嗪的方法各有优点,也存在一些不足之处:如比色法[1-4]、分光光度法[5]所用设备资金投入最少,但方法专一性欠佳。离子色谱法[6]、气相色谱法[7-8]、液相色谱法[11-12]分析哌嗪专一性、灵敏度、稳定性都比分光光度法和比色法大大提高,但由于这三者均是靠色谱保留时间来定性哌嗪,因此当分析一些复杂基质样品的时候定性和定量会存在一定的问题。液相色谱-串联质谱法[13-14]和气相色谱-串联质谱法[9-10]定性能力强、检测限低、抗干扰性强,但仪器设备资金投入较大,不利于方法普及。总体而言,哌嗪由于相对分子质量小、极性强、无发光基团等因素,因此对分析工作者有较大的挑战性。我国为化工和制药生产强国,哌嗪的用量巨大,在哌嗪的生产过程和以哌嗪为原料制造下游产品过程中,哌嗪对于环境污染在所难免,尤其是对于水体的污染是值得关注的一个方向。而当前研究环境类水质哌嗪检测方法很少,建立一种适合环境水体方面的检测方法尤其重要。
1实验部分
1.1仪器和装置
7890A-5975C气相色谱-质谱联用仪器,配备EI离子源,安捷伦公司;烘箱,上海博迅实业有限公司医疗设备厂;水浴氮吹仪,上海安谱实验科技股份有限公司;万分之一电子天平,梅特勒公司。
1.2材料与试剂
无水哌嗪,标准物质,纯度99.5%,Dr.Ehrenstorfer公司;N-甲基哌嗪,标准物质,纯度99.5%,中国食品药品检定研究院;N-乙基哌嗪,色谱纯试剂,纯度≥99.5%,Amethyst公司;五氟苯甲酰氯,分析纯,纯度≥99.0%,北京百灵威科技有限公司;丙酮,农残级试剂,纯度≥99.8%,上海安谱实验科技股份有限公司;乙酸乙酯,农残级试剂,纯度≥99.8%,北京百灵威科技有限公司;碳酸钠,分析纯,纯度≥99.8%,天津科密欧化学试剂有限公司;氯化钠,分析纯,纯度≥99.8%,国药试剂化学有限公司;氢氧化钠,分析纯,纯度≥99.5%,天津科密欧化学试剂有限公司;盐酸,优级纯,体积分数≥32%,国药试剂化学有限公司;正己烷,农残级试剂,纯度≥95.0%,北京百灵威科技有限公司;二甲胺盐酸盐,分析纯,纯度≥99.6%,国药试剂化学有限公司;
碳酸钠缓冲溶液(pH=9.5):称取碳酸钠0.424 g,加入40 mL纯水溶解,用盐酸溶液调节pH至9.5,加水定容至50 mL;
氢氧化钠溶液:称取氢氧化钠10 g,加入100 mL纯水溶解,混合均匀后待用;
盐酸水溶液(1+1):量取100 mL盐酸和100 mL纯水混合,混合均匀后待用;稀盐酸溶液(1mol/L):吸取盐酸9~100 mL容量瓶内,加水定容至刻度;
二甲胺水溶液:称取二甲胺盐酸盐5 g,加入纯水100 mL溶解,混合均匀后待用。
1.3样品的采样、运输和保存
地表水、地下水、生活饮用水、污水的采样方案、布点、频次、设备、采样流程等要求参照对应的国家标准进行[15-19]。
1.3.1采样容器
选择玻璃瓶采集和保存水样,玻璃瓶带盖子可密封,采样前瓶子用10%盐酸(或硝酸)浸泡8 h,自来水清洗干净,烘干备用,必要时可用重铬酸钾洗液浸泡过夜,再洗净烘干后使用。
1.3.2样品运输和保存
采集水样体积500 mL~1000 mL,如样品含有可沉降固体的(如泥沙),应通过自然沉降方式或玻璃纤维滤膜过滤除去沉降物,用盐酸水溶液(1+1)调节水样到pH≤2,水样应充满容器溢出,加盖密封后进行运输,尽快送回实验室,如样品不能及时分析,应该于4℃下保存,5 d内应完成分析工作。
1.3.3采样的质量控制
每批次样品至少需要一个运输空白样品、一个全程序空白样品,平行样控制在样品总量的10%以上。
1.4样品前处理和衍生
水样的净化:污染比较严重的水样需净化处理,取100 mL样品到250 mL分液漏斗中,加入正己烷30 mL进行萃取,静置分层后弃去有机层,留下水层,同样方法再用正己烷净化一次,留下水样待用,如发生乳化现象,可加入适量的氯化钠破乳。样品若为干净的水样,则无需净化,直接进行下一步操作。
取水样50 mL,用氢氧化钠溶液调节pH至7,再加入碳酸钠0.424 g,搅拌溶解,用稀盐酸溶液调节pH至9.5。
用移液管准确移取水样1 mL到20 mL的顶空瓶内,加入丙酮1 mL,五氟苯甲酰氯15μL,加盖密封,放入60℃烘箱内衍生1 h(反应公式见图1)。

衍生完毕,将顶空瓶从烘箱拿出冷却至室温,开盖后加入二甲胺水溶液1 mL,涡旋30 s,二甲胺和顶瓶内残存的五氟苯甲酰氯反应,衍生反应终止。再将顶空瓶置于35℃水浴下氮吹至2 mL左右(氮吹的目的是去除反应体系中的丙酮),用移液管准确加入乙酸乙酯1 mL,另加氯化钠0.3 g,涡旋萃取30 s,静置分层后取乙酸乙酯层装入进样小瓶内,进气相色谱-质谱仪器分析。
1.5标准溶液的制作
用万分之一的天平称取无水哌嗪50 mg到50 mL容量瓶内,加入纯水溶解后定容至刻度,摇匀,配成质量浓度为1000μg/mL的哌嗪标准母液,用移液管移取10 mL哌嗪母液到100 mL容量瓶内,加入纯水定容至刻度,配成质量浓度为100μg/mL的哌嗪中间液,再用相同方法继续稀释,得10μg/mL和1μg/mL的哌嗪工作标准溶液。
取20 mL顶空瓶内5个,用200μL移液枪依次加入1μg/mL哌嗪工作液0、20、40、80、160μL,再用1 mL移液枪移取pH为9.5的水溶液1 000、980、960、920、840μL按顺序加入这5个顶空瓶内,使得5个顶空瓶子中液体体积均为1mL,哌嗪溶液的质量浓度分别为0、20、40、80、160 ng/mL。再另取顶空瓶4个,用200μL移液枪依次加入10μg/mL哌嗪工作液32、64、128、256μL,同样用1 mL移液枪补加pH为9.5的水溶液968、936、872、744μL,使得这4个顶空瓶内的哌嗪标液质量浓度为320、640、1 280、2 560 ng/mL。上述质量浓度为0、20、40、80、160、320、640、1 280、2 560 ng/mL共9个顶空瓶中各加入丙酮1 mL,五氟苯甲酰氯15μL,加盖密封,放入60℃烘箱内衍生1 h,其余操作同“1.4”。
1.6气相色谱-质谱分析条件
汽化室温度设置:280℃;辅助温度:300℃;离子源温度:230℃;色谱柱:Thermo Fisher TG-5MS毛细管色谱柱,30 m×0.25 mm×0.25μm;柱温:85℃保持2 min,以30℃/min速度上升到300℃,保持2 min;进样方式:不分流进样,40 s后分流开启;进样量:1μL。
哌嗪衍生产物定性:配置质量浓度为10μg/mL的N-甲基哌嗪、N-乙基哌嗪、哌嗪混合标液,按照标准溶液衍生步骤处理,进气相色谱-质谱联用仪全扫描(质荷比为50~550),确定出哌嗪以及同系物的N-甲基哌嗪、N-乙基哌嗪的出峰时间和质谱离子情况(图2为N-甲基哌嗪、N-乙基哌嗪、哌嗪的五氟苯甲酰氯衍生产物的气质总离子流图;图3为N-甲基哌嗪的五氟苯甲酰氯衍生产物质谱图;图4为N-乙基哌嗪的五氟苯甲酰氯衍生产物质谱图;图5为哌嗪的五氟苯甲酰氯衍生产物质谱图)。
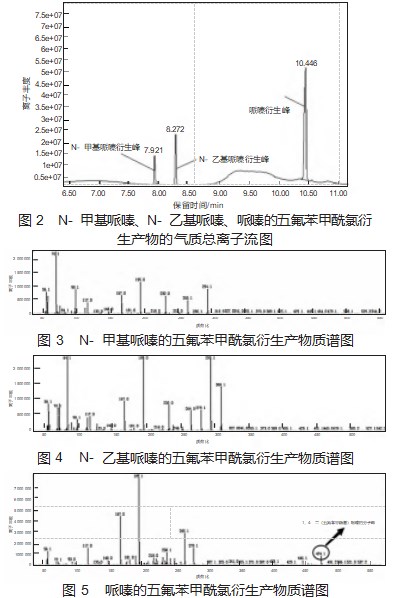
哌嗪定量质谱扫描方式:选择离子扫描,溶剂延迟6.5 min,扫描离子质荷比为195、265、279、474,定量离子(质荷比为474)为哌嗪双取代衍生产物的质谱分子峰,定性离子质荷比为195、265、279。
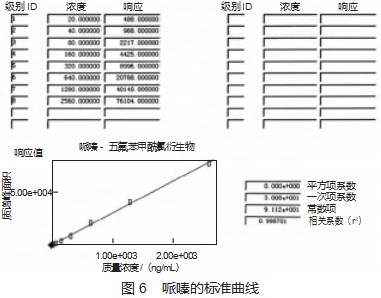
定量方式:外标法,标准曲线的线性方程为Y=30.08X+91.12,线性决定系数R2为0.998,线性相关系数R为0.999(图6哌嗪的标准曲线)。
1.7方法检出限
通过水样加标方式来确定检出限,3倍噪音比确定哌嗪检出限为6 ng/mL,10倍信噪比确定了定量限为20 ng/mL;当取水样1 mL分析,水中哌嗪的检出限为6μg/L,定量限为20μg/L。
1.8精密度和回收率
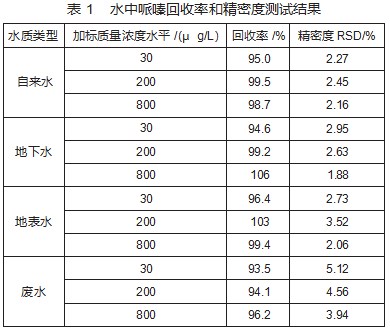
取自来水、地下水、地表水、废水4种基质的水样,进行加标回收率和精密度实验,水样分低(30μg/L)、中(200μg/L)、高(800μg/L)3个加标质量浓度水平进行,同一种基质同一个质量浓度进行6个样品测试,计算加标回收率和精密度。测试结果如表1。4种基质水样回收率在93.5%~106%,精密度RSD在1.88%~5.12%。
2结果讨论
2.1溶剂加入量的影响
室温下,1 mL丙酮和1 mL水样组合体系未能充分溶解15μL的五氟苯甲酰氯,在1 mL水存在条件下,丙酮一直要加入3 mL后五氟苯甲酰氯才能充分溶解(水样和丙酮体积比1∶3),但按照这个比例进行实验,测试下来标准曲线不成线性,主要原因是五氟苯甲酰氯和哌嗪在体系中浓度被过度稀释,导致衍生不充分。因此,本方案还是采用丙酮和水样体积1 mL+1 mL、15μL的五氟苯甲酰氯的方式进行,在稍微加热情况下(40℃或以上),五氟苯甲酰氯溶解度迅速提高,是可以完全溶解到体系中的,衍生反应顺利进行。
2.2衍生体系的pH对衍生效果的影响
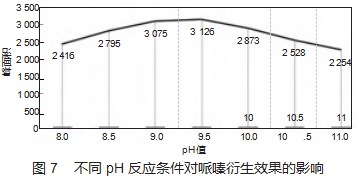
100 ng/mL的哌嗪标液1 mL,加入五氟苯甲酰氯15μL和1mL丙酮,在pH为8.0、8.5、9.0、9.5、10、10.5、11的条件下于60℃衍生1 h,样品处理后进气相色谱-质谱联用仪器分析后,比较不同pH条件下哌嗪衍生物峰面积大小(质荷比为474提取离子峰面积),结果如图7。从图7可以看出,五氟苯甲酰氯和哌嗪适合反应的pH范围是9~10,当pH达到9.5时可以得到最大的衍生峰。若反应体系pH过低,不利于甲酰化反应进行,例如当pH=8.0时衍生峰面积相当于pH=9.5衍生峰面积的77.3%;而当pH过高时则五氟苯甲酰氯会过早水解成五氟苯甲酸,进而失去和哌嗪反应的能力,衍生效果也会变差,例如当pH=11时衍生峰面积相当于pH=9.5衍生峰面积的72.1%;,从实验结果看,pH=9.5是进行衍生反应最优pH条件。
2.3衍生温度的影响
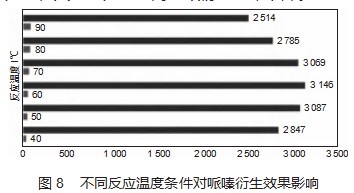
为了探究反应温度对衍生效果的影响,100 ng/mL的哌嗪标液1 mL,在pH=9.5条件下,加入五氟苯甲酰氯15μL和1mL丙酮,在40、50、60、70、80、90℃这几个温度点下进行衍生实验,样品处理后进气质联用仪器分析后得到如图8结果。通过实验发现,60℃是最佳衍生温度,50、70℃衍生的效果跟60℃相比差异很小,显著区别的是低于50℃和高于80℃的条件,如40℃温度衍生峰面积是60℃衍生峰面积的90.5%,80℃衍生峰面积是60℃衍生峰面积的88.5%,90℃衍生峰面积是60℃衍生峰面积的79.9%,说明五氟苯甲酰氯和哌嗪反应仅需比较温和的温度,太高的温度反而导致衍生收率下降。
2.4衍生时间的影响
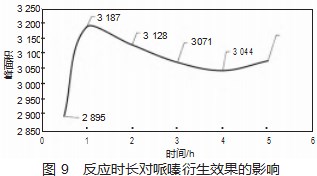
对于衍生时间对哌嗪衍生收率的影响,本实验设置0.5、1、2、3、4、5 h这6种衍生时长分别实验,衍生哌嗪标准溶液质量浓度为100 ng/mL,pH=9.5,五氟苯甲酰氯15μL,衍生温度60℃。测试结果如图9。通过实验发现,哌嗪和五氟苯甲酰氯反应十分迅速,0.5 h衍生峰面积即可达到1 h衍生的峰面90.8%,1 h反应时长便可以达到最高的收率,之后下降,但极其缓慢。因此,从衍生收率和衍生效率考虑,60℃衍生1 h是最优所需的衍生时长。
2.5衍生试剂用量的影响
五氟苯甲酰氯用量为10、20、30、40、50μL,质量浓度100 ng/mL的哌嗪衍生峰面积均无明显变化,考虑到经济性和充分性,本方法使用15μL的五氟苯甲酰氯。
2.6衍生产物的稳定性
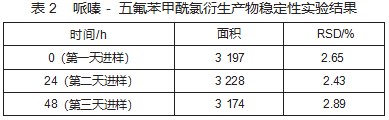
最优的衍生的条件下,制备100 ng/mL哌嗪标准溶液6个,样品当天进样测试后,更换成新进样盖子(加内垫),置于3~5℃的冰箱内保存,每隔24 h进行一次复测(复测前样品恢复至室温后进样),记录下数据,计算平均值和相对标准偏差,一共连续进行3 d,结果如表2。从3 d测试结果来看,哌嗪-五氟苯甲酰氯衍生产物的稳定性很好,在48 h内基本保持稳定。
3结论
本研究的实验条件下五氟苯甲酰氯和哌嗪衍生的产物均为“1,4-二(五氟苯甲酰基)哌嗪”,未检测到单取代物存在,双取代产物的稳定性很好,这点有别于对甲苯磺酰氯[12]、丹磺酰氯[13]衍生哌嗪。实验所用试剂便宜易得,方法的重复性、回收率、线性、检出限等均让人满意。当前现有技术中尚未见有环境水质哌嗪的GC-MS检测方法,本研究在这方面作了一些科学探索,有利于降低了仪器门槛(相对于GC-MS/MS和HPLC-MS/MS),提高了哌嗪检测的定性能力(相对于气相色谱、液相色谱、离子色谱),为后续研究工作者研究哌嗪检测提供一些检测思路。
参考文献:
[1]Senthilraja M.Colorimetric method for the determination of piperazine in pharmaceuticalformulations[J].Indian journal of pharmaceutical sciences,2006,68(6):843.
[2]Pankratz R E.Determination of piperazine salts in pharmaceutical liq-uids[J].Journal ofpharmaceutical sciences,1961,50(2):175-177.
[3]DessoukyY M,Ismaicl S A.Colorimetric determination of piperazine in pharmaceuticalformulations[J].Analyst,1974,99(1181):482-486.
[4]Wahbi A A M,Abounassif MA,Gad-KariemE A.Colorimetric deter-mination of piperazine withp-benzoquinone[J].Talanta,1986,33(2):179-181.
[5]黄川徽,徐铜文.紫外分光光度法快速测定哌嗪[J].南京工业大学学报(自然科学版),2005,27(2):122-24.
[6]朱岩,刘学健,陆州舜,等,离子色谱法测定哌嗪[J].化学世界,1994(3):150-152.
[7]甘冬彦,杨建玲,杨晓芸,等.GC法测定高哌嗪中乙二胺和哌嗪的残留量[J].药物评价研究,2020,43(6):1071-1074.
[8]李俊,王英瑛.GC测定氧氟沙星和诺氟沙星中N-甲基哌嗪和哌嗪的残留量[J].中国现代应用药学,2013,30(3):319-321.
[9]王雅娟,王波,张杨杨,等.气相色谱-串联质谱法检测鸭组织中哌嗪的残留[J].中国兽医学报,2018,38(7):1375-1380.
[10]赵霞,王波,崔璐璐,等.气相色谱-串联质谱检测鹅组织中哌嗪残留[J].分析试验室,2017,36(12):1423-1428.
[11]张杨杨.鸡组织、鸡蛋及猪肉中哌嗪残留柱前衍生—液相色谱荧光检测法的研究[D].扬州:扬州大学,2018.
[12]李欣,沈敏雅,杨倩,等.对甲基苯磺酰氯柱前衍生法测定水中哌嗪[J].分析试验室,2012,31(12):48-52.
[13]孙礼瑞.鸡肌肉中哌嗪残留液相色谱-串联质谱确证分析方法的研究[D].扬州:扬州大学,2015.
[14]江西出入境检验检疫局,湖北出入境检验检疫局,上海出入境检验检疫局,等.进出口动物源性食品中哌嗪残留量检测方法液相色谱-质谱/质谱法:SN/T 2317—2009[S].北京:国家质量监督检验检疫总司,2009.
[15]地表水环境质量监测技术规范:HJ/T 91.2-2022[S].2022.
[16]地块土壤和地下水中挥发性有机物采样技术导则:HJ 1019—2019[S].2019.
[17]地下水环境监测技术规范:HJ 164-2020[S].2020.
[18]污水监测技术规范:HJ 91.1—2019[S].2019.
[19]生活饮用水标准检验方法第2部分:水样的采集与保存:GB/T 5750.2—2023[S].2023.










