清胰利胆颗粒联合艾司奥美拉唑对急性胰腺炎预后的影响论文
2024-04-25 14:00:44 来源: 作者:hemenglin
摘要:目的 研究清胰利胆颗粒联合艾司奥美拉唑对急性胰腺炎( AP )患者炎症因子及预后的影响, 为提高该疾病的治疗效果提供 依据。方法 以随机数字表法将 2020 年 7 月
【摘要】目的 研究清胰利胆颗粒联合艾司奥美拉唑对急性胰腺炎( AP )患者炎症因子及预后的影响, 为提高该疾病的治疗效果提供 依据。方法 以随机数字表法将 2020 年 7 月至 2023 年 7 月于牡丹江医学院附属第二医院进行治疗的 60 例 AP 患者分为两组, 各 30 例。 给予对照组患者单纯艾司奥美拉唑进行治疗, 联合组患者接受清胰利胆颗粒联合艾司奥美拉唑治疗, 两组均治疗 7 d。比较两组患者临床 治疗效果, 治疗前后炎症因子及急性生理与慢性健康评分系统Ⅱ( APACHE Ⅱ)、 Ranson 评分、急性胰腺炎严重程度床边指数( BISAP ) 评分,以及治疗期间不良反应发生情况。结果 联合组患者治疗总有效率高于对照组;与治疗前比,治疗后两组患者血清白细胞介素 -6 ( IL-6 )、肿瘤坏死因子 -α( TNF-α ) 水平均降低, 联合组均较对照组更低;血清白细胞介素 -10( IL-10 )水平升高, 联合组均较对照组 更高;与治疗前比, 治疗后两组患者 APACHE Ⅱ、 BISAP 、Ranson 评分均降低, 联合组均较对照组更低(均 P<0.05 );对照组与联合组 不良反应总发生率比较( 13.33% 对比 6.67% ),差异无统计学意义(P>0.05 )。结论 清胰利胆颗粒联合艾司奥美拉唑可以显著提高 AP 治疗效果,减轻炎症反应,改善预后,且安全性良好。
【关键词】 急性胰腺炎 ; 清胰利胆颗粒 ; 艾司奥美拉唑 ; 炎症因子 ; 预后
急性胰腺炎(acute pancreatitis, AP)是一种起病急、 变化快的胰腺炎症性疾病,主要由饮食习惯差、胆道疾 病因素所致,临床主要表现为腹痛,对患者生活质量造 成严重影响。目前, AP 的主要治疗措施是采用抗炎、抑 制消化酶分泌等进行对症治疗,尚无特效治疗方法。奥 美拉唑为质子泵抑制剂,是治疗 AP 的常用药物之一,能 够抑制胃酸分泌,改善患者临床症状,但长期用药可能 会增加胃肠道感染的风险 [1]。在中医学理论指导下, AP 属于“腹痛”“胃心痛”等范畴,中医治疗的原则是行气 活血、清热解毒。清胰利胆颗粒是一种含有多种药用植 物和矿物质的中药制剂,具有调和脾胃、益气通经、活 血止痛、疏肝利胆的功效,可有效促进胃肠蠕动 [2-3] , 为 提高 AP 临床治疗有效性和安全性,在西药常规治疗的基 础上联合中药治疗已成为热门研究,基于此,本研究旨 在探讨清胰利胆颗粒联合艾司奥美拉唑对 AP 患者预后的 影响,现报道如下。
1资料与方法
1.1一般资料 以随机数字表法将 2020 年 7 月至 2023 年 7 月于牡丹江医学院附属第二医院进行治疗的 60 例 AP 患者分为两组, 各 30 例。对照组患者中男性 20 例, 女 性 10 例;年龄 30~55 岁, 平均(43.02±3.77)岁;病程 1~2 d,平均(1.20±0.20)d。联合组患者中男性 21 例,女性 9 例;年龄 29~54 岁,平均(43.01±3.98)岁;病程 1~2 d,平均(1.26±0.21)d。两组一般资料比较,差异无 统计学意义(P>0.05),可比。纳入标准:⑴符合《急性 胰腺炎诊治指南(2019 年,沈阳)》[4] 中 AP 的诊断标准, 主要临床症状为急性、剧烈、持续的中上腹疼痛,往往在 暴饮暴食或极度疲劳之后发生,多为突然发作,疼痛为持 续性进行性加重,似刀割样,疼痛向背部、肋部放射等; 且符合中医《急性胰腺炎中西医结合诊治方案》 [5] 中“腹 痛”的诊断标准,主症为急性腹痛腹胀,次症为恶心呕 吐、发热等,舌象为舌质暗红,舌苔白腻、黄厚,脉象为 脉弦、滑数等,辨证为肝郁气滞型;⑵对本次研究所使用 的药物无过敏史;⑶腹痛急性发作不超过 7 d。排除标准: ⑴处于妊娠期或者哺乳期;⑵合并胆道梗阻及自身免疫系 统类疾病;⑶患有胰腺假性囊肿或者胰腺癌。研究获得牡 丹江医学院附属第二医院医学伦理委员会批准,患者签署 知情同意书。
1.2治疗方法 患者入院后均接受禁食禁饮、持续胃肠 减压、营养支持及纠正水、电解质和酸碱平衡等常规治疗 方法。给予对照组患者注射用艾司奥美拉唑钠(开封康诺 药业有限公司,国药准字 H20233560.规格: 20 mg)静 脉滴注治疗,将 40 mg 该药物与 100 mL 0.9% 的氯化钠 溶液进行混合, 1 次 /12 h。联合组患者在对照组的基础上 采用清胰利胆颗粒(吉林巨仁堂药业股份有限公司,国药准字 Z22025312.规格: 10 g/ 袋) 口服治疗, 10 g/ 次, 3 次 /d,两组患者均连续治疗 7 d。
1.3观察指标 ⑴临床疗效:治疗后评估两组患者治疗 效果,显效:腹痛、腹胀、呕吐等症状缓解,肠鸣音恢 复,血和尿淀粉酶水平、血常规、肝功能检查均接近正 常,胰腺水肿程度较之前腹部 B 超、CT 检查有显著改善; 有效:症状缓解,肠鸣音存在但微弱,血和尿淀粉酶水 平、血常规、肝功能检查均明显改善,胰腺水肿程度较 之前腹部 B 超、CT 检查有轻微改善;无效:症状未缓解, 肠鸣音未恢复,血和尿淀粉酶水平、血常规、肝功能检 查及胰腺水肿程度均较治疗前无明显变化 [4]。治疗总有效 率 = 显效率 + 有效率。⑵炎症因子:于治疗前后空腹状 态下抽取患者静脉血 3 mL,离心(15 min,3 500 r/min), 取上层血清,采用酶联免疫吸附法测定血清白细胞介 素 -6(IL-6)、肿瘤坏死因子 - α(TNF-α ) 及白细胞介 素 -10(IL-10)水平。⑶预后指标:治疗前后采用急性生 理与慢性健康评分系统Ⅱ(APACHE Ⅱ) [6]、Ranson [7]、急 性胰腺炎严重程度床边指数(BISAP)[8] 评分评估两组患 者病情严重程度, APACHE Ⅱ评分包括急性生理、年龄、 慢性健康评分 3 部分, 总分范围 0~71 分, 分数越高, 病 情越严重;Ranson 包括 5 项入院时的临床指标和 48 h 内的 6 项指标,共计 11 项,每项指标记 1 分,总分为 11 分, 分数越高代表病情越严重;BISAP 评分总分 5 分,分数越 高代表病情越严重。⑷不良反应:记录两组患者治疗期间 包裹性胰腺坏死假性囊肿、器官衰竭的发生情况。不良反 应总发生率等于各项发生率之和。
1.4统计学方法 采用 SPSS 22.0 统计学软件分析数据, 计数资料以 [ 例 (%)] 表示,采用 χ2 检验;计量资料经 S-W 法检验证实符合正态分布,以 ( x ±s) 表示,组间比较采用独立样本 t 检验,组内治疗前后比较采用配对 t 检 验。P<0.05 表示差异有统计学意义。
2结果
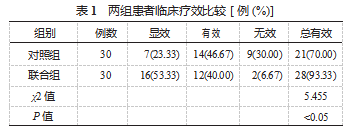
2.1两组患者临床疗效比较 与对照组总有效率比,联 合组较高,差异有统计学意义(P<0.05),见表 1.
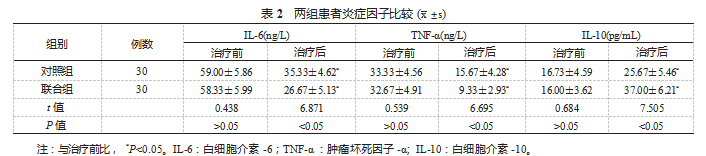
2.2两组患者炎症因子比较 与治疗前比,治疗后 两组血清 IL-6、TNF- α 均降低,血清 IL-10 升高,联 合组较对照组变化幅度均较大,差异均有统计学意义 (均P<0.05),见表 2.
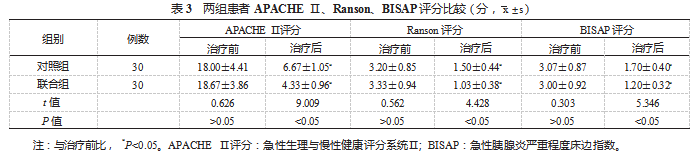
2.3两组患者 APACHEⅡ、Ranson、BISAP评分比 较 与治疗前比, 治疗后两组各项评分均降低, 联合组 APACHE Ⅱ、Ranson、BISAP 评分均较对照组更低,差异 均有统计学意义(均P<0.05),见表 3.
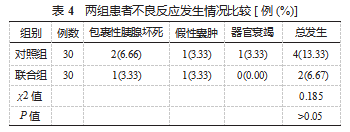
2.4两组患者不良反应发生情况比较 对照组与联合组 不良反应总发生率比较(13.33% 对比 6.67%),差异无统 计学意义(P>0.05),见表 4.
3讨论
AP 是一种剧烈急性炎症性疾病,病因众多,包括胆 道疾病、酗酒及不合理饮食等,这些因素可能触发病理性 细胞通路和细胞器功能障碍,最终导致腺泡细胞死亡、局 部及全身炎症,从而导致不可逆的胰腺组织损伤和功能障 碍。奥美拉唑可以通过减少胃酸分泌抑制胰腺分泌,但长 期用药可能引发胃肠道菌群失调,加之由于 AP 复杂的发 病机理,单一药物可能不足以治疗 AP。
中医将 AP 归为“腹痛”“内痈”,中医认为,脏腑 炎症可能是由于邪气、湿热蕴结所致;气滞则血瘀,湿则 胀满,当邪热炽盛时,就会形成内痈,治疗应以行气活 血、泻下邪热为原则。清胰利胆颗粒药物是一种中成药, 主要成分包括黄芩、黄连、木香等中药,具有清热解毒、 利胆止痛等功效 [9]。本研究将其与艾司奥美拉唑及常规治 疗联合应用,结果显示,联合组患者治疗总有效率高于对 照组,这说明清胰利胆颗粒联合艾司奥美拉唑治疗 AP 可 以提高临床治疗效果。分析原因,清胰利胆颗粒方中柴胡 疏泄肝胆,解郁止痛,为君药;牡蛎入肝经,软坚散结, 姜黄破血行气,通经止痛,两药合用,疏肝利胆,软坚散 结,行气活血止痛,为臣药;大黄活血祛瘀,通腑降浊, 延胡索行气活血止痛;牡丹皮、赤芍活血,消肿止痛;金 银花清热解毒,共为佐药;诸药合用,共奏行气解郁、活 血止痛、疏肝利胆之效,符合 AP 的治疗理论 [10]。
TNF-α 是一种早期促炎因子,IL-6 能够产生广泛的促 炎作用, 导致组织损伤, IL-10 是一种抗炎症细胞因子, 能 够抑制炎症介质的产生 [11]。通过分析两组炎症因子变化情 况发现, 治疗后联合组患者血清 TNF-α、IL-6 水平均低于对 照组, 血清 IL-10 高于对照组, 这说明清胰利胆颗粒联合艾 司奥美拉唑治疗 AP 可减轻炎症反应。清胰利胆颗粒不仅通 过调节促炎和抗炎反应, 削弱 AP 中的侵袭性因子和增强保 护性因子,对胃黏膜损伤发挥保护作用,还可以改善患者 系统微环境炎症,减轻胰腺腺泡细胞的凋亡,促进胰腺的 修复。药理学研究表明,清胰利胆颗粒中大黄可通过抑制 白三烯 B4 的生成, 发挥其抗炎作用 [12],柴胡皂苷能兴奋下 丘脑-垂体- 肾上腺皮质内分泌轴, 促进垂体分泌促肾上腺 皮质激素(ACTH),增强糖皮质激素的抗炎作用 [13]。
另外, 本研究中, 治疗后联合组 APACHE Ⅱ、Ranson、 BISAP 评分均低于对照组, 这提示清胰利胆颗粒联合艾司 奥美拉唑治疗 AP,可改善患者预后。分析原因, 清胰利胆 颗粒还可增加肠黏膜的密度、高度及面积,并上调肠道组 蛋白的水平,从而抑制肠道通透性和细菌从肠道的移位, 改善 AP 引起的肠屏障损伤,进而改善预后 [14]。本研究对 比两组安全性结果可见,差异无统计学意义,这说明清胰 利胆颗粒联合艾司奥美拉唑治疗 AP,安全性良好。分析其原因可能与清胰利胆颗粒种各有效成分均不会破坏肠道菌 群有关。
综上,清胰利胆颗粒联合艾司奥美拉唑可以显著提高 AP 治疗效果, 减轻炎症反应, 改善预后, 且安全性良好, 值得在临床上加以推广。
参考文献
[1] 孙笑非 , 许保海 . 疏肝利胆汤加味治疗急性胰腺炎 ( 肝胆湿热证 ) 的疗效分析 [J]. 中国中医急症 , 2023. 32(1): 127-129.
[2] 李梦阁 , 党志博 , 张广玉 , 等 . 中药三联疗法联合西医常规治疗 重症急性胰腺炎瘀毒互结证患者 41 例临床观察 [J]. 中医杂志 ,2021. 62(11): 961-965.
[3] 王军 . 清胰利胆颗粒联合乌司他丁和生长抑素治疗急性重症胰 腺炎的临床研究 [J]. 现代药物与临床 , 2016. 31(9): 1477-1481.
[4] 中华医学会消化病学分会胰腺疾病学组 , 《中华胰腺病杂志》编 委会 , 《中华消化杂志》编委会 . 中国急性胰腺炎诊治指南 (2019 年 , 沈阳 )[J]. 临床肝胆病杂志 , 2019. 39(11): 721-730.
[5] 中国中西医结合学会消化系统疾病专业委员会 . 急性胰腺炎中 西医结合诊治方案 [J]. 中国中西医结合消化杂志 , 2011. 19(3):207-209.
[6] 王露 , 黄兰 , 邵颖颖 , 等 . 急性生理功能和慢性健康状况评分系 统Ⅱ及严重程度床边指数评分对急性胰腺炎病情变化的预测价 值研究 [J]. 中国全科医学 , 2011. 14(32): 3693-3695.
[7] 蓝远强 , 黄丽珍 , 梁敏 , 等 . 血清学指标和相关评分系统预测 及诊断急性胰腺炎严重程度的进展 [J]. 现代消化及介入诊疗 ,2020. 25(11): 1539-1542.
[8] 张嘉 . 杨骥 . BISAP 评分系统对急性胰腺炎严重程度评估的荟萃 分析 [J]. 中华胰腺病杂志 , 2014. 14(3): 149-153.
[9] 毛庆峰 , 胡鹏 , 郝加庆 . 清胰利胆丸联合丙氨酰谷氨酰胺注射 液治疗老年重症急性胰腺炎的临床研究 [J]. 现代药物与临床 ,2023. 38(3): 655-659.
[10] 何健 , 俞隼 , 张静 . 血清 IL-6 和 TNF-α 对重症急性胰腺炎的早期 诊断价值分析 [J]. 临床肝胆病杂志 , 2023. 39(7): 1657-1664.
[11] 徐军鹏 , 张建峰 . 清胰利胆颗粒联合埃索美拉唑对老年急性胰腺 炎患者炎性介质和肠黏膜屏障功能的影响 [J]. 中国现代医学杂 志 , 2021. 31(8): 93-96.
[12] 李京心 , 张梦颖 , 郭瑞敏 , 等 . 大黄素通过抗炎作用抑制肺泡Ⅱ 型上皮细胞凋亡对急性肺损伤的治疗作用 [J]. 中国临床药理学 杂志 , 2022. 38(22): 2711-2715.
[13] 成睿珍 , 张春艳 . 柴胡皂苷类药理活性的研究进展 [J]. 职业与健 康 , 2021. 37(4): 568-572. 576.
[14] 张昔伟 , 张伟戈 , 王林恒 , 等 . 清胰利胆合剂灌肠在 ERCP 术后胰 腺炎和高淀粉酶血症预防中的作用及对炎症因子的影响 [J]. 山 东医药 , 2019. 59(28): 52-55.










